
【题目】按要求填空
(1)干冰是固态CO2的俗称,常用于人工降雨,44g干冰与A,B,C,D有如图所示的转化关系,请完成如图中的方框. 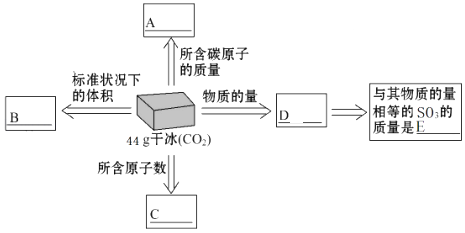
(2)标准状况下22.4L的HCl溶于水配成500mL溶液,所得溶液的物质的量浓度为 .
(3)配制1L 0.5molL﹣1NaOH溶液,需要1.25molL﹣1的NaOH溶液的体积是mL.
(4)19g MgX2含有Mg2+0.2mol,则MgX2的摩尔质量为 .
【答案】
(1)12g|22.4L|1.806×1024|1mol|64g
(2)2mol/L
(3)400
(4)95g/mol
【解析】解:(1)D.44g干冰的物质的量为: ![]() =1mol;
=1mol;
B.标准状况下该二氧化碳占有的体积为:1mol×22.4L/mol=22.4L;
C.所含原子物质的量为干冰的3倍,含有原子数目=1mol×3×6.02×1023mol﹣1=1.806×1024;
A.根据C原子守恒得n(C)=n(CO2),C原子的质量m=nM=1mol×12g/mol=12g;
E.三氧化硫与二氧化碳的物质的量相等,则该三氧化硫的质量m=nM=1mol×64g/mol=64g,
故答案为:12g;22.4L;1.806×1024;1mol;64g;(2)n(HC)= ![]() =1mol,c(HCl)=
=1mol,c(HCl)= ![]() =2mol/L,故答案为:2mol/L;(3)1L 0.5molL﹣1NaOH,配制过程中氢氧化钠的物质的量不变,则需要1.25molL﹣1的NaOH溶液的体积=
=2mol/L,故答案为:2mol/L;(3)1L 0.5molL﹣1NaOH,配制过程中氢氧化钠的物质的量不变,则需要1.25molL﹣1的NaOH溶液的体积= ![]() =0.4L=400mL,故答案为:400;(4)19g MgX2含有Mg2+0.2mol,根据Mg原子守恒得,n(MgX2)=n(Mg )=0.2mol,则MgX2的摩尔质量为:M(MgX2)=
=0.4L=400mL,故答案为:400;(4)19g MgX2含有Mg2+0.2mol,根据Mg原子守恒得,n(MgX2)=n(Mg )=0.2mol,则MgX2的摩尔质量为:M(MgX2)= ![]() =95g/mol,故答案为:95g/mol.
=95g/mol,故答案为:95g/mol.
(1)根据n= ![]() 计算44g干冰的物质的量,根据V=nVm计算标况下占有的体积,所含原子物质的量为干冰的3倍,再根据N=nNA计算含有原子数目,碳原子物质的量等于干冰的物质的量,根据m=nM计算含有碳原子的质量;三氧化硫与二婚头物质的量相等,根据m=nM计算三氧化硫的质量;(2)根据n=
计算44g干冰的物质的量,根据V=nVm计算标况下占有的体积,所含原子物质的量为干冰的3倍,再根据N=nNA计算含有原子数目,碳原子物质的量等于干冰的物质的量,根据m=nM计算含有碳原子的质量;三氧化硫与二婚头物质的量相等,根据m=nM计算三氧化硫的质量;(2)根据n= ![]() 计算HCl的物质的量,再根据c=
计算HCl的物质的量,再根据c= ![]() 计算所得溶液物质的量浓度;(3)根据稀释定律计算需要1.25molL﹣1的NaOH溶液的体积;(4)根据M=
计算所得溶液物质的量浓度;(3)根据稀释定律计算需要1.25molL﹣1的NaOH溶液的体积;(4)根据M= ![]() 计算MgX2的摩尔质量.
计算MgX2的摩尔质量.


科目:高中化学 来源: 题型:
【题目】同温同压下,NH3和H2S气体的密度比是;同质量的NH3和H2S气体的体积比是;同温同密度同体积的NH3和H2S气体中所含H个数比是;若两者所含H个数相等,它们的物质的量之比是;同温同体积下,同质量的NH3和H2S气体的压强之比是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生利用如图所示装置对电解质溶液导电性进行实验探究.下列说法中正确的是( ) 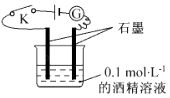
A.闭合开关K后,电流计 ![]() 指针不发生偏转,证明酒精溶液是非电解质
指针不发生偏转,证明酒精溶液是非电解质
B.闭合开关,往溶液中通入氯气,随着气体通入,电流计示数增大,故氯气是电解质
C.取用0.1 molL﹣1的蔗糖溶液替换酒精溶液,电流计的示数相同,说明蔗糖是非电解质
D.闭合开关,往烧杯中加NaCl固体,虽然固体溶解,由于不反应,故电流计指针不发生偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G为原子序数依次增大的短周期主族元素。B、C、D均能与A形成10电子分子,E单质可用于野外焊接钢轨的原料,F与D同主族。
(1)D、E、F的离子半径由大到小的顺序为___________(填离子符号)。
(2)写出能证明G比F非金属性强的一个化学方程式:_____________。
(3)F和G形成的一种化合物甲中所有原子均为8电子稳定结构,该化合物与水反应生成F单质、F的最高价含氧酸和G的氢化物,三种产物的物质的量之比为2:1:6,甲的电子式为_____,该反应的化学方程式为______________。
(4)C能分别与A和D按原子个数比1:2形成化合物乙和丙,乙的结构式为________。常温下,液体乙与气体丙反应生成两种无污染的物质,该反应的氧化产物与还原产物的物质的量之比为________。
(5)现取100 mL1 mol/L的E的氯化物溶液,向其中加入1 mol/L NaOH溶液产生了3.9 g沉淀,则加入的NaOH溶液体积可能为____mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g) ![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
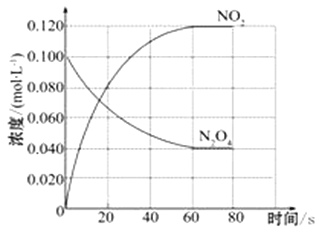
回答下列问题:
(1)反应的△H___________0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60s时段,反应速率v(N2O4)为_____________molL-1s-1,反应的平衡常数K1为______________。
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 molL-1s-1的平均速率降低,经10 s又达到平衡。
① T __________100℃(填“大于”“小于”),判断理由是______________________________________;
② 温度T时反应的平衡常数K2 为 ___________________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向______________(填“正反应”或“逆反应”)方向移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需配制一种仅含五种离子(水电离出的离子可忽略)的混合溶液,且在混合溶液中五种离子的物质的量浓度均为1 mol/L,下面四个选项中能达到此目的的是( )
A. Ca2+、K+、OH、Cl、NO3 B. Fe2+、H+、Br、NO3、Cl
C. Na+、K+、SO42、NO3、Cl D. Al3+、Na+、Cl、SO42、NO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是
A. 将混合气体通过盛有硫酸的洗气瓶
B. 将混合气体通过盛有水的洗气瓶
C. 将混合气体通过盛有足量溴水的洗气瓶
D. 将混合气体通过盛有澄清石灰水的洗气瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.1mol水的质量为18g/mol
B.标准状况下,3.01×1023个CO2分子的质量为22g
C.标准状况下,1mol任何物质体积约为22.4 L
D.二氧化硫的摩尔质量是64 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸的主要反应之一为2SO2(g)+O2(g)![]() 2SO3(g),反应过程中能量变化如图所示,下列说法错误的是
2SO3(g),反应过程中能量变化如图所示,下列说法错误的是
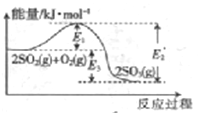
A. 该反应的正反应为放热反应 B. 向反应体系中加入催化剂后,图中E3不变
C. 该反应的焓变△H=(E1-E2)kJ/mol D. 升高温度,E1变大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com