
【题目】实验室需配制一种仅含五种离子(水电离出的离子可忽略)的混合溶液,且在混合溶液中五种离子的物质的量浓度均为1 mol/L,下面四个选项中能达到此目的的是( )
A. Ca2+、K+、OH、Cl、NO3 B. Fe2+、H+、Br、NO3、Cl
C. Na+、K+、SO42、NO3、Cl D. Al3+、Na+、Cl、SO42、NO3
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
【题目】氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:ClO3-+3HSO3-=3SO42-+ Cl-+3H+。己知该反应的速率随c(H+)的增大而加快。右图为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图。下列说法中不正确的是 ( )

A. 反应开始时速率增大可能是c(H+)所致
B. 纵坐标为v(Cl-)的v-t曲线与图中曲线完全重合
C. 图中阴影部分的面积表示t1~t2时间内ClO3-的物质的量的减少量
D. 后期反应速率下降的主要原因是反应物浓度减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废弃的电子产品称为电子垃圾,其中含铅、汞等有害物质、危害严重。下列对电子垃圾处理应予提倡的是①将电子垃圾掩埋地下 ②改进生产工艺,减少有害物质使用 ③依法要求制造商回收废旧电子产品 ④将电子垃圾焚烧处理
A.①③B.②④C.①④D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要的工业原料,下列有关乙烯叙述不正确的是
A. 常温常压下是气体 B. 能使溴的四氯化碳溶液褪色
C. 不能使酸性高锰酸钾溶液褪色 D. 在一定条件下能够聚合生成聚乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)干冰是固态CO2的俗称,常用于人工降雨,44g干冰与A,B,C,D有如图所示的转化关系,请完成如图中的方框. 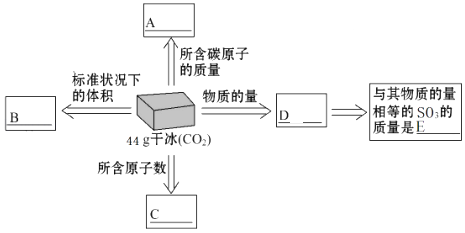
(2)标准状况下22.4L的HCl溶于水配成500mL溶液,所得溶液的物质的量浓度为 .
(3)配制1L 0.5molL﹣1NaOH溶液,需要1.25molL﹣1的NaOH溶液的体积是mL.
(4)19g MgX2含有Mg2+0.2mol,则MgX2的摩尔质量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量):
写出对应的化学方程式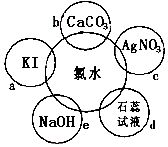
①b;
②c;
③e;
(2)能证明氯水具有漂白性的现象是;
(3)久置的氯水变为(填成份),用化学反应方程式表示为 .
(4)实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
填写字母2KMnO4+16HCl(浓)=5Cl2↑+2MnCl2+2KCl+8H2O
①请用双线桥标出该反应的电子转移方向和数目 .
②该反应中的氧化剂是 , 若消耗0.2mol氧化剂,则被氧化的还原剂的物质的量是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.L电子层不包含d能级
B.s电子绕核旋转,其轨迹为一个圆,而p电子是走“∞”形
C.当n=1时,可能有两个原子轨道
D.当n=3时,有3s、3p、3d、3f四个原子轨道
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材枓的生物相容性方面有很好的应用前景。PPG的一种合成路线如下:

已知:①烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢;
②化合物B为单氯代烃,化合物C的分子式为C5H8;
③E、F为相对分子质量差14的同系物,F是福尔马林的溶质;
④![]()
回答下列问题:
(1)A的结构简式为________________。
(2)由B生成C的化学方程式为_________________________________。
(3)由E和F生成G的反应类型为___________,G的化学名称为_______________。
(4)①由D和H生成PPG的化学方程式为________________________。
②若PPG平均相对分子质量为10000,则其平均聚合度约为__________(填标号)。
a.48 b.58 c.76 d.122
(5)D的同分异构体中能同时满足下列条件的共有________种(不含立体异构):
①能与饱和NaHCO3溶液反应产生气体
②既能发生银镜反应,又能发生皂化反应
其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是_________(写结构简式);D的所有同分异构体在下列—种表征仪器中显示的信号(或数据)完全相同,该仪器是____(填标号)。
a.质谱仪b.红外光谱仪 c.元素分析仪 d.核磁共振仪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:

(1)画出元素⑦的原子结构示意图_______________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_______(填化学式)。
(3)①、④、⑤、⑨中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的化学式:___________
(4)写出元素③的气态氢化物与其最高价含氧酸反应的化学方程式__________________ 写出元素②的单质与元素⑧最高价含氧酸浓溶液反应的化学方程式_______
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
![]()
X溶液与Y溶液反应的离子方程式为_____________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com