
【题目】工业制硫酸的主要反应之一为2SO2(g)+O2(g)![]() 2SO3(g),反应过程中能量变化如图所示,下列说法错误的是
2SO3(g),反应过程中能量变化如图所示,下列说法错误的是
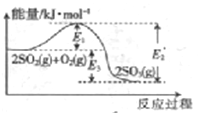
A. 该反应的正反应为放热反应 B. 向反应体系中加入催化剂后,图中E3不变
C. 该反应的焓变△H=(E1-E2)kJ/mol D. 升高温度,E1变大
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】按要求填空
(1)干冰是固态CO2的俗称,常用于人工降雨,44g干冰与A,B,C,D有如图所示的转化关系,请完成如图中的方框. 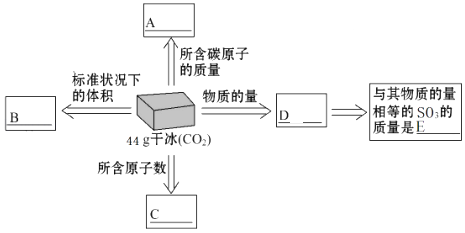
(2)标准状况下22.4L的HCl溶于水配成500mL溶液,所得溶液的物质的量浓度为 .
(3)配制1L 0.5molL﹣1NaOH溶液,需要1.25molL﹣1的NaOH溶液的体积是mL.
(4)19g MgX2含有Mg2+0.2mol,则MgX2的摩尔质量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子,在强碱性溶液中可以大量共存的是
A. K+ 、Fe3+、NO3- 、Cl- B. Ba2+ 、Na+ 、Cl- 、NO3-
C. NH4+、K+、NO3-、Cl- D. Na+ 、Al3+ 、Cl- 、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
A. 核酸中的N存在于碱基中,蛋白质中的N主要存在于肽键中
B. 糖类、脂质的组成元素都是C、H、O
C. 蛋白质中的S元素存在于氨基酸的R基中
D. 同一生物体不同组织细胞内化学元素种类大体相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:

(1)画出元素⑦的原子结构示意图_______________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_______(填化学式)。
(3)①、④、⑤、⑨中的某些元素可形成既含离子键又含共价键的化合物,写出其中一种化合物的化学式:___________
(4)写出元素③的气态氢化物与其最高价含氧酸反应的化学方程式__________________ 写出元素②的单质与元素⑧最高价含氧酸浓溶液反应的化学方程式_______
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
![]()
X溶液与Y溶液反应的离子方程式为_____________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将含49g H2SO4的某浓硫酸加水,配成500ml溶液.
(1)求所得硫酸的物质的量浓度
(2)若将此溶液稀释成1L溶液,取出0.1L再与65g的锌反应,求可以得到标准状况下氢气的体积.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com