
����Ŀ���Ա���Ϊԭ�ϵĺϳ�·��������ʾ,�밴Ҫ������:
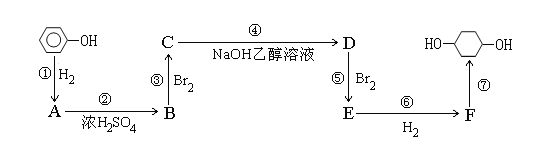
(1)д��A���ʵ�����:__________����������������ڼӳɷ�Ӧ����__________
(2)д����Ӧ�ڢܵĻ�ѧ��Ӧ����ʽ:
��__________________________________________________________________
��__________________________________________________________________
(3)��Ӧ�ݿ����Ƶ�E��ͬʱ�õ����ָ����������һ�ָ�����G�Ľṹ��ֻ��3�ֲ�ͬ����ԭ�ӣ�������G����ͼ�Тߵķ�Ӧ�����л���H��д��H�ṹ��ʽΪ:__________
(4)1,3-����ϩ��Ӧ�ù㷺���л�����ԭ�ϣ��������������ϳ��ȶ������������Ϣд����1,3-����ϩΪԭ���Ʊ��ȶ��ĵ���![]() �ĺϳ�·��(��Ҫ�����Լ�����ѡ)��(ʾ��:CH3CH2OH
�ĺϳ�·��(��Ҫ�����Լ�����ѡ)��(ʾ��:CH3CH2OH ![]() CH2=CH2
CH2=CH2![]() BrCH2CH2Br)___________________________
BrCH2CH2Br)___________________________
���𰸡������� �٢ۢݢ� ![]()
![]()
![]() +H2O
+H2O ![]()
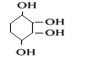
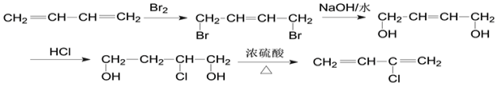
��������
���Ӵ���������ɻ���������������Ũ���ᡢ���������·�����ȥ��Ӧ���ɻ���ϩ������ϩ���嵥�ʷ����ӳɷ�Ӧ����1��2-���廷���飬1��2-���廷������NaOH�Ĵ���Һ�м��ȣ�������ȥ��Ӧ���ɹ����ϩ���������ϩ�����嵥�ʿɷ���1��2�ӳɡ�1��4�ӳɻ�ȫ�ӳɡ�
(1)���Ӵ�����ɵû���������Ϊ�����⣬��ΪŨ������ˮ����Ϊ̼̼˫�����巢���ӳɷ�Ӧ����Ϊ������ȥ����Ϊ̼̼˫�����巢���ӳɷ�Ӧ����Ϊ�����⣬��Ϊ±������ˮ�ⷴӦ�����ϣ����ڼӳɷ�Ӧ���У��٢ۢݢޣ�
(2)�ڻ�������Ũ������ˮ�ķ�Ӧ����ʽΪ��![]()
![]()
![]() +H2O��
+H2O��
���ڶ��廷�������������ƴ���Һ������ȥ��Ӧ����ѧ����ʽΪ��![]() ��
��
��3��DΪ�����ϩ���������巢���ӳɷ�Ӧʱ��������1��2�ӳɲ��� ��1��4�ӳɲ���
��1��4�ӳɲ���![]() ����ȫ�ӳɲ���
����ȫ�ӳɲ���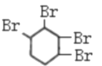 ������1��2�ӳɲ�����6���⣬1��4�ӳɲ�����3���⣬ȫ�ӳɲ�����3���⣬���Ը�����GΪ
������1��2�ӳɲ�����6���⣬1��4�ӳɲ�����3���⣬ȫ�ӳɲ�����3���⣬���Ը�����GΪ ������ȫˮ������ɲ���Ϊ��
������ȫˮ������ɲ���Ϊ��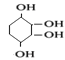 ��
��
��4���Ƚ�1��3-����ϩ��Ŀ�����Ľṹ��𣬾����ڵ�2��̼������һ����ԭ�ӡ�ͨ������ͨ�����Ȼ��ⷢ���ӳɷ�Ӧ���룬���ʽϸߡ�����Ҫ��1��3-����ϩ�м�����̼ת����̼̼˫����ͨ����1��4�ӳɣ�����ȥ���ɣ����Ժϳ�·�����Ϊ��
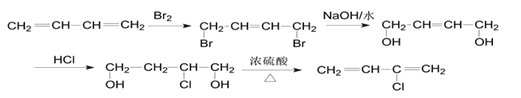 ��ע��Ҫ��ˮ�⣬�ټӳɣ��ٽ��д�����ȥ���Ա����������ԭ�ӡ�
��ע��Ҫ��ˮ�⣬�ټӳɣ��ٽ��д�����ȥ���Ա����������ԭ�ӡ�


 ���źþ���Ԫ����ĩ��ϵ�д�
���źþ���Ԫ����ĩ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ʯ����ֻ�������������SiO2��ȡ36g���ڹ�����ϡ�����У����ˡ�ϴ�ӡ�������5.6g�������õ�����Һ�м���������NaOH��Һ�����ˡ�ϴ�Ӻ������գ���32g����ɫ���壮�����������н��۲���ȷ���ǣ�������
A. ������ʯת��Ϊ����ɫ����Ĺ����з�����������ԭ��Ӧ
B. ���������õ�����Һ��n��Fe2+����n��Fe3+��=1��1
C. ����ʯ�е�����������Ļ�ѧʽһ����Fe3O4
D. ��ϡ����Ϊ3.0molL��1 400mL����Ӧǰ������仯���Բ��ƣ�����Һ��ʣ��H+�����ʵ���Ũ����0.5molL��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ҫ�Ľ������ϣ�������(��Ҫ�ɷ���Al2O3��������SiO2��Fe2O3����)�ǹ�ҵ����ȡ����ԭ�ϡ�ʵ����ģ�ҵ����������Ϊԭ�������������[NH4Al(SO4)2]�Ĺ���������ͼ��ʾ��
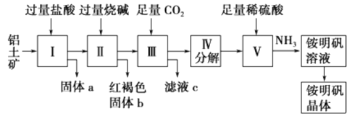
��ش��������⣺
(1)����a�Ļ�ѧʽΪ________������b��ѧʽΪ________������ͨ������CO2���巢����Ӧ�����ӷ���ʽΪ________________��
(2)������ȡ�������Һ�Ļ�ѧ����ʽΪ__________________��
(3)���������������Ҫ�õ��ķ��뷽����__________________�����������Һ�������������IJ�����__________________��
(4)��������������������������ƣ��ټ���������ᣬ��ʱ���ȳ��ֵĹ���a��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������H����Ҫ���л������E��F��һ�������ºϳɣ������ַ�Ӧ������ʡ�ԣ�����ע���ͷ��ָ��
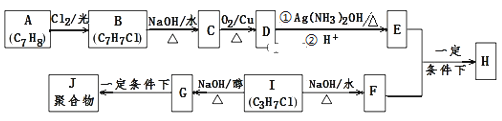
��֪������Ϣ��
i��A���ڷ�������H����������
ii��I�ĺ˴Ź�������Ϊ����壬�ҷ�������Ϊ6��1��
�ش��������⣺
��1��E�ĺ��������������� ______ ��B�Ľṹ��ʽ��___________________��
��2��B��C��G��J�����ķ�Ӧ���ͷֱ�Ϊ ___________��____________��
��3����E+F��H�Ļ�ѧ����ʽ��____________________________________��
��D��������Һ��Ӧ�Ļ�ѧ����ʽ��__________________________________��
��4��E��ͬϵ��K��E��Է���������28����K��ͬ���칹�干 ______ �֣����к˴Ź���������ʾΪ4��壬�ҷ����֮��Ϊ6:2:1:1��д������Ҫ��ĸ�ͬ���칹��Ľṹ��ʽΪ��д��1�ּ��ɣ� ____________________________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪:��һ�������£����Է���R��CH![]() CH2+HX
CH2+HX![]()
A��B��C��D��E������ת����ϵ:
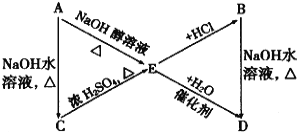
����A��B�ֱ��ǻ�ѧʽΪC3H7Cl������ͬ���칹�塣����ͼ�и����ʵ�ת����ϵ����д���пհ�:
(1) B�Ľṹ��ʽ:_________________________
(2) ������з�Ӧ�Ļ�ѧ����ʽ:
��A��C__________________________________________________________________;
��E��D__________________________________________________________________;
��.������ֲ��֦Ҷ��ȡ�ľ��������к������мס������ֳɷ�:

(1)���к��еĹ����ŵ�����Ϊ______________________(����������)��
(2)�ɼ�ת��Ϊ���辭���й���(����ȥ������Ӧ���ز���,��ͬ):
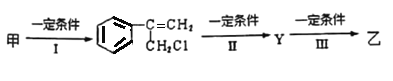
�ٷ�ӦI�ķ�Ӧ������________________________����ӦII��������_________________��
�ڷ�ӦIII�Ļ�ѧ����ʽΪ__________________________________(����ע����Ӧ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����120 ��ʱ����a L��ϩ��b L���顢c L��Ȳ(b>c)��d L����(����)���(a+b+c+d=25)����ȼʹ֮���ȼ�պָ���ԭ�����¶ȣ�������������������
A. 10 L B. 15 L C. 25 L D. 27 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪AgCl��ˮ�е��ܽ������ȹ��̡���ͬ�¶��£�AgCl��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪T1�¶���Ksp(AgCl)=1.6��10-9,����˵����ȷ����
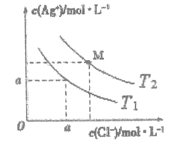
A. T1>T2
B. a =4.0��10-5
C. M����Һ�¶ȱ�ΪT1ʱ����Һ��Cl-��Ũ�Ȳ���
D. T2ʱ����AgCl��Һ�У�c(Ag+)��c(Cl-)���ֱܷ�Ϊ2.0��10-5mol/L��4.0��10-5mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ�Ͻ�㷺���ں��չ�ҵ�����и�����л��������Ʊ�ͭ������Ʒ�Ĺ������£�
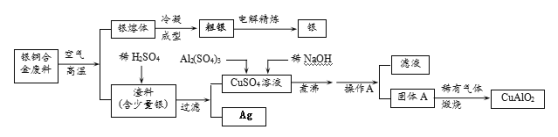
��ע��Al(OH)3��Cu(OH)2�����ֽ�ɶ�Ӧ��������ҿ�ʼ�ֽ���¶ȷֱ�Ϊ450����80����
��1��д��������ϡ���ᷴӦ�Ļ�ѧ����ʽ��________________________��
��2����������A�����Ϊ �� ��
��3������A������Ϊ_______________��
��4������ͭ�Ͻ���ͭ����������Ϊ64%��������5.0 kg�����е�ͭ����ȫת��Ϊ mol CuAlO2��������Ҫ1.0 molL��1��Al2(SO4)3��Һ L��
��5��CuSO4��ҺҲ�������Ʊ��������壬����������� �� �����ˡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������(SiO2)�ֳƹ�ʯ�����Ʊ��輰�仯�������Ҫԭ��(����ת����ͼ)������˵����ȷ����
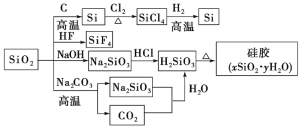
A. SiO2������HF��Ӧ��������NaOH��Ӧ����������������
B. SiO2��Si���ǹ��ά����
C. �轺��ˮ����ظ�����
D. ͼ����ʾת����Ӧ���Ƿ�������ԭ��Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com