
| A�����¶��£�0.31 mol��L-1��HF��Һ��pH=2 |
| B�������¶Ȼ�����Ũ�ȣ�HF�ĵ���ƽ�ⳣ���������� |
| C������Һ��ϲ���������� |
| D���͵�CaF2��Һ�м�ˮ��c(Ca2+)һ���ȼ�ˮǰ��С |
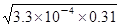 ��1��10��2mol/L��pH��1����A��ȷ��B�����볣��ֻ���¶ȵ�Ӱ�죬����Ũ�ȵı仯���仯����B����C��0.31 mol/L��HF��Һ��c��H+����c��F-����1��10��2mol/L����C�����ڸ��¶���ȡŨ��Ϊ0.31 mol��L-1��HF��Ũ��Ϊ0.002 mol��L-1��CaCl2��Һ�������Ϻ�c��F-����0.5��10��2mol/L��c��Ca2+����0.001mol/L����c2��F-����c��Ca2+������0.5��10��2��2��0.001��2.5��10��8��1.46��10-10����˸���ϵ����CaF2������������C����ȷ��D���͵�CaF2��Һ�м�ˮ����Һ�������DZ��͵ģ�����c(Ca2+)��һ���ȼ�ˮǰ��С��D����ȷ����ѡA��
��1��10��2mol/L��pH��1����A��ȷ��B�����볣��ֻ���¶ȵ�Ӱ�죬����Ũ�ȵı仯���仯����B����C��0.31 mol/L��HF��Һ��c��H+����c��F-����1��10��2mol/L����C�����ڸ��¶���ȡŨ��Ϊ0.31 mol��L-1��HF��Ũ��Ϊ0.002 mol��L-1��CaCl2��Һ�������Ϻ�c��F-����0.5��10��2mol/L��c��Ca2+����0.001mol/L����c2��F-����c��Ca2+������0.5��10��2��2��0.001��2.5��10��8��1.46��10-10����˸���ϵ����CaF2������������C����ȷ��D���͵�CaF2��Һ�м�ˮ����Һ�������DZ��͵ģ�����c(Ca2+)��һ���ȼ�ˮǰ��С��D����ȷ����ѡA��

 �����Ļ���������人������ϵ�д�
�����Ļ���������人������ϵ�д� ���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д�
���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������Һ�У���ˮ�����������������Ũ�Ⱦ�Ϊ1��10��11mol/L |
| B���ֱ��ˮϡ��100����������Һ��pH����Ϊ9 |
| C����ˮ�е�c(NH+)��Ba(OH)2��Һ�е�c(Ba2+)��� |
| D���ֱ���������pHΪ1�����ᣬ���ߵĵ�����������С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��CH3COOH��CH3COO-+H+ |
B��Br-+H2O  HBr+OH- HBr+OH- |
C��CO32-+2H2O  H2CO3+2OH- H2CO3+2OH- |
D��NH4++2H2O  NH3��H2O+H3O+ NH3��H2O+H3O+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ⶨ�䵼��������ͬ |
| B����������п�۷�Ӧ����ʼ������ͬ |
| C����������п�۷�Ӧ���������������Ϊ1��1��100 |
| D����ͬŨ������������Һ��Ӧ����������������Һ�����Ϊ1��2��100 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���Ҵ� | B������ | C������ | D���մ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
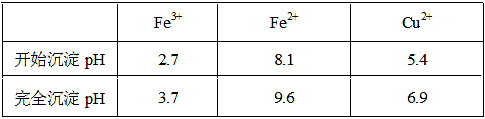
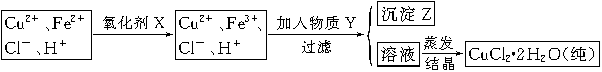
| A��NaClO | B��H2O2 | C��KMnO4 | D��HNO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢ڢ� | B���٢ڢ� | C���٢ڢۢ� | D���٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢ۢݡ��� | B���٢ܢݡ��� |
| C���ڢܡ��� | D���ۢ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com