
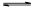 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
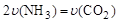 B.密闭容器中总压强不变
B.密闭容器中总压强不变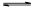 NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。
NH4HCO3+NH3·H2O。该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如图所示。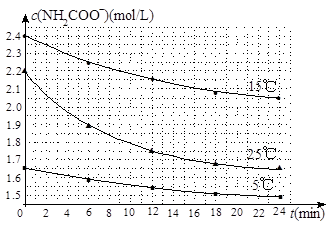
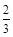
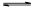 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)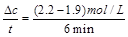 =0.05mol·L-1·min-1;
=0.05mol·L-1·min-1;

科目:高中化学 来源:不详 题型:单选题
 bB(g)达平衡后,保持温度不变,,当达到新的平衡时,B的浓度是原来的60%,则
bB(g)达平衡后,保持温度不变,,当达到新的平衡时,B的浓度是原来的60%,则| A.平衡向正反应方向移动了 | B.物质A的转化率减少了 |
| C.物质B的质量分数增加了 | D.a > b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 C(g)达到平衡时,C的体积分数为40%。试回答有关问题。
C(g)达到平衡时,C的体积分数为40%。试回答有关问题。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 N2(g)+2CO2(g)的反应。关于该反应,下列说法正确的是( )
N2(g)+2CO2(g)的反应。关于该反应,下列说法正确的是( )| A.只要使用合理的催化剂及载体,就可完全清除NO和CO |
| B.该反应达到平衡时v(NO)正=v(CO)逆 |
| C.假设该反应在密闭容器中进行,一段时间后达到平衡时c(NO)=c(CO) |
| D.使用性能好的催化剂可使反应的平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Si(s)+4HCl(g);ΔH=+Q kJ·mol-1(Q>0)
Si(s)+4HCl(g);ΔH=+Q kJ·mol-1(Q>0)| A.反应过程中,若增大压强因为反应速率增大,所以能提高SiCl4的转化率 |
B.已知,一定温度下,反应的平衡常数(k)为定值,若向已经达到平衡状态的容器中再次加入四种物质,若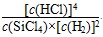 >k,平衡就要向正反应方向移动 >k,平衡就要向正反应方向移动 |
| C.反应至4 min时,若HCl的浓度为0.12 mol·L-1,则H2的反应速率为0.03 mol/(L·min) |
| D.当反应吸收热量为0.025Q kJ时,生成的HCl可被100 mL 1 mol·L-1的NaOH溶液恰好完全吸收 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
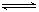 N2O4;△H<O,在密闭容器中达到平衡。平衡时改变外界条件,使反应再次平衡,新平衡时,c(NO2)/c(N2O4)与原平衡相比变大了,则改变条件的可能有
N2O4;△H<O,在密闭容器中达到平衡。平衡时改变外界条件,使反应再次平衡,新平衡时,c(NO2)/c(N2O4)与原平衡相比变大了,则改变条件的可能有| A.保持容器容积和温度不变,向容器内补充了NO2 |
| B.保持容器压强和温度不变,向容器内补充了N2O4 |
| C.保持容器容积和温度不变,向容器内补充了N2 |
| D.保持容器的容积不变,升高了温度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
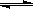 bB(g)达到平衡后,保持温度不变,将容器体积缩小一半,当达到新平衡时,B的浓度是原来的1.6倍,则( )
bB(g)达到平衡后,保持温度不变,将容器体积缩小一半,当达到新平衡时,B的浓度是原来的1.6倍,则( )| A.平衡向正反应方向移动了 | B.物质A的转化率增大了 |
| C.物质B的质量分数减小了 | D.A>b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
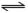 bB(g)+cC(g),在温度不变的条件下,再充入一定量的A,重新达到平衡时,下列判断中正确的是
bB(g)+cC(g),在温度不变的条件下,再充入一定量的A,重新达到平衡时,下列判断中正确的是| A.若a=b+c时,B的物质的量分数变大 | B.若a=b+c时,B的物质的量分数不变 |
| C.若a>b+c时,A的转化率不变 | D.若a<b+c时,A的转化率变大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 5C(g),起始时4个容器所盛A2和B2的量如下表所示:
5C(g),起始时4个容器所盛A2和B2的量如下表所示:| 容量 | 甲 | 乙 | 丙 | 丁 |
| A2(mol) | 2 | 1 | 2 | 1 |
| B2(mol) | 1 | 1 | 2 | 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com