
����Ŀ���������ʵ���ҳ�����ҩƷ�Լ�̽��11�š�17��Ԫ�صĽ������������ǽ���������ǿ����֪ʵ�����������õ���������ҩƷ����ֽ��һ����Ʒ��
��������裺
��1����_________���ֽ����ֱ���ˮ��Ӧ��ͨ���۲��������ݵ����ʱ��ó���________��_________������������
��2����ʵ���Ҳ������й赥�ʣ������Բ�0.1mol/L��_________ ��Һ��_________ ��Һ��Na2SO4��Һ�� pH���ƶ���������Һ��ˮ��������ó�_________��_________ ������������ۺ����������ǿ��˳����__________���Ӷ��ó���__________�ǽ���������ǿ��
��3����ȡ���͵���ˮ�ͱ��͵���������Һ���ý�__________������ͨ��__________�����ֱ�ӵó��ǽ�����S��Cl����
��ƺ�ʵʩ������
��1�����б��ķ�ʽ����ʵ�鷽����ʵ�������йػ�ѧ����ʽ��������ʵ�鱨���е�ʵ�����ݡ�__________________��
��2��ʵ�������___________��
��3�����������ʽṹ����֪ʶ���ͽ���_________��
���𰸡� �ơ�þ���� �� �� Na2SiO3 Na3PO4 H2SiO3 H3PO4 H2SiO3��H3PO4��H2SO4 Si��S ������ˮ�μӵ�������������Һ�е� ��Һ����dz��ɫ��������
ʵ�鷽�� | ʵ������ | �йػ�ѧ����ʽ |
��ɰֽ�����þ���������ֱ�Ͷ�뵽ʢ�з�ˮ��С�ձ��У� �ٷֱ�μӷ�̪ | Ͷ��þ�����Թ��д������ݲ������μӷ�̪����Һ���dz��ɫ��Ͷ���������� �������������� | Mg+2H2O |
��һ�̶�����С����Ͷ�뵽ʢ����ˮ��Ԥ�ȵ��з�̪��С�� ���� | �Ƹ���ˮ���ϣ�Ѹ���۳�����С���Ĵ��ζ�������������֮��ʧ����Һ�ܿ�� ��ɫ | 2Na+2H2O�T2NaOH+H2�� |
�ò������ֱ�պȡ 0.1mol/L ��Na2SiO3(aq)��Na3PO4(aq)��Na2SO4(aq)�� �� pH | Na2SiO3(aq)�� pH��Na3PO4(aq)��pH���Ҷ�����7��Na2SO4(aq)�� pH Ϊ7(����) | SiO32��+2H2O PO43��+H2O |
�õι���ʢ��5mL������������Һ���Թ��еμӱ��͵���ˮ | �Թ����е���ɫ�������� | Cl2+H2S�T2HCl+S�� |
�����ԣ�Na��Mg��Al���ǽ����ԣ�Si��P��S��Cl Na��Mg��Al��Si��S��Clԭ�Ӻ��ⶼ���������Ӳ㣬����������������Ϊ1��2��3��4��6��7��ԭ�Ӱ뾶��������������С������ԭ�Ӻ˶��������ӵ�������������ǿ��ʧ���������������õ���������ǿ
��������
��������裺
(1)���������ڵ��ơ�þ�����ֱ���ˮ��Ӧ���ɹ۲쵽���Ƶ����������ݵ������ڼ�С������Ƶ����Ľ������ڼ������ʴ�Ϊ���ơ�þ��������������
(2)������������ˮ����������ˮ��Ĺ��ɣ����ⶨ��������Һ����������Һ����������Һ��pH��pH�ڼ�С�����������������������������ǿ���Ӷ��ó��ǽ�����Si��P��S���ʴ�Ϊ��Na2SiO3��Na3PO4��H2SiO3��H3PO4��H2SiO3��H3PO4��H2SO4��Si��S��
(3)���������������ԣ�������л�ԭ�ԣ�������ˮ�μӵ�������������Һ�У���۲쵽��Һ����dz��ɫ�������ɣ���˵��Cl�ķǽ����Դ���S���ʴ�Ϊ��������ˮ�μӵ�������������Һ�еģ���Һ����dz��ɫ�������ɣ�
��ƺ�ʵʩ������
(1)����þ����������Ҫ��ɰֽ��ĥ������ˮ��þ��Ӧ��������������������ˮ��Ӧ��Na2SiO3(aq)�� pH��Na3PO4(aq)��pH���Ҷ�����7��Na2SO4(aq)��pHΪ7(����)��������ˮ�μӵ�������������Һ�У���۲쵽��Һ����dz��ɫ�������ɣ��ʴ�Ϊ��
ʵ�鷽�� | ʵ������ | �йػ�ѧ����ʽ |
��ɰֽ��ĥ���þ���������ֱ�Ͷ�뵽ʢ�з�ˮ��С�ձ��У� �ٷֱ�μӷ�̪ | Ͷ��þ�����Թ��д������ݲ������μӷ�̪����Һ���dz��ɫ��Ͷ���������� �������������� | Mg+2H2O |
��һ�̶�����С����Ͷ�뵽ʢ����ˮ��Ԥ�ȵ��з�̪��С�� ���� | �Ƹ���ˮ���ϣ�Ѹ���۳�����С���Ĵ��ζ�������������֮��ʧ����Һ�ܿ�� ��ɫ | 2Na+2H2O�T2NaOH+H2�� |
�ò������ֱ�պȡ 0.1mol/L ��Na2SiO3(aq)��Na3PO4(aq)��Na2SO4(aq)�� �� pH | Na2SiO3(aq)�� pH��Na3PO4(aq)��pH���Ҷ�����7��Na2SO4(aq)�� pH Ϊ7(����) | SiO32��+2H2O PO43��+H2O |
�õι���ʢ��5mL������������Һ���Թ��еμӱ��͵���ˮ | �Թ����е���ɫ�������� | Cl2+H2S�T2HCl+S�� |
��
(2)���ݽ�����ˮ��Ӧ�ľ��ҳ̶ȿ�֪������Na��Mg��Al�����ݷǽ�����ۺ���������Կ�֪�ǽ����� Si��P��S��Cl���ʴ�Ϊ�������ԣ�Na��Mg��Al���ǽ����ԣ�Si��P��S��Cl��
(3)��Na��Mg��Al��Si��S��Clԭ�Ӻ��ⶼ���������Ӳ㣬����������������Ϊ1��2��3��4��6��7��ԭ�Ӱ뾶��������������С������ԭ�Ӻ˶��������ӵ�������������ǿ��ʧ���������������õ���������ǿ����������ڴ��� ��Ԫ�صĽ������ڼ������ǽ���������ǿ���ʴ�Ϊ��Na��Mg��Al��Si��S��Clԭ�Ӻ��ⶼ���������Ӳ㣬����������������Ϊ1��2��3��4��6��7��ԭ�Ӱ뾶��������������С������ԭ�Ӻ˶��������ӵ�������������ǿ��ʧ���������������õ���������ǿ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H��Al��O��N��S��Fe�dz���������Ԫ�ء�
��1��Sλ��Ԫ�����ڱ�______���ڵ�______�壬Fe�Ļ�̬ԭ�Ӻ���۵����Ų�ʽΪ______��O�Ļ�̬ԭ�Ӻ�����______���˶�״̬��ͬ�ĵ��ӡ�
��2���������������=�����
��һ������ | ������ | �е� | �ǽ����� |
N______S | Fe3+______ Al3+ | NH3______H2O | 16O______18O |
��3����֪�����������Ȼ�ѧ����ʽ��
4Fe��s��+302��g��=2Fe2O3��s����H=��a kJ/mol
4Al��s��+3O2��g��=2Al2O3��s����H=��b kJ/mol
��Al��s���ĵ��ʺ�Fe2O3��s����Ӧ���Ȼ�ѧ����ʽ��______��
��4��FeSO4��Һ�������ᷢ����Ӧ��д���˷�Ӧ�����ӷ���ʽ�����������ת�Ƶķ������Ŀ____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ�����Ʒ�к�������������Na2SO4�����������̽��о����������еģ� �����Ǻ��ʵ��Լ����ڣ� ������ʵ��������ơ�д���йط�Ӧ�Ļ�ѧ����ʽ��

��1�������١��ڡ��ۡ�������������Լ��ֱ�Ϊ_______��______��______��_____��
��2�������١��ܡ��IJ������Ʒֱ�Ϊ_________��_______��_______��
��3��д���йص����ӷ�Ӧ����ʽ��
�ڢڲ���_____________________________��
�ڢݲ���_____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж��Ȼ�ѧ����ʽ![]() H2��g��+
H2��g��+![]() I2��g���T�THI��g�� ����=+26 kJ��mol-1�������У���ȷ����
I2��g���T�THI��g�� ����=+26 kJ��mol-1�������У���ȷ����
A��1 mol������1 mol��������ȫ��Ӧ��Ҫ����26 kJ������
B��1������Ӻ�1���������ȫ��Ӧ��Ҫ����52 kJ������
C��1 mol H2��g����1 mol I2��g����ȫ��Ӧ����2 mol��HI����������52 kJ������
D��![]() mol H2��g����
mol H2��g����![]() mol I2��g����ȫ��Ӧ�ų�26 kJ������
mol I2��g����ȫ��Ӧ�ų�26 kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ���Ӧ��������������� ��




A. ͼ�ױ�ʾһ���¶���FeS��CuS�ij����ܽ�ƽ�����ߣ���Ksp(FeS)>Ksp(CuS)
B. ͼ�ұ�ʾpH=2�ļ�����������Һϡ��ʱ��pH�仯������������:����<����
C. 25��ʱ��ͼ����ʾ��0.100mol��L-1��NaOH��Һ�ζ�25.00mL����ĵζ���������c(HCl)=0.080mol��L-1
D. ͼ����ʾ��ӦN2(g)+3H2(g)![]() 2NH3(g)ƽ��ʱNH3�����������ʼ
2NH3(g)ƽ��ʱNH3�����������ʼ![]() �仯����������ת���ʣ�aA(H2)<aB(H2)
�仯����������ת���ʣ�aA(H2)<aB(H2)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��F���ֶ���������Ԫ�أ�ԭ������������������B�ĵ����ڳ�����Ϊ˫ԭ�ӷ��ӣ�����A�ĵ��ʿ��γ���̬����X��X��ˮ��Һ�ʼ��ԣ�D�ļ���������X������ͬ����������D��ͬ����Ԫ����ԭ�Ӱ뾶����Ԫ�أ�EԪ�ص�ԭ�������ȴ�������������ӣ�C��F����Ԫ�ص�ԭ������㹲��13 �����ӡ���
��1��B��ԭ�ӽṹʾ��ͼΪ ��X�Ļ�ѧ����Ϊ ��
��2��B���ʵĵ���ʽΪ ��E����̬�⻯��ĽṹʽΪ ��C��D�γɵ����ֻ������У�ԭ�Ӹ�����Ϊ1:1���������������еĻ�ѧ��Ϊ ������������ ���������ӻ��������������ۻ�����������
��3��B��C��E�ֱ���A�γɵĻ����������ȶ����� ��д��ѧʽ����
��4��D��ͬ���ڼ������������Ӱ뾶�� ��Ԫ�ء�
��5��F�ĵ����ڷ�Ӧ�г��� ��������������������ԭ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԭ���װ������ͼ��ʾ������ܷ�ӦΪ2Ag��Cl2===2AgCl������˵����ȷ����(����)

A. ������ӦΪAgCl��e��===Ag��Cl��
B. �ŵ�ʱ������Ĥ�Ҳ���Һ���д�����ɫ��������
C. ����NaCl��Һ�������ᣬ�����ܷ�Ӧ��֮�ı�
D. ����·��ת��0.01 mol e��ʱ������Ĥ�����Һ��Լ����0.02 mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ������������ԭ��Ӧ����
A. CaO + H2O = Ca(OH)2 B. CaCO3 + 2HCl= CaCl2 + CO2��+H2O
C. 2H2O2 ![]() 2H2O + O2�� D. CaCO3
2H2O + O2�� D. CaCO3![]() CaCO3 + CO3��
CaCO3 + CO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E�������ʻ������֮����ת����ϵ��ͼ��ʾ��AΪ�ؿ��к������������ķǽ���Ԫ�صĵ��ʣ��侧��ṹ����ʯ���ơ�
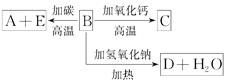
����գ�
(1)�γɵ���A��ԭ�ӵĽṹʾ��ͼΪ________����������ϼ�Ϊ________��
(2)B�Ļ�ѧʽΪ_______________��B��̼��Ӧ����A��E�Ļ�ѧ����ʽΪ_________________________��
(3)C�Ļ�ѧʽΪ________��D�Ļ�ѧʽΪ____________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com