
【题目】下列反应中属于氧化还原反应的是
A. CaO + H2O = Ca(OH)2 B. CaCO3 + 2HCl= CaCl2 + CO2↑+H2O
C. 2H2O2 ![]() 2H2O + O2↑ D. CaCO3
2H2O + O2↑ D. CaCO3![]() CaCO3 + CO3↑
CaCO3 + CO3↑
科目:高中化学 来源: 题型:
【题目】如何利用实验室常见的药品试剂探究11号~17号元素的金属性逐渐减弱,非金属性逐渐增强?已知实验室有你想用到的仪器和药品、试纸等一切用品。
猜想与假设:
(1)用_________三种金属分别与水反应,通过观察生成气泡的速率便会得出从________到_________金属性逐渐减弱。
(2)因实验室不可能有硅单质,但可以测0.1mol/L的_________ 溶液和_________ 溶液及Na2SO4溶液的 pH,推断三种盐溶液的水解情况,得出_________、_________ 、硫酸三种最高价含氧酸的酸性强弱顺序是__________,从而得出从__________非金属性逐渐增强。
(3)制取饱和的氯水和饱和的氢硫酸溶液,用将__________方法,通过__________现象便直接得出非金属性S比Cl弱。
设计和实施方案:
(1)用列表的方式(从实验方案、实验现象、有关化学方程式)完成你的实验报告中的实验内容。__________________。
(2)实验结论是___________。
(3)请你用物质结构理论知识解释结论_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s) = Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
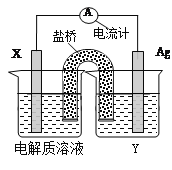
(1)电极X的材料是________;电解质溶液Y是_________;
(2)银电极为电池的________极,发生的电极反应为__________________;X电极上发生的电极反应为________________________;
(3)外电路中的电子是从_______电极流向________电极。
(4)若电极X质量减少6.4g,则Ag极质量增加______ g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示3套实验装置,分别回答下列问题:


(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入KSCN溶液呈无色,再滴入氯水即可观察到铁钉附近的溶液变红色,表明铁被_______(填氧化、还原);向插入碳棒的玻璃筒内滴入酚酞试液,可观察到碳棒附近的溶液变红,该电极反应为_______________。
(2)装置2中的石墨是_________极(填“正”或“负”),该装置发生的总反应的离子方程式为___________________________________。
(3)装置3中甲烧杯盛放100 mL 0.2 mol·L-1的NaCl溶液,乙烧杯盛放100 mL 0.5 mol·L-1的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞试液,观察到石墨电极附近首先变红。
①电源的M端为_________极,甲烧杯中铁电极的电极反应为________________;
②乙烧杯中电解反应的离子方程式为___________________________________;
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,则甲烧杯中产生的气体在标准状况下为____________ mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表物质按碱、酸、盐、碱性氧化物、酸性氧化物的顺序分类正确的是( )
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
B | KOH | HCl | NaCl | CaO | CO |
C | NaOH | H2CO3 | CaCl2 | CuO | SO2 |
D | NaOH | HNO3 | BaCO3 | NO | SO3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,将一定量A、B气体混合后发生反应:xA(g)+yB(g)![]() zC(g)+mD(s)。平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.3mol/L。则下列有关判断正确的是 ( )
zC(g)+mD(s)。平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.3mol/L。则下列有关判断正确的是 ( )
A. x+y>z+m B. 混合气体的密度一定减小
C. 平衡向正反应方向移动 D. B的转化率一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用石油产品A(C4H8),可以合成材料化学重要的物质G和H。己知:
①A和C的核磁共振氢谱都有2组峰,且峰面积之比分别为1∶3和1∶2
②E和F都可发生银镜反应;E的分子式为:C4H4O2
③H2C=CH2+H2O2![]()
![]()
④R-CH2-CHO+HCHO![]()
![]()
G和H的合成路线如下图所示:
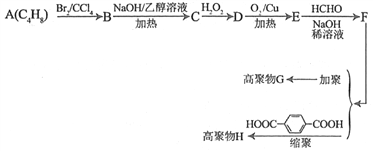
请回答下列问题:
(1)C的名称________________;F中官能团名称为____________________。
(2)A的同分异构体共有___________种(不包括A本身,不含立体异构)
(3)写出B到C的化学方程式和反应类型:
化学方程式为______________________________________________,反应类型是___________。
(4)D→E的化学方程式为___________________________________________。
(5)H的结构简式为_______________________________________________,G的结构简式为____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.反应条件是加热的反应都是吸热反应
B.化学反应除了生成新的物质外,还伴随着能量的变化
C.物质燃烧不一定是放热反应
D.放热的化学反应不需要加热就能发生
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com