
【题目】(1)已知NO2和N2O4可以相互转化N2O4 (g)![]() 2NO2 (g)△H=+57.2kJ/mol。t℃时,现将一定量NO2和N2O4的混合气体通入体积为2 L的恒温密闭容器中,反应物浓度随时间变化关系如下表所示,据此回答相关问题:
2NO2 (g)△H=+57.2kJ/mol。t℃时,现将一定量NO2和N2O4的混合气体通入体积为2 L的恒温密闭容器中,反应物浓度随时间变化关系如下表所示,据此回答相关问题:
时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
c(x)/mol·L-1 | 0.2 | C | 0.6 | 0.6 | 1.2 | C1 | C1 |
c(Y)/mol·L-1 | 0.6 | c | 0.4 | 0.4 | 0.4 | C2 | C2 |
①前10 min内用N2O4表示的化学反应速率v(N2O4)=__________,t℃时,该反应的化学平衡常数K=__________。
②20min时,若只改变了某一个条件,该条件可能是__________。
③t℃时,若开始时向容器中充入1mol的NO2、0.2mol N2O4,则v(正)________v(逆)(填“>”“<”或“=”)
(2)一定压强下,向10L密闭容器中充入1molS2Cl2和1molCl2,发生反应S2Cl2(g) + Cl2(g)![]() 2SCl2(g)。Cl2和SCl2的消耗速率(v)与温度(T)的关系如图所示:
2SCl2(g)。Cl2和SCl2的消耗速率(v)与温度(T)的关系如图所示:
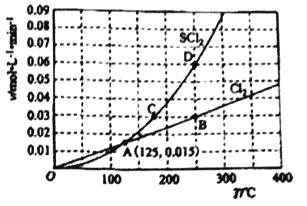
①ABCD四点对应状态下,达到平衡状态的有__________。
②△H2_______0(填“>”“<”或“=”)
【答案】 0.02 mol·L-1 ·min-1 0.9mol·L-1 充入1.2molNO2(增大NO2浓度也可) < BD <
【解析】
(1)①X、Y的起始浓度分别为0.2mol/L、0.6mol/L,10min时到达平衡,X浓度增大了0.4mol/L、Y的浓度减小0.2mol/L,因为NO2、N2O4与按物质的量2:1反应,则X为NO2、Y为N2O4;v(N2O4)=![]() =0.02mol.L-.min
=0.02mol.L-.min
平衡常数K=
c2(NO2) |
c(N2O4) |
=
0.62 |
0.4 |
=2.25,
因此,本题正确答案是:0,02 mol.L-.min;2.25;
②20min时,Y(N2O4)的浓度不变,X(NO2)的浓度增大,改变的条件应是增大NO2的浓度,等效为增大压强,平衡向生成N2O4的向逆反应进行,减少2molNO2的同时混合气体总物质的量减小1mol,则混合气体中NO2的百分含量减小,因此,本题正确答案是:增大NO2的浓度。
t℃时,若开始时向容器中充入1mol的NO2、0.2mol N2O4,则v(正)________v(逆)(填“>”“<”或“=”)
③ C(NO2)=![]() =0.5mol/L C(N2O4)=
=0.5mol/L C(N2O4)=![]() =0.1mol/L Q=
=0.1mol/L Q=![]() =0.4<2,25,所以平衡向逆反应方向移动。所以v(正) <v(逆),故答案:<。
=0.4<2,25,所以平衡向逆反应方向移动。所以v(正) <v(逆),故答案:<。
(2)①根据反应II:S2Cl2 (g) +Cl2 (g)![]() 2SCl2 (g)可知,用氯气的消耗速率表示正反应速率和用SCl2的消耗速率表示逆反应速率,二者之比为1:2时转化为用同一种物质表示的正逆反应速率相等,达到平衡状态,由图像可知B、D点时的正逆反应速率之比为1:2,达到平衡状态;故达到平衡状态的有:B D。
2SCl2 (g)可知,用氯气的消耗速率表示正反应速率和用SCl2的消耗速率表示逆反应速率,二者之比为1:2时转化为用同一种物质表示的正逆反应速率相等,达到平衡状态,由图像可知B、D点时的正逆反应速率之比为1:2,达到平衡状态;故达到平衡状态的有:B D。
② B、D点为平衡点,由图中数据可知,B、D点的状态对应的温度为250℃,300℃时,SCl2的消耗速率大于氯气的消耗速率的2倍,说明平衡逆向移动,则正反应为放热反应,ΔH2<0。正确答案:<。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.加热杀死流感H7N9病毒是因为蛋白质受热发生盐析
B.医用酒精灭活新冠肺炎病毒是利用其氧化性
C.我国研制的重组新冠疫苗无需冷藏保存
D.乙烯的产量通常用来衡量一个国家石油化工的水平
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解硫酸钠溶液生产硫酸和烧碱的装置如图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1:2,下列有关说法正确的是(说明:阳离子交换膜只允许阳离子通过,阴离子交换膜只允许阴离子通过)
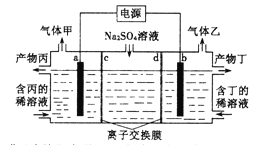
A. a电极反应式为:2H++2e—=H2↑ B. 产物丙为硫酸
C. d为阴离子交换膜 D. Na2SO4溶液浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】市场销售的某种精制食用盐包装袋上有如下说明:
产品标准 | GB5461 |
产品等级 | 一级 |
配料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50mg/kg |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
KIO3+KI+H2SO4=K2SO4+I2+H2O,______________
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应后溶液显酸性,写出该反应的离子方程式:_____________________________。
②某同学设计回收四氯化碳的操作步骤如下,请将缺少的操作步骤补充完整。
a.将碘的四氯化碳溶液置于分液漏斗中; b.加入适量Na2SO3溶液
c.____________________ d.分离出下层液体。
(3)已知:I2+2S2O32=2I-+S4O62-。某质量检验监督局测定食用精制盐的碘含量,其步骤为:
a.准确称取12.7g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,以6.0×10-4mol·L-1的Na2S2O3标准溶液滴定,消耗20.00mL标准液。
①判断c中滴定反应恰好完全的现象是_____________________。
②根据以上实验和包装袋说明,所测精制盐的碘含量是____mg/kg。
(4)用惰性电极电解KI溶液可制备碘酸钾,则阳极反应式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在T ℃时,难溶物Ag2CrO4在水溶液中的溶解平衡曲线如下图所示,又知T ℃时AgCl的Ksp=1.8×10-10。下列说法错误的是

A. T ℃时,Ag2CrO4的Ksp为1×10-11
B. T ℃时,Y点和Z点的Ag2CrO4的Ksp相等
C. T ℃时 , X点的溶液不稳定,会自发转变到Z点
D. T ℃时,将0.01 mol·L-1的AgNO3溶液逐渐滴入20 mL 0.01 mol·L-1的KCl和0.01 mol·L-1的K2CrO4混合溶液中,Cl-先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程(如图),乙醛在两电极分别转化为乙醇和乙酸。下列对电解过程的分析正确的是

A. 以铅蓄电池为电源,则a极为Pb电极
B. 石墨Ⅱ电极附近的pH逐渐减小
C. 阳极反应为CH3CHO+H2O-2e-=CH3COOH+2H+
D. 每处理含8.8g乙醛的废水,转移电子的数目为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下图装置电解硫酸钾溶液来获得氧气、氢气、硫酸和氢氧化钾。
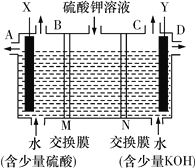
(1)X极与电源的________(填“正”或“负”)极相连,氢气从________(填“A”“B”“C”或“D”)口导出。
(2)离子交换膜只允许一类离子通过,则M为________(填“阴离子”或“阳离子”,下同)交换膜,N为________交换膜,图中少量硫酸和少量氢氧化钾的作用是________________________________________。
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的电极反应式为______________________________________________。
(4)若使用铅蓄电池作电源完成上述电解,当制得11.2 L标准状况下的氢气时,理论上铅蓄电池消耗硫酸________ mol,正极板质量增加______g,负极板质量增加________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2O2是呼吸面具中常用的供氧剂,下列关于Na2O2的叙述正确的是( )
A. Na2O2中阴、阳离子的个数比为1:1
B. Na2O2分别与水、CO2反应,产生相同量的O2时,需要水和CO2的物质的量相等
C. Na2O2与CO2反应过程中,只做氧化剂
D. Na2O2与SO2的漂白原理相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com