
【题目】下列离子方程式或化学方程式正确的是( )
A.铁与水蒸气在高温下反应:2Fe+3H2O![]() Fe2O3+3H2
Fe2O3+3H2
B.Na投入水中:Na+H2O=Na++OH-+H2↑
C.氢氧化铁胶体的制备Fe3++3H2O=Fe(OH)3↓+3H+
D.大理石溶于醋酸的反应:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑
 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:
【题目】现有某有机物A,欲推断其结构,进行如下实验:
(1)取15gA 完全燃烧生成22gCO2和9gH2O,该有机物的实验式为_________________。
(2)质谱仪检测得该有机物的相对分子质量为90,则该物质的分子式为__________。
(3)若该有机物在浓硫酸共热的条件下,既能与乙酸反应,又能与乙醇反应,还能2分子A 反应生成含六元环的物质,则A 的结构简式为__________________。
(4)写出A发生缩聚反应生成高分子化合物的方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)物质的分离与提纯是化学的重点,请根据下列实验目的,分别选择相应的操作和实验装置。下列为操作:
a.蒸馏 b.结晶法 c.加适量水,过滤 d.加热(或灼烧) e.加适量盐酸,蒸发 f.萃取分液 g.分液 h.升华
下列为实验装置:
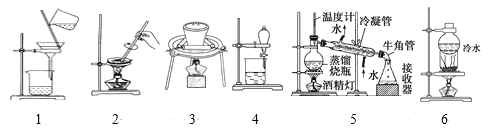
(1)从碘水中提取碘:___、__。(分别填操作序号及实验装置图编号,下同)。
(2)除去氧化钙中的碳酸钙:___、___。
(3)除去硫酸钡中的硝酸钾:___、___。
(4)分离固体细沙和碘的方法:___、___。
(5)除去氯化钠晶体中的碳酸钠:___、__。
(6)分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合液(两者互溶):__、_。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]()
![]()
![]() (R、R'可表示烃基或官能团)。A可发生如图转化(方框内物质均为有机物,部分无机产物已略去):
(R、R'可表示烃基或官能团)。A可发生如图转化(方框内物质均为有机物,部分无机产物已略去):
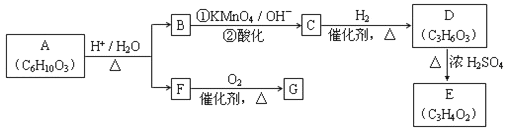
请回答:
(1)F的蒸气密度是相同条件下H2密度的31倍,且分子中无甲基。已知1mol F与足量金属钠作用产生H2 22.4L(标准状况),则F的分子式是_____,名称是__________.
(2)G与F的相对分子质量之差为4,则G具有的性质是______(填字母)
a.可与银氨溶液反应 b.可与乙酸发生酯化反应
c.可与氢气发生加成反应 d.1mol G最多可与2mol新制Cu(OH)2发生反应
(3)D能与NaHCO3溶液发生反应,且两分子D可以反应得到含有六元环的酯类化合物,E可使溴的四氯化碳溶液褪色,则D→E的化学方程式是______________,该反应类型是_____反应
(4)H与B互为同分异构体,且所含官能团与B相同,则H的结构简式可能是:_________.
(5)A转化为B和F的化学方程式是__________.
(6)A的同分异构体含有两种官能团,该化合物能发生水解,且1mol该化合物能与4mol银氨溶液反应,符合该条件的同分异构体一共有__________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Na、Na2O、Na2O2的混合物与足量的水反应,在标准状况下得到a L混合气体。将该混合气体通过电火花引燃,恰好完全反应,则原混合物中Na、Na2O、Na2O2的物质的量之比可能为
A. 2:1:1
B. 1:1:2
C. 1:2:1
D. 4:3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,正确的是( )

A.用如图装置进行实验,将装置①中的AlCl3滴入装置②浓氢氧化钠溶液中可观察到有大量白色沉淀产生
B.利用装置③可制备氢氧化亚铁并长时间观察其颜色
C.装置④不能验证Na2CO3和NaHCO3两种固体的热稳定性
D.用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来说明金属铝的熔点较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫直接排放会危害环境。利用工业废碱渣(主要成分Na2CO3)可吸收烟气中的SO2并制备无水Na2SO3,其流程如图1。
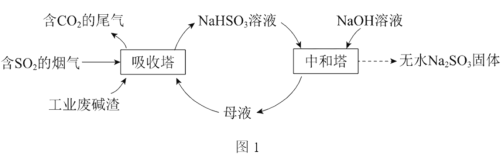
已知:H2SO3、HSO3、SO32在水溶液中的物质的量分数随pH的分布如图2,Na2SO3·7H2O和Na2SO3的溶解度曲线如图3。
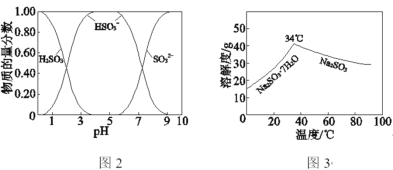
(1)Na2CO3溶液显碱性,用离子方程式解释其原因:_____________________。
(2)吸收烟气
①为提高NaHSO3的产率,应控制吸收塔中的pH为________。
②已知下列反应:
SO2(g)+2OH(aq)==SO32(aq)+H2O(l)ΔH1=164.3kJ·mol1
CO2(g)+2OH(aq)==CO32(aq)+H2O(l)ΔH2=109.4kJ·mol1
2HSO3(aq)==SO32(aq)+SO2(g)+H2O(l)ΔH3=+34.0kJ·mol1
吸收塔中Na2CO3溶液吸收SO2生成HSO3的热化学方程式是________。
③吸收塔中的温度不宜过高,可能的原因是________(写出1种即可)。
(3)制备无水Na2SO3
①中和塔中反应的离子方程式为_________________________________。
②从中和塔得到的Na2SO3溶液中要获得无水Na2SO3固体,需控制温度____________,同时还要_______________,以防止Na2SO3氧化。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反-2-己烯醛(D)是一种重要的合成香料,下列合成路线是制备D的方法之一。根据该合成路线回答下列问题:
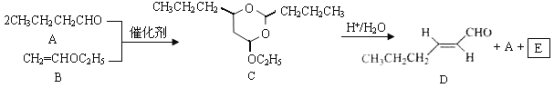
已知: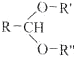
![]() RCHO+R'OH+R"OH
RCHO+R'OH+R"OH
(1)A的名称是__________;B分子中共面原子数目最多为__________;C分子中与环相连的三个基团中,不同化学环境的氢原子共有__________种。
(2)D中含氧官能团的名称是__________,写出检验该官能团的化学反应方程式:__________。
(3)E为有机物,能发生的反应有__________。
a.聚合反应b.加成反应c.消去反应d.取代反应
(4)B的同分异构体F与B有完全相同的官能团,写出F所有可能的结构:________。
(5)以D为主要原料制备己醛(目标化合物),在方框中将合成路线的后半部分补充完整。
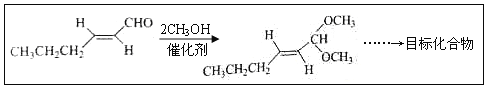
(6)问题(5)的合成路线中第一步反应的目的是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香烃在工业生产中有着重要的用途。下列有关苯乙烯和2-苯基丙烯(![]() )的说法错误的是( )
)的说法错误的是( )
A.二者互为同系物
B.均能使澳水溶液褪色
C.分子中的所有原子均可能在同平面上
D.均能发生取代反应和加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com