
【题目】超临界状态下的CO2流体溶解性与有机溶剂相似,可提取中药材的有效成分,工艺流程如下。

下列说法中错误的是( )
A.浸泡时加入乙醇有利于中草药有效成分的浸出
B.高温条件下更有利于超临界CO2流体萃取
C.升温、减压的目的是实现CO2与产品分离
D.超临界CO2流体萃取中药材具有无溶剂残留、绿色环保等优点
科目:高中化学 来源: 题型:
【题目】对于可逆反应N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0,下列各项对示意图的解释与图像相符的是
2NH3(g) ΔH<0,下列各项对示意图的解释与图像相符的是

A. ①压强对反应的影响(p2>p1) B. ②温度对反应的影响
C. ③平衡体系增加N2对反应的影响 D. ④催化剂对反应的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,容积相同的甲、乙、丙3个恒容密闭容器中发生可逆反应:2SO2(g)+O2(g)![]() 2SO3(g);
2SO3(g); ![]() 。实验测得起始、平衡时的有关数据如下表:
。实验测得起始、平衡时的有关数据如下表:
容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | |||
SO2 | O2 | SO3 | Ar | ||
甲 | 2 | 1 | 0 | 0 | 放出热量:Q1 |
乙 | 1.8 | 0.9 | 0.2 | 0 | 放出热量:Q2 |
丙 | 1.8 | 0.9 | 0.2 | 0.1 | 放出热量:Q3 |
下列叙述正确的是 ( )
A.Q1=Q2=Q3="197" kJ
B.若在上述条件下反应生成2molSO3(s)的反应热为△H1,则△H1<-197 kJ·mol-1
C.甲、乙、丙3个容器中反应的平衡常数不相等
D.达到平衡时,丙容器中SO2的体积分数最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水![]() 的制备流程如下:
的制备流程如下:
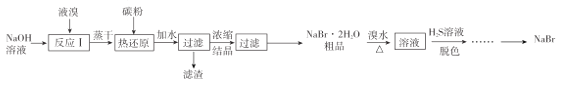
已知:①![]() ;
;
②![]() 溶于
溶于![]() 溶液生成
溶液生成![]() ,离子方程式可表示为
,离子方程式可表示为![]() 。
。
请回答:
(1) “反应I”所用![]() 溶液最好是饱和溶液,理由是____________
溶液最好是饱和溶液,理由是____________
(2)已知“热还原”反应中,氧化剂和还原剂物质的量之比为![]() ,若该反应中消耗了
,若该反应中消耗了![]() 碳粉,则理论上最终可制得
碳粉,则理论上最终可制得![]() 的质量为_____________(不考虑制备过程中的损失)。
的质量为_____________(不考虑制备过程中的损失)。
(3)“脱色”过程中生成了两种强酸,写出该过程的离子方程式:______________________
(4)用![]() 与
与![]() 溶液反应是制备
溶液反应是制备![]() 的另一种方法,反应过程中有气体和沉淀生成,写出此方法的化学方程式:___________________
的另一种方法,反应过程中有气体和沉淀生成,写出此方法的化学方程式:___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】托特罗定M合成路径如下(反应条件已略去):

已知信息:① (不稳定)
(不稳定)
②
③G遇![]() 溶液显紫色,H中含有3个六元环
溶液显紫色,H中含有3个六元环
请回答:
(1)M的分子式是__________,化合物K的结构简式是______________。
(2)下列说法正确的是__________
A.化合物B转化为C是消去反应,F转化为G是取代反应
B.化合物C转化为D的反应及F转化为G的反应都只需加入强碱后水解即可
C.![]() 化合物I与
化合物I与![]() 反应,最多消耗
反应,最多消耗![]()
D.等物质的量的A和D完全燃烧消耗的氧气量相等
(3)写出![]() 的化学方程式:__________________.
的化学方程式:__________________.
(4)M的同系物![]() 有多种同分异构体,同时符合下列条件的同分异构体的结构简式如
有多种同分异构体,同时符合下列条件的同分异构体的结构简式如 ,请再写出3种:____________________。
,请再写出3种:____________________。
①分子中含有2个独立的苯环;
②![]() 谱和
谱和![]() 谱检测显示分子中有5种化学环境不同的氢原子,有
谱检测显示分子中有5种化学环境不同的氢原子,有![]() 键,无
键,无![]() 键和
键和![]() 键。
键。
(5)设计以甲苯和乙酸酐( )为原料制备D肉桂酸(
)为原料制备D肉桂酸( )的合成路线(无机试剂任选,合成中须用到上述已知信息①②.用流程图表示):__________________________________________________________
)的合成路线(无机试剂任选,合成中须用到上述已知信息①②.用流程图表示):__________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
盐酸
分子式:HCl
相对分子质量:36.5
密度:1.19gcm-3HCl的质量分数:36.5%
(1)该浓盐酸中HCl的物质的量浓度为__________mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是______。
a.溶液的浓度
b.溶液中HCl的质量
c.溶液中Cl-的数目
d.溶质的质量分数
(3)某学生欲用上述浓盐酸和蒸馏水配制40mL物质的量浓度为0.400mol/L的稀盐酸。
①该学生需要量取_______ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?______(填“偏大”、“偏小”、“无影响”)
a.用量筒量取浓盐酸时仰视观察凹液面
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
(4)①假设该同学成功配制了0.400mol/L的盐酸,他又用该盐酸中和含0.8gNaOH的溶液,则该同学需取_______ mL盐酸。
②假设该同学用新配制的盐酸中和含0.8g NaOH的溶液,发现比①中所求体积偏小则可能的原因是_______。
a.加水时超过刻度线,用胶头滴管吸出
b.配制溶液时,未洗涤烧杯
c.配制溶液时,俯视容量瓶刻度线
d.配置溶液时,量取浓盐酸后用蒸馏水洗涤量筒并转移至烧杯中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把500mL含有BaCl2和KCl的混合溶液分成5等份,取一份加入含a mol 硫酸钠的溶液恰好使钡离子完全沉淀;另取一份加入含b mol 硝酸银的溶液恰好使氯离子完全沉淀.则该混合溶液中钾离子浓度为( )
A. 0.1(b-2a)mol/LB. 10(2a-b)mol/LC. 10(b-a)mol/LD. 10(b-2a)mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、铝、铜等金属及其化合物在日常生活中应用广泛,请回答下列问题。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸,离子方程式为_______________________________________________________;Y与过量浓硝酸反应后溶液中含有的盐的化学式为____________;
(2)某溶液中含有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___________(填编号)。
A.Mg2+ B.Fe2+ C.Al3+ D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:

①Na2CO3溶液可以除油污,原因是(用离子方程式表示)________________________________;
②操作Ⅱ中沉淀的洗涤方法是___________________________________________________________
③请写出生成FeCO3沉淀的离子方程式_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度和体积固定的密闭容器中,可逆反应H2(g)+I2(g) ![]() 2HI(g) (无色)达平衡状态,该状态下,说法不正确的是( )
2HI(g) (无色)达平衡状态,该状态下,说法不正确的是( )
A. 可逆反应停止 B. I2浓度不再变化
C. HI浓度不再变化 D. 混合气体颜色不再变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com