
【题目】用如图所示装置分别进行下列各组物质的导电性实验,小灯泡的亮度比反应前明显减弱的是

A. 向亚硫酸钠溶液中通入氯气
B. 向硝酸银溶液中通入少量氯化氢
C. 向氢碘酸饱和溶液中通入少量氧气
D. 向氢氧化钠溶液中通入少量氯气
【答案】C
【解析】
电解质溶液的导电性与离子浓度及离子所带的电荷有关,离子浓度越大,溶液导电性越强,溶液导电能力明显减弱说明溶液中离子浓度明显减小,据此分析解答。
A. 向亚硫酸钠溶液中通入氯气,发生反应:Na2SO3+Cl2+H2O=Na2SO4+2HCl,反应后的溶液中离子浓度增大,溶液导电能力明显增强,故A不选;
B. 向硝酸银溶液中通入少量氯化氢,发生反应:AgNO3+HCl=AgCl↓+HNO3,反应后的溶液中离子浓度变化不明显,溶液导电能力变化不明显,故B不选;
C. 向氢碘酸饱和溶液中通入少量氧气,发生反应:4HI+O2=2I2+2H2O,反应后的溶液中离子浓度减小,溶液导电能力明显减弱,故C选;
D. 向NaOH溶液中通入少量Cl2,发生反应:Cl2+2NaOH=NaCl+NaClO+H2O,反应后的溶液中离子浓度变化不明显,溶液导电能力变化不明显,故D不选,答案选C。


科目:高中化学 来源: 题型:
【题目】[化学—选修5:有机化学基础]A(C2H4)是基本的有机化工原料。用A和常见的有机物可合成一种缩醛类香料。具体合成路线如图(部分反应条件略去):

已知以下信息:
①![]()
②D为能与金属钠反应的芳香族化合物
回答下列问题:
⑴A的名称是_________,图中缩醛的分子式是_________。
⑵B的结构简式为_______。
⑶以下有关C的说法正确的是_________。
a.易溶于水 b.分子中所有原子可能在同一平面
c.与乙醇互为同系物 d.在一定条件下能发生消去反应生成乙炔
⑷③、⑤的有机反应类型依次为为______、______,④的化学方程式为_____________。
⑸写出满足下列条件的苯乙醛的所有同分异构体的结构简式:含有苯环,加入FeCl3溶液显紫色,核磁共振氢谱有5组峰,峰面积之比为2∶2∶2∶1∶1。 ________________
⑹参照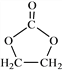 的合成路线,设计一条由2-氯丙烷和必要的无机试剂制备
的合成路线,设计一条由2-氯丙烷和必要的无机试剂制备 的合成路线(注明必要的反应条件)。_________________________________
的合成路线(注明必要的反应条件)。_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学实验”进课堂,某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验。先给钠预热,当钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。

以下叙述错误的是
A. 反应生成的大量白烟是氯化钠晶体
B. 玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免污染空气
C. 钠着火燃烧产生苍白色火焰
D. 棉球外沿滴一滴淀粉碘化钾溶液,可据其颜色变化判断氯气是否被碱液完全吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法中,不正确的是
A.75%的乙醇溶液作医用消毒剂B.Fe3O4用作红色油漆和涂料
C.ClO2可用作自来水消毒剂D.Na2O2用作呼吸面具等的供氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示:

(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):
A________、 B________、 D________、E________。
(2)写出下列反应的化学方程式(请注明反应条件):
A+H2O: ____________________;
A → D: ____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHSO4在水中的电离方程式为NaHSO4![]() Na++H++SO42-。某温度下,向c(H+)=1×10-6 mol·L-1的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的c(H+)=1×10-2 mol·L-1。下列对该溶液的叙述不正确的是
Na++H++SO42-。某温度下,向c(H+)=1×10-6 mol·L-1的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的c(H+)=1×10-2 mol·L-1。下列对该溶液的叙述不正确的是
A. 该温度高于25 ℃
B. 由水电离出来的H+的浓度为1×10-10 mol·L-1
C. 加入NaHSO4晶体会抑制水的电离
D. 取该溶液加水稀释100倍,溶液中的c(OH-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镇痛药物J的合成方法如下:

已知:

(1)B的名称为_________________;F的结构简式为_______________。
(2)C中含氧官能团名称为_______________;②的反应类型为____________反应。
(3)③的化学方程式为_______________________________ 。
(4)有机物K分子组成比F少两个氢原子,符合下列要求的K的同分异构体有________种。
A.遇FeCl3显紫色 B.苯环上有三个取代基
(5)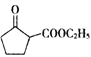 是一种重要的化工中间体。以环已醇(
是一种重要的化工中间体。以环已醇(![]() )和乙醇为起始原料,结合己知信息选择必要的无机试剂,写出
)和乙醇为起始原料,结合己知信息选择必要的无机试剂,写出 的合成路线____________________。(已知:RCH=CHR’
的合成路线____________________。(已知:RCH=CHR’![]() RCOOH+R’COOH,R、R'为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
RCOOH+R’COOH,R、R'为烃基。用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表是一座开放的“元素大厦”,元素大厦尚未充满。若发现119号元素,请您在元素大厦中安排好它的“房间”
A. 第八周期第ⅠA族B. 第七周期第0族
C. 第七周期第ⅦA族D. 第六周期ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应原理在科研和生产中有广泛应用,根据题意回答下列问题:
I工业上制备Na2S的反应原理如下
①Na2SO4(s)===Na2S(s)+2O2(g) △H1=+1011.0kJ·mol-1
②C(s)+O2(g)===CO2(g) △H2=-393.5kJ·mol-1
③2C(s)+O2(g)===2CO(g) △H3=-221.0kJ·mol-1
④Na2SO4(s)+4C(s)===Na2S(s)+4CO(g) △H4
(1)△H4=___________ kJ·mol-1。
(2)反应④能自发进行的条件是___________。
(3)工业上制备Na2S不用反应①,而用反应④的理由是_____________________________。
Ⅱ.在一定温度下,向某恒容密闭容器中充入等物质的量的NO和CO发生反应:2NO(g)+2C0(g) ![]() 2CO2(g)+N2(B) △H=-748kJ/mo1。用气体传感器测得不同时间NO的浓度如下:
2CO2(g)+N2(B) △H=-748kJ/mo1。用气体传感器测得不同时间NO的浓度如下:
时间(s) | 0 | 10 | 20 | 30 | 40 | …… |
C(NO)/mol/L | 0.100 | 0.050 | 0.025 | 0.010 | 0.010 | …… |
(1)计算此温度下该反应的K=______________________。
(2)达到平衡时,下列措施能提高NO转化率的是___________(填序号)。
A.选用更有效的催化剂
B.降低反应体系的温度
C.充入氩气使容器内压强增大
D.充入CO使容器内压强增大
Ⅲ.工业上常用臭氧处理含NO2-的废水。
(1)O3氧化NO2-可产生NO3-和O2,反应中每生成1mol的O2转移___________mol电子。
(2)O3可由电解稀硝酸制得,原理如图。图中阴极为___________(填“A”或“B”),阳极(惰性电极)的电极反应式为____________________________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com