
【题目】(1)K2SO4和Al2(SO4)3饱和溶液中c(K+)=0.2mol·L-1,c(SO42-)=0.7mol·L-1。
①写出Al2(SO4)3的电离方程式____________。
②c(Al3+)等于______mol·L-1。
(2)粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥沙等不溶性杂质。我们食用的精盐是用粗食盐提纯而得到的。回答下列问题。
①除去Mg2+,需要加入的碱溶液为(从下列选项中选出答案,填字母,下同):___;除去SO42-,需要加入的盐溶液为:______。
A.NaOH B.KOH C.BaCl2 D.Ba(NO3)2
②经过操作①后再加入饱和Na2CO3溶液,直至不再产生沉淀为止。这步操作的目的是:除去_____和_____。(填写离子符号)
③将经过操作②后的悬浊液过滤,滤液中还有两种杂质,最后在滤液中加入适量的溶液是(填溶质化学式)_________。
【答案】Al2(SO4)3=2Al3++3SO42- 0.4 A C Ca2+ Ba2+ HCl
【解析】
(1)①Al2(SO4)3是强电解质,在溶液中发生完全电离;②根据K2SO4和Al2(SO4)3混合溶液中溶液中正负离子之和为0可知,![]() ,由于c(K+)=0.2mol·L-1,c(SO42-)=0.7mol·L-1,可以解得;
,由于c(K+)=0.2mol·L-1,c(SO42-)=0.7mol·L-1,可以解得;
(2)①除去Mg2+,需要加入碱溶液,为了不引入新的杂质,因此需要加入NaOH溶液;除去SO42-,需要加入钡盐,为了不引入新的杂质,加入BaCl2;②经过操作①后再加入饱和Na2CO3溶液,直至不再产生沉淀为止,是为了除去粗盐中的Ca2+,以及操作①未反应的Ba2+;③将经过操作②后的悬浊液过滤,滤液中还有CO32-和OH-两种杂质,为除去这两种杂质,最后在滤液中加入HCl。
(1)①Al2(SO4)3是强电解质,在溶液中发生完全电离,电离方程式为:Al2(SO4)3=2Al3++3SO42-;②根据K2SO4和Al2(SO4)3混合溶液中溶液中正负离子之和为0可知,![]() ,由于c(K+)=0.2mol·L-1,c(SO42-)=0.7mol·L-1,故
,由于c(K+)=0.2mol·L-1,c(SO42-)=0.7mol·L-1,故![]() =0.4mol/L;
=0.4mol/L;
(2)①除去Mg2+,需要加入碱溶液,为了不引入新的杂质,因此需要加入NaOH溶液,答案选A;除去SO42-,需要加入钡盐,为了不引入新的杂质,加入BaCl2,答案选C;②经过操作①后再加入饱和Na2CO3溶液,直至不再产生沉淀为止,是为了除去粗盐中的Ca2+,以及操作①未反应的Ba2+;③将经过操作②后的悬浊液过滤,滤液中还有CO32-和OH-两种杂质,为除去这两种杂质,最后在滤液中加入HCl,反应的离子方程式为:H++OH-=H2O,CO32-+2H+=CO2+H2O。


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
【题目】我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2=H2O2+S,已知甲池中发生的反应:


下列说法正确的是( )
A. 甲池中碳棒上发生的电极反应为AQ+2H+-2e-=H2AQ
B. 乙池溶液中发生的反应为H2S+I3-=3I-+S+2H+
C. 该装置中电能转化为光能
D. H+从甲池移向乙池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.2mol MnO2和50mL 12mol·L-1盐酸混合后缓慢加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀,物质的量为x mol(不考虑盐酸的挥发),则x的取值范围是
A.x=0.3B.x<0.3C.0.3<x<0.6D.以上结论都不对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化学中化合物的结构可用键线式表示,如CH2=CHCH2Br可表示为![]() 。环之间共用一个碳原子的化合物称为螺环化合物,螺[2.2]戊烷(
。环之间共用一个碳原子的化合物称为螺环化合物,螺[2.2]戊烷(![]() )是最简单的一种。下列关于该化合物的说法错误的是( )
)是最简单的一种。下列关于该化合物的说法错误的是( )
A. ![]() 与环戊烯互为同分异构体
与环戊烯互为同分异构体
B. ![]() 二氯代物超过两种
二氯代物超过两种
C. ![]() 所有碳原子均处同一平面
所有碳原子均处同一平面
D. ![]() 的一氯代物有1种,所有碳原子均处同一平面
的一氯代物有1种,所有碳原子均处同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于同分异构体(不考虑立体异构)的数目判断正确的是( )
选项 | A | B | C | D |
分子式(或结构简式) | C5H10O2 | C5H10 |
| C7H16 |
已知条件 | 能与碳酸氢钠反应 | 能使溴 水褪色 | 一氯代物 | 分子中含 有3个甲基 |
同分异构体数目 | 4 | 3 | 4 | 5 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从环己烷可制备1,4-环己二醇,下列有关7步反应(其中无机产物都已略去),试回答:
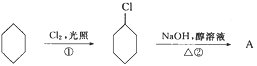
![]()
![]()
(1)本题涉及的有机物中,一共出现了四种不同的官能团,这些官能团的名称为________、________、________、_______。
(2)B的结构简式__________________,C的结构简式__________________。
(3)写出反应①的方程式__________________;③的反应类型是_________________;
(4)写出反应④的反应方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:
![]()
从A出发发生图示中的一系列反应,其中B和C按1:2反应生成Z。F和E按1:2反应生成W,F的核磁共振氢谱只有两种峰,W和Z互为同分异构体。
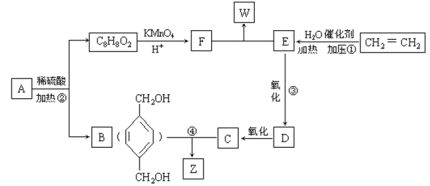
回答下列问题:
(1)写出反应类型:①_____________________,②______________________________。
(2)写出下列反应的化学方程式:
③_____________________________________________________;
④_____________________________________________________。
(3)与B互为同分异构体,属于酚类且苯环上只有两个取代基的化合物有___种(不包括对映异构体)。
(4)A的结构简式可能为_________________________________。
(5)已知酯与醇有如下反应:
RCOOR′+R″OH![]() RCOOR″+R′OH(R、R′、R″代表烃基)
RCOOR″+R′OH(R、R′、R″代表烃基)
B与W在上述条件下可形成高分子化合物Q,请写出B与W生成Q的化学方程式________。
(6)同一碳原子上连两个羟基时结构不稳定,易脱水生成醛或酮:
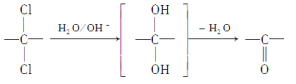
根据已有知识并结合相关信息,写出以对二甲苯为原料(其他无机试剂任选)制备![]() 的合成路线。__________________
的合成路线。__________________
合成路线示意图,如: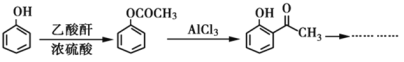
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组依据反应AsO43-+2I-+2H+![]() AsO33-+I2+H2O设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
AsO33-+I2+H2O设计如图原电池,探究pH对AsO43-氧化性的影响。测得电压与pH的关系如图。下列有关叙述错误的是
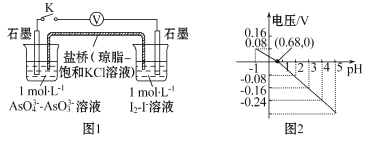
A.调节pH可以改变反应的方向
B.pH=0.68时,反应处于平衡状态
C.pH=5时, 负极电极反应式为2I--2e -= I2
D.pH>0.68时,氧化性I2>AsO43-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨法溶浸氧化锌烟灰制取高纯锌的工艺流程如图所示。溶浸后氧化锌烟灰中锌、铜、镉、砷元素分别以Zn(NH3)42+、Cu(NH3)42+、Cd(NH3)42+、AsCl52-的形式存在。
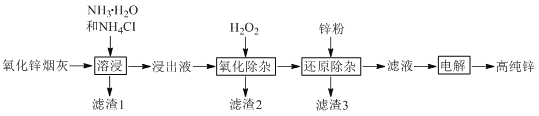
注:“氧化除杂”中,AsCl52-转化为As2O5胶体吸附聚沉除去,溶液始终接近中性。
回答下列问题:
(1)Zn(NH3)42+中Zn的化合价为________,“溶浸”中ZnO发生反应的离子方程式为________。
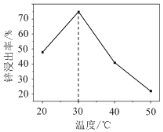
(2)锌浸出率与温度的关系如图所示,分析30 ℃时锌浸出率最高的原因为________。
(3)“滤渣3”的主要成分为________。
(4)“电解”时Zn(NH3)42+在阴极放电的电极反应式为_______。阳极区放出一种无色无味的气体,将其通入滴有KSCN的FeCl2溶液中,无明显现象,该气体是________(写化学式)。电解后的电解液经补充________(写一种物质的化学式)后可返回“溶浸”工序继续使用。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com