
【题目】常温下,用0.05molL﹣1 KOH溶液滴定 10.00mL0.05molL﹣1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(体积变化忽略不计).下列说法错误的是( )
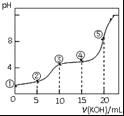
A.点②溶液中:c(K+)+c(H+)=c(HC2O4﹣)+c(C2O42﹣)+c(OH﹣)
B.点③溶液中:c(K+)=c(HC2O4﹣)+c(C2O42﹣)+c(H2C2O4)
C.点④溶液中:c(K+)+c(H2C2O4)+c(HC2O4﹣)+c(C2O42﹣)=0.05 molL﹣1
D.点⑤溶液中:c(K+)>c(HC2O4﹣)>c(C2O42﹣)>c(OH﹣)>c(H+)
【答案】AD
【解析】
A.任何电解质溶液中都存在电荷守恒,根据电荷守恒得c(K+)+c(H+)=c(HC2O4﹣)+2c(C2O42﹣)+c(OH﹣),故A错误;
B.二者恰好完全反应生成KHC2O4,该点溶液中溶质为KHC2O4,任何电解质溶液中都存在物料守恒,根据物料守恒得c(K+)=c(HC2O4﹣)+c(C2O42﹣)+c(H2C2O4),故B正确;
C.点④溶液中存在等物质的量浓度的K2C2O4和KHC2O4,由物料守恒可知,c(K+)+c(H2C2O4)+c(HC2O4﹣)+c(C2O42﹣)=![]() =0.05molL﹣1,故C正确;
=0.05molL﹣1,故C正确;
D.该点溶液中二者恰好完全反应,溶液中溶质为K2C2O4,草酸根离子水解导致溶液呈碱性,但其水解程度较小,所以c(HC2O4﹣)<c(C2O42﹣),故D错误;
故答案为AD。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】A~F都是有机化合物,它们的转化关系如下:
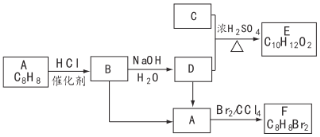
请回答下列问题:
(1)化合物C中含有官能团的名称为________,A为一取代芳香烃,共面的碳原子最多有________个。
(2)D中含有一个甲基,由B生成D的化学方程式为________。
(3)由A生成B的反应类型为________。
(4)由B生成A的反应条件是________。
(5)E存在于栀子香油中,其结构简式为________。
(5)在F的同分异构体中,苯环上一硝化产物只有一种,核磁共振有两组峰且峰面积比为![]() 的是________(填结构简式)。
的是________(填结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)工业合成氨的原理为N2(g)+3H2(g)2NH3(g) H=-92.4kJ·mol-1。现将6molN2和14molH2充入如图所示密闭容器中,保持压强不变,开始时活塞的位置如图1所示,当反应达到平衡时,活塞的位置如图2所示。

①下列表述能说明反应已达到平衡的是___(填字母)。
A.活塞不再移动
B.容器内压强不再改变
C.容器内气体密度不再改变
D.容器内气体的平均相对分子质量不再改变
②已知某次反应过程中逆反应速率随时间的变化关系如图所示,在t1时刻改变了某一条件,则改变的一种条件是_____。

(2)治理NO的一种方法是先将NO氧化成NO2后,再将NO2通入还原性碱溶液中电解转化成N2,其中氧化的反应原理为NO(g)+O3(g)NO2(g)+O2(g) H<0。下列说法正确的是____(填字母)。
A.已知该反应在较低温度下能自发进行,说明S=0
B.加入催化剂,可降低反应的活化能和焓变,从而加快反应的速率
C.活化分子有效碰撞理论中,活化能指活化分子平均能量与非活化分子平均能量的差值
D.在一定温度下,向恒容密闭容器中充入物质的量之比为1:3的NO和O3,达到平衡时NO转化率为a,再充入一定量物质的量之比为1:3的NO和O,NO转化率不变。
(3)处理汽车尾气中的氮氧化物还可以用NH3还原法,假设在恒容密闭容器中,仅发生反应:![]() △H<0。测得NO的平衡转化率随温度的变化关系如图所示,已知温度为T3时,反应达到平衡所需时间为10min。请在图中画出不同温度下(其他条件均相同),反应都经过10min时,NO转化率的曲线示意图_____________。
△H<0。测得NO的平衡转化率随温度的变化关系如图所示,已知温度为T3时,反应达到平衡所需时间为10min。请在图中画出不同温度下(其他条件均相同),反应都经过10min时,NO转化率的曲线示意图_____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中,不能用勒夏特列原理解释的是
A. 冰镇的啤酒打开后泛起泡沫
B. 对N2+3H2![]() 2NH3的反应,使用铁触媒可加快合成氨反应的速率
2NH3的反应,使用铁触媒可加快合成氨反应的速率
C. 工业制取金属钾Na(l)+KCl(l)![]() NaCl(l)+K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来
D. 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸混合溶液100mL,逐渐加入铁粉,产生气体的量随铁粉加入量的变化如图所示.下列说法错误的是( )

A.H2SO4浓度为4mol/L
B.溶液中最终溶质为FeSO4
C.原混合酸中NO3﹣浓度为0.2mol/L
D.AB段反应为:Fe+2Fe3+→3Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙炔(C2H2)和丙烯腈(![]() )是有机合成工业的重要原料。工业上曾用CaC2和H2O反应制取乙炔,用乙炔和氢氰酸(HCN)在氯化亚铜等催化作用下生产丙烯腈。
)是有机合成工业的重要原料。工业上曾用CaC2和H2O反应制取乙炔,用乙炔和氢氰酸(HCN)在氯化亚铜等催化作用下生产丙烯腈。
(1) Cu+的基态核外电子排布式为________。Cu元素在周期表中位置____________。无水CuSO4晶体是白色晶体,溶于水得蓝色溶液,显蓝色的离子的化学式为___________;向蓝色的硫酸铜溶液中滴加氨水直至过量,再加入无水乙醇,最终现象是___________。
(2)![]() 的电子式为________。
的电子式为________。
(3) 与CN-互为等电子体的分子是________(填常见、稳定物质的化学式)。
(4) 丙烯腈分子中碳原子轨道的杂化类型是________。
(5) 1 mol丙烯腈分子中含π键的数目为________mol。
(6)丙烯腈(![]() )分子中共面的原子数目最多为________。
)分子中共面的原子数目最多为________。
(7)H2O分子的VSEPR模型是________,分子的立方体构型是____________。水凝结成冰,冰中水分子的配位数是__________冰的密度比水小,原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前环境问题已有多种解决方案,垃圾是放错地方的财富,上海实行垃圾分类的措施获得一致好评,某科研小组利用惰性电极和离子交换膜对厨房垃圾发酵液进行直流电渗析法处理可得到乳酸(HA),其原理如图所示(图中HA表示乳酸分子,A—表示乳酸根离子)。下列说法正确的是( )
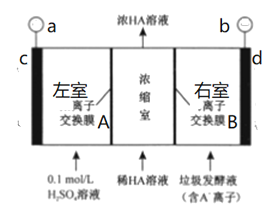
A.电子从电源a极流到c极,从d极流入电源b极
B.离子交换膜B为阳离子交换膜
C.通电后,左室的pH会上升
D.c电极发生的反应为:2H2O-4e-=4H++O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图是短周期的一部分,若c原子的最外层上有5个电子,则下列说法中错误的是
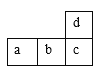
A.a单质可跟d的最高价氧化物对应的水化物反应
B.原子半径a>b>c﹥d
C.b的氢化物比c的氢化物不稳定
D.a的最高价氧化物的水化物比b的最高价氧化物的水化物酸性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某石油化工产品X的转化关系如图,下列判断不正确的是( )
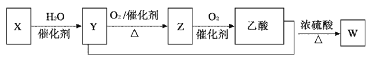
A. X可以发生加聚反应B. Y能与钠反应产生氢气
C. Z与CH3OCH3互为同分异构体D. W的结构简式为CH3COOC2H5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com