
【题目】羟氡(NH2OH)为一元弱碱(25℃时,电离常数Kb=9.0×l0-9),其电离方程式为:NH2OH+H2O![]() NH3OH++OH-。用0.lmol/L盐酸滴定20mL0.lmol/L NH2OH溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(己知:lg3=0.5)。下列说法不正确的是( )
NH3OH++OH-。用0.lmol/L盐酸滴定20mL0.lmol/L NH2OH溶液,恒定25℃时,滴定过程中由水电离出来的H+浓度的负对数与盐酸体积的关系如图所示(己知:lg3=0.5)。下列说法不正确的是( )
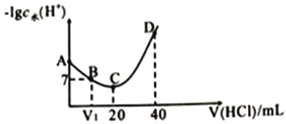
A. A、B、C、D四点对应的溶液中NH2OH电离常数相等
B. A点对应溶液的pH=9.5
C. D点对应溶液中存在:c(H+)=c(OH-)+c(NH3OH+)+c(NH2OH)
D. C点时,溶液呈酸性
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。

(1)写出装置甲的电解总反应方程式________________________________________。
(2)为完成上述实验,正确的连接顺序为E→_________________(填写连接的字母)。
(3)对硬质玻璃管里的氧化铜粉末进行加热前,需要先通一段时间某气体并检验该气体的纯度,检验该气体已经纯的具体的操作和现象为_______________________________。
(4)乙装置的a瓶溶液可选用__________________。
A.淀粉碘化钾溶液 B.酸性高锰酸钾溶液 C.硫化钠溶液 D.Fe(NO3)2溶液
(5)若a瓶中盛放过量的NaHSO3溶液,写出发生的离子反应方程式_____________________。
(6)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案。精确测量硬质玻璃管的质量为a g,加入CuO后,精确测量硬质玻璃管和CuO的总质量为b g , 实验完毕后:
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
乙方案不足之处是________________________________________________________。
按甲方案进行计算,Cu的相对原子质量为__________。(用含a、b、c的式子来表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. ![]() 溶液和
溶液和![]() 溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分相同
溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分相同
B. 配制![]() 溶液时,将
溶液时,将![]() 固体溶解在硫酸中,然后再用水稀释到所需的浓度
固体溶解在硫酸中,然后再用水稀释到所需的浓度
C. ![]() 溶液不可保存在带磨口玻璃塞的玻璃瓶中
溶液不可保存在带磨口玻璃塞的玻璃瓶中
D. 泡沫灭火器中常使用的原料是碳酸钠和硫酸铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是 ( )
A. 0.1molH218O与D2O的混合物中所含中子数为NA
B. 17g羟基所含电子的数目为10NA
C. lLpH=l的H2SO4溶液中含有的H+数目为0.2NA
D. 密闭容器中1molH2(g)与1molI2(g)共热反应制备HI增加2NA个H-I键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不用其他试剂,用最简单的方法鉴别下列物质 ①NaOH溶液 ②Mg(NO3)2溶液 ③CuSO4溶液 ④KCl溶液;
正确的鉴别顺序是( )
A.①②③④
B.③④②①
C.④①②③
D.③①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳的化合物的转换在生产、生活中具有重要的应用,如航天员呼吸产生的CO2用Sabatier反应处理,实现空间站中O2的循环利用。
Sabatier反应:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g);
CH4(g)+2H2O(g);
水电解反应:2H2O(1) ![]() 2H2(g) +O2(g)。
2H2(g) +O2(g)。
(1)将原料气按n(CO2):n(H2)=1:4置于密闭容器中发生Sabatier反应,测得H2O(g)的物质的量分数与温度的关系如图所示(虚线表示平衡曲线)。

①该反应的平衡常数K随温度降低而________(填“增大”或“减小”)。
②在密闭恒温(高于100℃)恒容装置中进行该反应,下列能说明达到平衡状态的是_____。
A.混合气体密度不再改变 B.混合气体压强不再改变
C.混合气体平均摩尔质量不再改变 D. n(CO2):n(H2)=1:2
③200℃达到平衡时体系的总压强为p,该反应平衡常数Kp的计算表达式为_______。(不必化简,用平衡分,压代替平衡浓度计算,分压=总压×物质的量分数)
(2)Sabatier反应在空间站运行时,下列措施能提高CO2转化率的是____(填标号)。
A.适当减压 B.合理控制反应器中气体的流速
C.反应器前段加热,后段冷却 D.提高原料气中CO2所占比例
(3)一种新的循环利用方案是用Bosch反应CO2(g)+4H2(g)![]() C(s)+2H2O(g)代替Sabatier反应。
C(s)+2H2O(g)代替Sabatier反应。
①已知CO2(g)、H2O(g)的生成焓分别为-394kJ/mol、-242kJ/mol,Bosch反应的△H=_____kJ/mol。(生成焓指一定条件下由对应单质生成lmol化合物时的反应热)
②一定条件下Bosch反应必须在高温下才能启动,原因是______________。若使用催化剂,则在较低温度下就能启动。
③Bosch反应的优点是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强酸性无色透明溶液中,下列各组离子能大量共存的是( )
A.Zn2+、Al3+、SO42-、Cl-B.Ag+、Na+、NO3-、Cl-
C.Fe3+、K+、Cl-、NO3-D.Ba2+、NH4+、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】难挥发性二硫化钽(TaS2)可采用如下装置提纯。将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下:TaS2(s)+2I2(g) ![]() TaI4(g)+S2(g)下列说法正确的是
TaI4(g)+S2(g)下列说法正确的是

A. 在不同温度区域,TaI4的量保持不变
B. 在提纯过程中,I2的量不断减少
C. 在提纯过程中,I2的作用是将TaS2从高温区转移到低温区
D. 该反应的平衡常数与TaI4和S2的浓度乘积成反比
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com