
【题目】用一种硫化矿(含45%SiO2、20.4% Al2O3、30%FeS和少量GeS2等)制取盆景肥料NH4Fe(SO4)2及铝硅合金材料的工艺流程如下 :
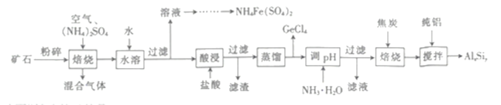
(1)“矿石”粉碎的目的是_____________________ 。
(2)“混合气体”经过水吸收和空气氧化能再次利用。
①“焙烧”时,GeS2发生反应的化学方程式为____________________。
②“混合气体”的主要成分是_______________ (填化学式).
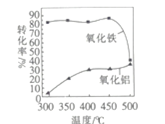
③FeS焙烧产生的Fe2O3会与(NH4)2SO4反应生成NH4Fe(SO4)2,该反应的化学方程式为_______________。 Al2O3也能发生类似反应.这两种氧化物转化为硫酸盐的转化率与温度的关系如图,上述流程中最适宜的“焙烧” 温度为_____________________。
(3)GeCl4的佛点低,可在酸性条件下利用蒸馏的方法进行分离,酸性条件的目的是_________。
(4)用电解氧化法可以增强合金 AlxSiy的防腐蚀能力,电解后在合金表面形成致密、耐腐蚀的氧化膜(主要成分为Al2O3), 电解质溶液为 H2SO4-H2C2O4混合溶液,阳极的电极反应式为______________________。
(5)假设流程中SiO2 损失了20%,Al2O3 损失了25%,当投入1 t硫化矿,加入了54kg纯铝时,铝硅合金中x:y=______________。
【答案】使矿石充分灼烧 GeS2+3O2![]() GeO2+2SO2 SO2、NH3 4(NH4)2SO4+Fe2O3
GeO2+2SO2 SO2、NH3 4(NH4)2SO4+Fe2O3![]() 2NH4Fe(SO4)2+3H2O+6NH3↑ 300℃ 防止GeCl4水解 2Al-6eˉ+3H2O =Al2O3+6H+ 5:6
2NH4Fe(SO4)2+3H2O+6NH3↑ 300℃ 防止GeCl4水解 2Al-6eˉ+3H2O =Al2O3+6H+ 5:6
【解析】
硫化矿(含45%SiO2、20.4% Al2O3、30%FeS和少量GeS2等)粉碎后加入硫酸铵在空气中焙烧,-2价S被氧化生成SO2,Ge元素转化为GeO2,FeS焙烧产生的Fe2O3会与(NH4)2SO4反应生成NH4Fe(SO4)2,控制焙烧温度,防止Al2O3也发生类似的反应;加水后,NH4Fe(SO4)2溶解,经系列处理得到NH4Fe(SO4)2;过滤得到滤渣为SiO2、Al2O3和GeO2,加盐酸溶解,Al2O3和GeO2得到的相应的氯化物,二氧化硅不溶解,过滤得到二氧化硅滤渣;蒸馏分离滤液中的GeCl4后再加入氨水调节pH得到Al(OH)3沉淀,过滤取Al(OH)3沉淀,与前序滤渣SiO2和焦炭高温焙烧还原得到Al和Si,再加纯铝搅拌得到合金。
(1)矿石粉碎后可以增大与空气的接触面积,使矿石充分灼烧;
(2)①“焙烧”时,GeS2中-2价S被氧化生成SO2,Ge元素转化为GeO2,方程式为GeS2+3O2![]() GeO2+2SO2;
GeO2+2SO2;
②混合气体中主要有硫元素被氧化生成的SO2,以及铵盐分解产生的NH3;
③Fe2O3会与(NH4)2SO4反应生成NH4Fe(SO4)2,该反应为非氧化还原反应,根据元素守恒可得方程式为4(NH4)2SO4+Fe2O3![]() 2NH4Fe(SO4)2+3H2O+6NH3↑;因流程的目的是要是制备NH4Fe(SO4)2和硅铝合金,所以要使Fe2O3尽量反应,而Al2O3不反应,据图可知300℃时大部分氧化铁转化为硫酸盐,只有极少量氧化铝转化为硫酸盐,所以最合适的温度为300℃;
2NH4Fe(SO4)2+3H2O+6NH3↑;因流程的目的是要是制备NH4Fe(SO4)2和硅铝合金,所以要使Fe2O3尽量反应,而Al2O3不反应,据图可知300℃时大部分氧化铁转化为硫酸盐,只有极少量氧化铝转化为硫酸盐,所以最合适的温度为300℃;
(3)GeCl4易水解,蒸馏过程中会HCl挥发造成彻底水解,所以需要在酸性条件下防止GeCl4水解,再进行蒸馏;
(4)电解池中阳极失电子发生氧化反应,根据题意可知Al单质被氧化成三氧化二铝,电解质溶液显酸性,所以电极方程式为2Al-6eˉ+3H2O =Al2O3+6H+;
(5)1 t硫化矿中SiO2的质量为1000kg×45%=450kg,流程中损失20%,所以被利用的二氧化硅的质量为450kg×(1-20%)=360kg,则n(Si)=![]() =6000mol;1 t硫化矿中SiO2的质量为1000kg×20.4%=204kg,流程中损失25%,所以被利用的Al2O3的质量为204kg×(1-25%)=153kg,又加入54kg铝,则n(Al)=
=6000mol;1 t硫化矿中SiO2的质量为1000kg×20.4%=204kg,流程中损失25%,所以被利用的Al2O3的质量为204kg×(1-25%)=153kg,又加入54kg铝,则n(Al)=![]() =5000mol,所以合金AlxSiy中x:y=5:6。
=5000mol,所以合金AlxSiy中x:y=5:6。


科目:高中化学 来源: 题型:
【题目】我国科学家意外发现一种罕见无机化合物YZX2W3(结构如图所示) ,其中W、X、Y为同一短周期元素, X、Z为短周期同一主族元素且Z的核电荷数是X的2倍,下列说法正确的是

A.元素非金属性强弱顺序为X>Y> W
B.Z的氧化物的水化物是强酸
C.NaY的水溶液不能存放在玻璃试剂瓶中
D.X与Z具有相同的最高化合价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯氧化铜[xCuO·yCuCl2·zH2O]在农业上可用作杀菌剂。以废铜(主要杂质为Fe)为原料,经溶解氧化、调节pH、过滤等步骤,可制备氯氧化铜。
(1)工业上用H2O2和HCl溶解氧化废铜时,反应生成Cu2+时的离子方程式为________。
(2)加Cu2(OH)2CO3调节混合液pH时,其优点是________。
(3)为测定氯氧化铜的组成,现进行如下实验:
步骤Ⅰ:称取0.4470 g氯氧化铜固体,放入锥形瓶中,加入一定量30%的硝酸使固体完全溶解。滴加K2CrO4溶液作指示剂,用0.100 0 mol·L-1 AgNO3标准溶液滴定溶液中的Cl-,滴定至终点时消耗AgNO3标准溶液20.00 mL(已知Ag2CrO4为砖红色沉淀)。
步骤Ⅱ:称取0.2235 g氯氧化铜固体,放入锥形瓶中,加入一定量硫酸使固体完全溶解。溶液中加入过量的KI固体,充分反应后向溶液中滴入数滴淀粉溶液,用0.200 0 mol·L-1 Na2S2O3标准溶液滴定,滴定至终点时消耗Na2S2O3标准溶液10.00 mL。
已知步骤Ⅱ中所发生的反应如下:2Cu2++4I-===2CuI↓+I2;2Na2S2O3+I2===2NaI+Na2S4O6。
①步骤Ⅰ滴定终点时的实验现象是_____。
②通过计算确定氯氧化铜的化学式(写出计算过程)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为3L的密闭容器中化学反应CO(g)+2H2(g)![]() CH3OH(g)达到平衡状态。
CH3OH(g)达到平衡状态。
(1)该反应的平衡常数表达式K=__;根据图,升高温度,K值将__(填“增大”、“减小”或“不变”)。
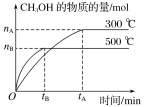
(2)500℃时,从反应开始到化学平衡状态,以H2的浓度变化表示的化学反应速率是__(用nB、tB表示)。
(3)判断该可逆反应达到化学平衡状态的标志是__(填字母,下同)。
a.υ生成(CH3OH)=υ消耗(CO) b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变 d.CO、H2、CH3OH的浓度均不再变化
(4)300℃时,将容器的容积压缩到原来的![]() ,在其他条件不变的情况下,对平衡体系产生的影响是____。
,在其他条件不变的情况下,对平衡体系产生的影响是____。
a.c(H2)减小 b.正反应速率加快,逆反应速率减慢
c.CH3OH的物质的量增加 d.重新平衡时![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关系正确的是( )
A.熔点:正戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷
B.密度:CCl4>苯>H2O
C.同质量的物质燃烧耗O2量:甲烷>乙烯>乙炔
D.同物质的量的下列物质燃烧耗O2量:环已烷>苯=乙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨和硝酸都是重要的工业原料。
(1)标准状况下,将500 L氨气溶于水形成1 L氨水,则此氨水的物质的量浓度为__mol· L-1(保留三位有效数字)。工业上常用过量氨水吸收二氧化硫,该反应的化学方程式为__。
(2)氨氧化法是工业生产中合成硝酸的主要途径。合成的第一步是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮,该反应的化学方程式为__。
下列反应中的氨与氨氧化法中的氨作用相同的是__。
A.2Na+2NH3===2NaNH2+H2↑ B.2NH3+3CuO===3Cu+N2+3H2O
C.4NH3+6NO===5N2+6H2O D.HNO3+NH3===NH4NO3
工业中的尾气(假设只有NO和NO2)用烧碱进行吸收,反应的离子方程式为2NO2+2OH﹣===NO2-+NO3-+H2O和NO+NO2+2OH﹣===□ +H2O(配平该方程式)。______________
(3)向27.2 g Cu和Cu2O的混合物中加入某浓度的稀HNO3500 mL,反应过程中产生的气体只有NO。固体完全溶解后,在所得溶液(金属阳离子只有Cu2+)中加入1 L 1 mol·L-1的NaOH溶液使金属离子恰好完全沉淀,此时溶液呈中性,所得沉淀质量为39.2 g。
①Cu与稀HNO3反应的离子方程式为__。
②Cu与Cu2O 的物质的量之比为__。
③HNO3的物质的量浓度为__mol·L-1。
(4)有H2SO4和HNO3的混合溶液20 mL,加入0.25 molL﹣1Ba(OH)2溶液时,生成沉淀的质量w(g)和Ba(OH)2溶液的体积V(mL)的关系如图所示(C 点混合液呈中性)。则原混合液中H2SO4的物质的量浓度为__mol·L-1,HNO3的物质的量浓度为__mol·L-1。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海冰是海水冻结而成的咸水冰,海水冻结时,部分来不及流走的盐分(设以NaCl为主)以卤汁的形式被包裹在冰晶之间,形成“盐泡”,其大致结构如图所示,若海冰的冰龄达到1年以上,则融化后的水为淡水。下列叙述正确的是
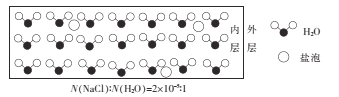
A.海冰内层“盐泡”越少,密度越大
B.海冰冰龄越短,内层的“盐泡”越少
C.每含1mol H2O的海冰内就有2×l0-5 NA个NaCl分子(NA为阿伏加德罗常数)
D.海冰内层NaCl的浓度约为l0-3 mol/L(设冰的密度为0.9 g.cm-3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计装置,进行实验探究KMnO4与浓盐酸的反应。
[实验1]设计如图1所示装置,并验证氯气的漂白性。
(1)高锰酸钾与浓盐酸的反应中,浓盐酸表现出的性质是_________;若实验中产生2.24 L(标准状况)Cl2,设NA为阿伏加德罗常数的值,则转移的电子数为___________。
(2)利用装置C验证氯气是否具有漂白性,则装置中I、II、III处依次放入的物质可能是__________________。
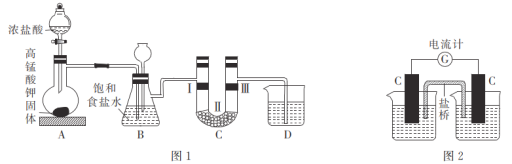
[实验2]设计如图2所示装置,左侧烧杯中加入100 mL由2.00 mol·L-1 KMnO4和6 mol·L-1 H2SO4组成的混合溶液,右侧烧杯中加入100 mL 5.00 mol·L-1 BaCl2溶液,盐桥选择KNO3琼脂。
(3)若用98%的浓硫酸(密度为1.84 g·cm-3)配制500 mL 6 mol·L-1的稀硫酸时,除了需用到玻璃棒、烧杯、量筒之外,还必须用到的玻璃仪器为____________;下列操作会导致所配溶液浓度偏小的是____________(填字母)。
A.容量瓶内壁附有水珠却未干燥处理 B.加水定容时俯视刻度线
C.颠倒摇匀后发现凹液面低于刻度线又加水补足 D.稀释过程中有少量液体溅出烧杯外
(4)左侧烧杯中石墨电极上的电极反应式为________________________________;盐桥中的K+移向____________ (填“左”或“右”)侧烧杯的溶液中。
(5)实验发现,其他条件不变,改用10.0 mol·L-1 H2SO4时,生成氯气的速率比使用6 mol·L-1 H2SO4时快且产生的气体体积更大,其可能的原因是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质,以C4H10为燃料,该电池工作原理如图。下列说法正确的是( )
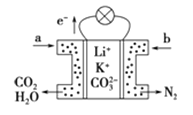
A.a为![]() ,b为
,b为![]()
B.在熔融电解质中,![]() 向正极移动
向正极移动
C.此电池在常温时也能工作
D.通入丁烷的一极是负极,电极反应式为![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com