
����Ŀ���Ӻ�ˮ�п�����ȡ�ܶ����õ����ʣ�����Ӻ�ˮ�������õ���±ˮ�п�����ȡ�⡣����̿�������ǹ�ҵ���ķ���֮һ�����������£�

������ʾ����. pH=2ʱ��NaNO2��Һֻ�ܽ� I������ΪI2��ͬʱ����NO
��. I2+5Cl2+6H2O === 2HIO3+10HCl
��. 5SO32��+2IO3��+2H+===I2+5SO42��+H2O
��1����Ӧ�ٵ����ӷ���ʽ____________________��
��2���������У�����I2�����ԣ��������X�ķ�����____________��
��3����֪����Ӧ����ÿ����3mol I2ת��5mol���ӣ����ӷ���ʽ��__________��
��4��Cl2������KMnO4�ȶ��dz��õ�ǿ�����������ù���������±ˮ�е�I��ȴѡ���˼۸�ϸߵ�NaNO2��ԭ����_______________________��
��5���������У���֪��Ӧ�۹��˺���Һ���Դ���������I2��I����IO3�������ֱ�������Һ�е�I����IO3������ʵ�鷽������������ʵ���пɹ�ѡ����Լ���ϡH2SO4��������Һ��Fe2(SO4)3��Һ��Na2SO3��Һ
a.��Һ��CCl4�����ȡ����Һ��ֱ��ˮ���õ�����Һ���鲻���ⵥ�ʴ��ڡ�
b._____________________��
���𰸡� 2NO2��+2 I��+4H+===I2+2NO +2H2O ��������ȡ������ᾧ���������ᾧ���۷֣� 3 I2+3CO32��===5 I��+ IO3��+3CO2 ��3 I2+6 CO32��+3H2O===5 I��+ IO3��+6HCO3�� ���������Ը�����صȶ��dz��õ�ǿ�����������������I2(���������ƽ��ܰѵ����������ɵⵥ��,��˼�Լ���) ��ˮ��ȡ������Һ���Թ��У����뼸�ε�����Һ���μ�Fe2(SO4)3��Һ������Һ������˵����Һ�к���I��������ˮ����ȡ������Һ���Թ��У����뼸�ε�����Һ���������ữ���μ�Na2SO3��Һ������Һ������˵����Һ�к���IO3��
����������1����Ӧ��ΪpH=2ʱ��NaNO2��Һ�� I������ΪI2��ͬʱ����NO�����䷴Ӧ�����ӷ���ʽΪ��2NO2��+2 I��+4H+===I2+2NO +2H2O����2������I2�����������ԣ��������X�ķ�������������ȡ������ᾧ����3��������֪��������Ӧ����ÿ����3mol I2ת��5mol���ӣ������������ԭ��Ӧ�е�ʧ������Ϊ5����0������Ϊ+5�ۺʹ�0�۽���Ϊ-1�ۣ��������ӷ���ʽ�ǣ�3I2+3CO32��=5I��+ IO3��+3CO2 ��3I2+6 CO32��+3H2O=5I��+ IO3��+6HCO3������4��Cl2������KMnO4�ȶ��dz��õ�ǿ�����������ù���������±ˮ�е�I��ȴѡ���˼۸�ϸߵ�NaNO2��ԭ�������������Ը�����صȶ��dz��õ�ǿ�����������������I2���Ӷ��ò���I2����5��������Һ�е�I������ѡ���������������������ĵⵥ�������۱�����������Һ�е�IO3�������û�ԭ�����仹ԭ�����ⵥ�������۱������Ӷ��ü죬�ʷ���Ϊ����ˮ��ȡ������Һ���Թ��У����뼸�ε�����Һ���μ�Fe2(SO4)3��Һ������Һ������˵����Һ�к���I��������ˮ����ȡ������Һ���Թ��У����뼸�ε�����Һ���������ữ���μ�Na2SO3��Һ������Һ������˵����Һ�к���IO3����


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����л�������Ժ��ֱ�ֵ��ϣ�ֻҪ�������ʵ���֮�Ͳ��䣬��ȫȼ��ʱ�����ĵ����������ʵ��������ɵ�ˮ�����ʵ����ֱ���ȵ���
A��������Ҵ� B��������Ҵ�
C�����ͱ����� D����Ȳ�ͱ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������¼������л���ѧ��Ϊһ�Ŷ�����ѧ��֧���ǣ� ��
A.1828��¹���ѧ��ά���״���ʵ������ϳ�������
B.19���ͳ�����仯ѧ�ұ�������˹�״�ʹ�á��л���һ�ʣ�������ˡ��л���ѧ���͡��л�������ĸ���
C.1965���ҹ���ѧ���˹��ϳ��˾���������Եĵ����ʩ����ᾧţ�ȵ���
D.1830�꣬�¹���ѧ�����ϣ�������л�������Ķ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2KMnO4��5H2C2O4��3H2SO4��K2SO4��2MnSO4��10CO2����8H2O��
ij��ѧС�����������Ӧԭ����������ʵ�飺
�����ⶨH2C2O4��Һ�����ʵ���Ũ��
ʵ�鲽�����£�
��ȡ����H2C2O4��Һ25.00mL������ƿ�У��ټ���������ϡ���
����0.1mol��L��1KMnO4��Һ�ζ����յ㣬��¼���ݣ�
���ظ��ζ�2�Σ�ƽ������KMnO4��Һ20.00mL��
��ش�
��1���ζ�ʱ����KMnO4��Һװ��________��������ʽ��������ʽ�����ζ����С�
��2�����ڲ���������֮ǰ�����ô���H2C2O4��Һ��ϴ��ƿ������H2C2O4��Һ��Ũ�Ȼ�________������ƫ������ƫС��������Ӱ��������
��3���������е���ζ��յ�ʱ������Ϊ________��
��4������H2C2O4��Һ�����ʵ���Ũ��Ϊ________mol��L��1��
����̽����Ӧ��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ���������ʵ�鷽����ʵ���¶Ⱦ�Ϊ25������
ʵ����� | ���V��mL | |||
0.1mol��L��1KMnO4��Һ | 0.1mol��L��1H2C2 O4��Һ | 0.1mol��L��1H2SO4��Һ | H2O | |
�� | 2.0 | 5.0 | 6.0 | 7.0 |
�� | 2.0 | 8.0 | 6.0 | V1 |
�� | 2.0 | V2 | 6.0 | 2.0 |
��ش�
��5������V1��________��V2��________��
��6��ʵ������Ҫ������������________��
��7��ʵ����________������������������������0.2mol��L��1�������0.1mol��L��1H2SO4��Һ��������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W��ԭ�����������������У�XԪ��ԭ�ӵ��������������ڲ��������2����X��Z�ĺ˵����֮��Ϊ3��4��W��Z�����WZ2��WZ3���ֻ���������ֻ�����֮���ͨ�����淴Ӧ�ת�����ش��������⣺
��1��ZԪ����Ԫ�����ڱ��е�λ����________________��WԪ��ԭ�ӵĽṹʾ��ͼΪ____________________��
��2��ʵ������ȡYԪ����̬�⻯��Ļ�ѧ����ʽΪ________________________��
��3�����������£�WԪ������������Ӧˮ�����Ũ��Һ��XԪ�صĵ��ʷ�����Ӧ��д���÷�Ӧ�Ļ�ѧ����ʽ________________________���ռ���Ӧ���������壬ijͬѧ�����ͼװ�ü����������ɣ��Լ�������������Aƿ�е��Լ���_____________________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. ��������ʾ��ѧ��Խ�ι̣�Խ���Զ���
B. �ɼ�����ԭ�Ӻ�Խ��������Խ�̣���ѧ��Խ�ι̣��γɵ����ʵ�����Խ�ȶ�
C. �ƻ���ѧ��ʱ�������������γɻ�ѧ��ʱ�ͷ�����
D. �������������������I��I���ļ��ܴ�С�й�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ϊ�˼����Լ���������������ֵ�Ԫ������Ϊ�ǡ��أ������ǣ�84Po��Ԫ�ص�һ��ͬλ�ص�����������������1.49������ԭ�ӵ�������Ϊ�� ��
A.84
B.125
C.209.16
D.209
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ����ˮ�ܽ⡢���ˡ������Ȳ������ɽ����и������������ǣ�������
A.����ء���������
B.����ͭ����������
C.�Ȼ��ء���������
D.����ͭ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ྦྷ���ǵ��ʹ��һ����̬�����������Ƭ��̫���ܵ�ؼ��ߴ����ƾ�����Ҫԭ�ϡ���֪�ྦྷ���������ҵ��ȡ������ͼ��ʾ��
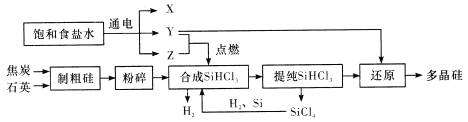
����˵���������
A. Y��Z�ֱ�ΪH2��Cl2
B. ��ȡ�ֹ�Ĺ����н�̿��ʯӢ�ᷢ������Ӧ����̼���裬�ڸø���Ӧ�У��������뻹ԭ�������ʵ���֮��Ϊ1��1
C. SiHCl3����ˮ�⣬����ȫˮ��IJ���ΪH2SiO3��H2��HCl���ݴ��Ʋ�SiHCl3�й�Ԫ�صĻ��ϼ�Ϊ+2��
D. Y��SiHCl3�Ʊ��ྦྷ��ķ�Ӧ�����û���Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com