
【题目】氰![]() 的化学性质与卤素
的化学性质与卤素![]() 很相似,化学上称之为拟卤素,其氧化性介于
很相似,化学上称之为拟卤素,其氧化性介于![]() 和
和![]() 之间,下列有关反应方程式不正确的是
之间,下列有关反应方程式不正确的是 ![]()
![]()
A.![]() 和NaOH溶液反应:
和NaOH溶液反应:![]()
B.![]() 和HCN反应:
和HCN反应:![]() 浓
浓![]()
C.向KCN溶液中加入碘水:![]()
D.在NaBr和KCN混合溶液中通入少量![]() :
:![]()
科目:高中化学 来源: 题型:
【题目】选做[化学—选修3:物质结构与性质] (15分)X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大。X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子单电子数在同周期元素中最多,W与Z同周期,第一电离能比Z的低,R与Y同一主族,Q的最外层只有一个电子,其他电子层电子均处于饱和状态。请回答下列问题:
(1)R核外电子排布式为__________________。
(2)X、Y、Z、W形成的有机物YW(ZX2)2中Y、Z的杂化轨道类型分别为__________,ZW3-离子的立体构型是__________。
(3)Y、R的最高价氧化物的沸点较高的是_____________(填化学式),原因是_________________。
(4)将Q单质的粉末加入到ZX3的浓溶液中,并通入W2,充分反应后溶液呈深蓝色,该反应的离子方程式为______________________________________。
(5)W和Na的一种离子化合物的晶胞结构如图,该离子化合物为____________(填化学式)。Na+的配位数为_____________,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为__________。已知该晶胞的密度为ρg·cm-3,阿伏加德罗常数为NA,则两个最近的W离子间距离为 nm(用含ρ、NA的计算式表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以NH3代替氢气研发燃料电池是当前科研的一个热点。使用的电解质溶液是2mol·L1的KOH溶液,电池总反应为:4NH3+3O2=2N2+6H2O。该电池负极的电极反应式为____________________;每消耗3.4g NH3转移的电子数目为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不同条件下,用O2氧化a mol/L FeCl2溶液过程中所测的实验数据如图所示。下列分析或推测合理的是
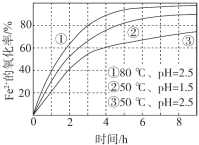
A. 由①、②可知, pH越大,+2价铁越易被氧化
B. 由②、③推测,若pH>7,+2价铁更难被氧化
C. 由①、③推测,FeCl2被O2氧化的反应为放热反应
D. 60℃、pH=2.5时, 4 h内Fe2+的平均消耗速率大于 0.15a mol/(L·h)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机化合物的同分异构体数目判断正确的是( )
A. 分子式为C5H10,含碳碳双键的烯烃为6种
B. 分子式为C8H10,含苯环的有机物为3种
C. 分子式为C5H12O,且能与Na反应的有机物为8种
D. 分子式为C5H10O2,且能与Na2CO3反应的有机物为10种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)戊烷的某种同分异构体只有一种一氯代物,试书写它的结构简式______
(2)分子式为C6H12的某烃的所有碳原子都在同一平面上,则该烃的结构简式为_________,若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为__________。
(3)某芳香烃结构为![]() 。它的分子式为________,一氯代物有________种。
。它的分子式为________,一氯代物有________种。
(4)分子式为C8H10的芳香烃,苯环上的一氯代物只有一种,该芳香烃的结构简式是______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雷美替胺是首个没有列为特殊管制的非成瘾失眠症治疗药物,合成该有机物过程中涉及如下转化,下列说法不正确的是( )
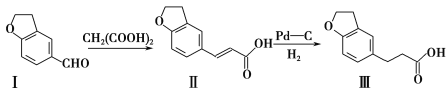
A.溴水无法区分化合物I和化合物Ⅱ
B.化合物Ⅰ、Ⅱ、Ⅲ均能与NaHCO3溶液发生反应
C.1 mol化合物Ⅲ最多能与3 mol H2发生加成反应
D.化合物Ⅰ、Ⅱ、Ⅲ分子中不存在手性碳原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属及其化合物在国民经济发展中起着重要作用。
(1)铜在潮湿的空气中能发生吸氧腐蚀而生锈,铜锈的主要成分为Cu2(OH)2CO3(碱式碳酸铜)。该过程中负极的电极反应式为_________。
(2)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其原理如图所示:
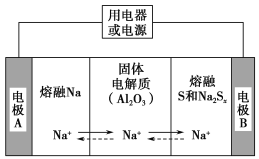
①根据下表数据,请你判断该电池工作的适宜温度应控制在_________。
物质 | Na | S | Al2O3 |
熔点/℃ | 97.8 | 115 | 2 050 |
沸点/℃ | 892 | 444.6 | 2 980 |
a.100 ℃以下 b.100 ℃~300 ℃
c.300 ℃~350 ℃ d.350 ℃~2 050 ℃
②放电时,电极A为_________极,S发生_________反应。
③放电时,内电路中Na+的移动方向为_________(填写“从A到B”或“从B到A”)。
④充电时,总反应为Na2Sx=2Na+Sx(3<x<5),Na所在电极与直流电源_________极相连,阳极的电极反应式________。
(3)某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。
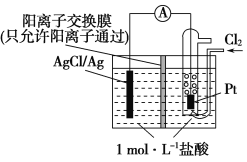
①正极反应为_________。
②当电路中转移0.005 mol e-时,交换膜左侧溶液中约减少_________mol离子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是氢氧燃料电池构造示意图。下列说法不正确的是( )

A. a极是负极
B. 电流由b通过灯泡流向a
C. 该电池总反应是2H2+ O2=2H2O
D. b极的电极反应为:O2+2H2O+4e-=4OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com