
【题目】下列有关实验现象的预测或装置的选用正确的是
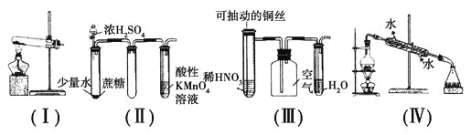
A.用装置(Ⅰ)加热草酸晶体获取某些气体(草酸晶体的熔点101.5 ℃,分解温度约为150 ℃)
B.用装置(Ⅱ)进行实验时,酸性KMnO4溶液中出现气泡,且颜色逐渐褪去
C.用装置(Ⅲ)进行实验时,广口瓶内先有浅红棕色气体出现后又变为无色,且不会产生空气污染
D.用装置(Ⅳ)分离溴苯和苯的混合物
科目:高中化学 来源: 题型:
【题目】某同学研究铝及其化合物的性质时设计了如下两个实验方案:
方案①:2.7 g Al![]() X溶液
X溶液![]() Al(OH)3沉淀
Al(OH)3沉淀
方案②:2.7 g Al![]() Y溶液
Y溶液![]() Al(OH)3沉淀
Al(OH)3沉淀
NaOH溶液和稀盐酸的浓度均是3 mol·L-1,如图是向X溶液和Y溶液中分别加入NaOH溶液或稀盐酸时产生沉淀的物质的量与加入盐酸或氢氧化钠溶液体积之间的关系。下列说法正确的是( )

A. X溶液溶质为AlCl3,Y溶液溶质为NaAlO2
B. b曲线表示的是向X溶液中加入NaOH溶液
C. 在O点时两方案中所得溶液浓度相等
D. a、b曲线表示的反应都是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧杯中盛有物质的量浓度相等的盐酸、氢氧化钠溶液各1 L,分别向其中加入等质量的铝片,反应完全后,甲中产生H2的体积为2.24 L,乙中产生H2的体积为3.36 L(气体体积均在标准状况下测定),则下列判断正确的是
A. 甲、乙中铝都有剩余
B. 铝片的质量是1.8 g
C. 盐酸或氢氧化钠的物质的量浓度为0.1 mol/L
D. 盐酸或氢氧化钠的物质的量浓度为0.2 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是
A. 液氨汽化时要吸收大量的热,常用作制冷剂
B. 新能源汽车的推广与使用有助于减少光化学烟雾的产生
C. 手机外壳上贴的碳纤维外膜是一种新型的无机非金属材料
D. 海水淡化能解决淡水供应危机,向海水中加净水剂明矾可以使海水淡化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据相关概念下列说法正确的是
A. 只含共价键的物质一定是共价化合物
B. 氯化钠发生状态变化时,一定会破坏离子键
C. 物质中分子间的作用力越大,分子越稳定
D. 都是由非金属元素形成的化合物只能是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示元素周期表的前三周期,表中的字母各代表一种元素,请回答下列问题:

①写出D单质的电子式____________;A与E的上一周期同主族元素形成的原子个数比为1:1的化合物的电子式_______________。
②E和F分别形成的气态氢化物中较稳定的是(填写氢化物的化学式)_____________;
③A的最高价氧化物对应的水化物中所含化学键为___________________,其水溶液与B单质反应的离子方程式为___________________________;
④写出实验室制备F单质的化学方程式______________________________________。
⑤将Fe与C的一种单质(导体)用导线连接,共同浸入到食盐水中构成闭合回路,其中C极为_____极(填正或负),该电极反应式为:____________________。
⑥以D2H4和O2为原料,与KOH溶液形成的原燃料电池中,负极反应式为___________,
(生成物对环境友好无污染)
当外电路转移0.2 mol电子时,消耗的O2在标准状况下的体积为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物在酸性催化条件下发生水解反应,生成两种不同的有机物,且这两种有机物的相对分子质量相等,该有机物是( )
①蔗糖②麦芽糖③乙酸丙酯④丙酸丙酯
A. ①③ B. ②④ C. ①④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,将1.0L c molL-1CH3COOH溶液与0.1molNaOH固体混合,使之充分反应。然后向该混合溶液中加入CH3COOH或CH3COONa固体(忽略体积和温度变化),引起溶液pH的变化如图所示。下列叙述错误的是

A. 水的电离程度:c>b>a
B. a点对应的混合溶液中,C(CH3COOH)>C(Na+ )>c(OH-)
C. 该温度下,醋酸的电离平衡常数Ka=![]()
D. 当混合溶液呈中性时,c(Na+ )=c(CH3COO-)>c(H+) =c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是( )

A. 如上图所示是测定中和热的简易装置,大小两烧杯间填满碎泡沫塑料的作用是固定小烧杯
B. 若用50 mL 0.55 mol·L-1的氢氧化钠溶液,分别与50 mL 0.50 mol·L-1的盐酸和50 mL0.50 mol·L-1的硫酸充分反应,两反应测定的中和热不相等
C. 实验时需要记录初始温度T1和最高温度T2
D. 做一次实验根据公式即可得出中和反应的反应热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com