
【题目】图中表示2NO(g)+O2(g)![]() 2NO2(g)△H<0,能正确反映该可逆反应变化的图象是( )
2NO2(g)△H<0,能正确反映该可逆反应变化的图象是( )
A. 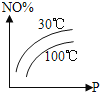 B.
B. 
C.  D.
D. 
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图是常见的四种有机物的比例模型示意图。下列说法正确的是( )

A. 甲能使酸性高锰酸钾溶液褪色
B. 乙可与溴水发生取代反应使溴水褪色
C. 丙在铁作催化剂条件下与溴水发生取代反应
D. 丁在浓硫酸、加热条件下可与乙酸发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷、乙烯和苯都是重要的化工原料,请回答下列问题。
(1)甲烷的电子式为__________,写出在光照条件下,甲烷与氯气发生反应生成气态有机物的化学方程式:________。
(2)下列叙述不正确的是________
A. CH4与C4H10互为同系物 B. C5H12有3种同分异构体
C. 烷烃的卤代反应很难得到纯净物 D. 烷烃分子中,相邻的三个碳原子可能在同一条直线
(3) 下列物质不可能是乙烯加成产物的是(__________)
A. CH3CH3 B. CH3CHCl2 C. CH3CH2OH D. CH3CH2Br
(4)若将乙烯通入到紫色高锰酸钾溶液中,可以观察到__________,乙烯发生的反应类型为________。
(5) 苯的结构简式:________,它与液溴在催化剂作用下发生取代反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“C1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH、HCOOH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。
(1)一定温度下,在两个容积均为2 L的密闭容器中,分别发生反应:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。相关数据如下:
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。相关数据如下:
容器 | 甲 | 乙 |
反应物投入量 | 1molCO2(g)和 3molH2(g) | 1mol CH3OH (g)和 1molH2O(g) |
平衡时c(CH3OH) | c1 | c2 |
平衡时能量变化 | 放出29.4kJ | 吸收a kJ |
请回答:
①a=_______________;
②若甲中反应10 s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是___________。
(2)甲烷的一个重要用途是制取H2,其原理为CO2(g)+CH4(g) ![]() 2CO(g)+2H2(g)。在密闭容器中通入等物质的量浓度的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示,则压强p1_____(填“大于”或“小于”)p2;压强为p2时,在y点:v(正)______(填“大于”“小于”或“等于”)v(逆)。
2CO(g)+2H2(g)。在密闭容器中通入等物质的量浓度的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示,则压强p1_____(填“大于”或“小于”)p2;压强为p2时,在y点:v(正)______(填“大于”“小于”或“等于”)v(逆)。

(3)一定条件下,治理汽车尾气的反应是2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g) ΔH<0。在恒温恒容的密闭容器中通入n(NO)∶n(CO)=2∶1的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是________(填字母)。
2CO2(g)+N2(g) ΔH<0。在恒温恒容的密闭容器中通入n(NO)∶n(CO)=2∶1的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时刻一定达到平衡状态的是________(填字母)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是国际化学元素周期表年。1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列;准确的预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。

下列说法不正确的是
A.元素甲的原子序数为31
B.元素乙的简单气态氢化物的沸点和稳定性都低于CH4
C.原子半径比较:甲>乙>Si
D.乙的单质可以作为光电转换材料用于太阳能电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质检验是化学研究常用的方法之一。下列有关溶液成分的检验,结论不正确的是
A.若滴加酚酞溶液,溶液变红,原溶液不一定是碱溶液
B.若先滴加足量新制氯水,再滴加少量KSCN溶液,溶液变为血红色,则原溶液一定含有Fe2+
C.若滴加Na2CO3溶液,产生白色沉淀,则原溶液可能含有Ca2+
D.若滴加稀盐酸,产生能使澄清石灰水变浑浊的气体,则原溶液中可能含CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,使H2和O2的混合气体26g充分发生反应,所得产物在适当温度下跟足量的固体Na2O2反应,使固体增重2g。原混合气体中H2和O2的物质的量之比为( )
A.1:10B.9:1C.4:1D.4:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.在如图装置中,用 NaOH 溶液、铁屑、稀 H2SO4 等试剂制备 Fe(OH)2。

(1)在试管Ⅰ里加入的试剂是_____;
(2)在试管Ⅱ里加入的试剂是_____;
(3)为了制得白色 Fe(OH)2 沉淀,在试管Ⅰ和Ⅱ中加入试剂后应________(填“打开”或者“关闭”)止水夹,反应一会儿后应________(填“打开”或者“关闭”)止水夹。
II.某化学兴趣小组用下图装置制取并探究氯气的性质。[A装置中发生反应的化学方程式:2KMnO4+16HCl(浓)=2KCl+2MnCl2 + 5Cl2↑+ 8H2O ]

(1)A装置中a仪器的名称是_____________。
(2)实验室制氯气也可用MnO2与浓盐酸反应,化学方程式为:_____
(3)实验进行一段时间后,可观察到______(填“B”或“C”)装置中有色布条褪色,请用化学方程式表示其褪色原因__________。
(4)当氯气进入D装置后,可观察到溶液颜色变为____(填“红色”或“蓝色”),写出该反应的离子方程式为_________。
(5)E装置中反应的化学方程式为________。
(6)用31.6 g KMnO4固体与足量的浓盐酸反应,最多可生成标准状况下_____L氯气。(KMnO4的摩尔质量为158 g·mol-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2和CH4催化重整可制备合成气,对减缓燃料危机具有重要意义,其反应历程示意图如图:

下列说法不正确的是( )
A.合成气的主要成分为CO和H2
B.①→②过程可表示为CO2+NiC=2CO+Ni
C.①→②过程吸收能量
D.Ni在该反应中做催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com