
【题目】下列固体中经充分加热分解,无固体残留的是( )
A.NH4HCO3B.NaHCO3C.Al(OH)3D.CaCO3
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.为除去FeSO4溶液中的Fe2(SO4)3,可加入铁粉,再过滤
B.为除去溴苯中的溴,可用NaOH溶液洗涤,再分液
C.为除去乙炔气中少量的H2S,可使其通过CuSO4溶液
D.为除去CO2中少量的SO2,可使其通过饱和Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国自主研制的大型客机C919的机身大量使用铝锂合金材料。这是利用了铝锂合金性质中的( )
A.高强度、低密度B.高强度、导热性
C.低密度、导电性D.导电性、导热性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟是一种卤族元素。但它与其他卤素在单质和化合物的制备与性质上存在较明显的差异
(1)研究发现,SbF5能将MnF4从离子[MnF6]2-的盐中反应得到,SbF5转化成稳定离子[SbF6]-的盐。而MnF4很不稳定,受热易分解为MnF3和F2。根据以上研究写出以K2MnF6和SbF5为原料,在423 K的温度下制备F2的化学方程式:____________________。
(2)现代工业以电解熔融的氟氢化钾(KHF2)和氟化氢(HF)混合物制备氟单质,电解制氟装置如图所示。
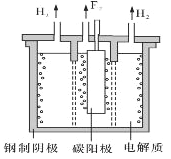
①已知KHF2是一种酸式盐,写出阴极上发生的电极反应式______________。
②电解制氟时,要用镍铜合金隔板将两种气体产物严格分开的原因是____________ 。
③HF的水溶液能用于蚀刻玻璃,其化学反应方程式为:_____________________。
④已知25℃时,氢氟酸(HF)的电离平衡常数Ka=3.6×10-4。某pH=2的氢氟酸溶液,由水电离出的c(H+)=_________mol/L;若将0.01 mol/L HF溶液与pH=12的NaOH溶液等体积混合,则溶液中离子浓度大小关系为:__________________。
⑤又已知25℃时,溶度积常数Ksp(CaF2)=1.46×10-10。现向1L0.2 mol/L HF溶液中加入1L0.2 mol/L CaCl2溶液,____________(填“是”、“否”) 有沉淀产生,并通过列式计算说明__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奈必洛尔是一种用于血管扩张的降血压药物。用于合成奈必洛尔中间体G的部分流程如图:
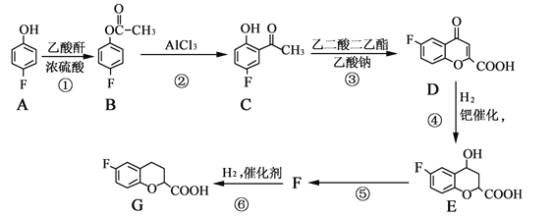
已知:乙酸酐的结构简式为![]() ,请回答下列问题:
,请回答下列问题:
(1)G物质中的官能团的名称是羧基、_____________、__________________;
(2)反应A→B的化学方程式为_____________________;
(3)写出满足下列条件的C的同分异构体的结构简式:__________、_____________;
Ⅰ苯环上只有两种取代基。 Ⅱ.分子中只有4种不同化学环境的氢。Ⅲ.能与NaHCO3反应生成CO2。
(4)根据已有知识并结合相关信息,写出以![]() 和乙酸酐为原料制备
和乙酸酐为原料制备![]() 的合成路线流程图(无机试剂任选)。___________________。
的合成路线流程图(无机试剂任选)。___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求填空:
(1)相同物质的量的O2和O3的质量比 , 分子个数比为 , 所含氧原子的个数比为 .
(2)在200mL 2mol/L MgCl2溶液中,溶质的质量为g.此溶液中Mg2+的物质的量浓度为mol/L,Cl﹣的物质的量浓度为mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向溴化钠、碘化钠的混合溶液中通入足量氯气,加热将溶液蒸干,并灼烧至质量不再改变为止,最后残留的物质是 ( )
A.NaClB.NaCl、NaBr、NaIC.NaBr、NaID.NaI
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com