
【题目】25℃时,取浓度均为0.2mol·L-1的醋酸溶液和氨水溶液各10 mL,分别用0.1 mol·L-1NaOH溶液、0.1 mol·L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示。下列说法正确的是 ( )
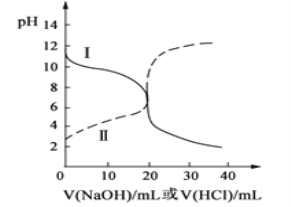
A. 曲线Ⅰ:滴加溶液到10 mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B. 曲线Ⅰ:滴加溶液到20 mL时:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C. 曲线Ⅱ:滴加溶液到10 mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]
D. 曲线Ⅱ:滴加溶液在10 mL~20 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+)
【答案】C
【解析】
根据未加盐酸和氢氧化钠时图象纵坐标所对应pH值可知,曲线Ⅰ线是盐酸滴定氨水,因为当未滴加溶液时,Ⅰ的pH>7;曲线Ⅱ线是氢氧化钠滴定醋酸滴定氨水,因为当未滴加溶液时,曲线Ⅱ的pH<7。
A项、曲线Ⅰ线是盐酸滴定氨水,故A错误;
B项、曲线I为酸滴定碱溶液,当滴加溶液到20mL时,溶液中的溶质是氯化铵,溶液呈酸性,则c(H+)>c(OH-),溶液中存在电荷守恒c(Cl-)+c(OH-)=c(NH4+)+c(H+),所以得c(Cl-)>c(NH4+),盐类水解程度较小,所以离子浓度大小顺序为:c(Cl-)>c(NH4+)>c(H+)>c(OH-),故B正确;
C项、滴加溶液到10mL时,溶液中的溶质是等物质的量浓度的醋酸和醋酸钠,溶液中存在物料守恒c(CH3COO-)+c(CH3COOH)=2c(Na+),溶液中存在电荷守恒c(CH3COO-)+c(OH-)=c(H+)+c(Na+),所以得c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)],故C正确;
D项、曲线Ⅱ线是氢氧化钠滴定醋酸滴定氨水,故D错误。
故选C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断不正确的是( )
A. 第二阶段,Ni(CO)4分解率较高
B. 该反应达到平衡时,4v(Ni(CO)4)生成=v(CO)生成
C. 增加c(CO),平衡向正向移动,反应的平衡常数增大
D. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吸烟有害健康,烟草中的剧毒物尼古丁的结构简式如右图所示,有关其叙述正确的是( )
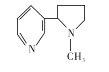
A. 尼古丁分子中的六元环不是正六边形
B. 尼古丁分子中的C、N原子均处于同一平面内
C. 该有机物属于芳香族化合物
D. 尼古丁的一氯代物有10种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧是理想的烟气脱硝剂,其脱硝反应为 2NO2(g)+O3(g) ![]() N2O5(g)+O2(g)。有关说法正确的是( )
N2O5(g)+O2(g)。有关说法正确的是( )
A. 增大压强可增大反应速率 B. 升高温度可减小反应速率
C. 达到平衡时,v(正)=v(逆)=0 D. 达到平衡时,NO2转化率为100%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. Al箔插入稀HNO3中,无现象,说明Al箔表面被HNO3氧化,形成致密的氧化膜
B. 如图所示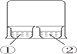 ,①中为AlCl3溶液,②中为浓氨水,①中有白色沉淀生成
,①中为AlCl3溶液,②中为浓氨水,①中有白色沉淀生成
C. AlCl3![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3
Al(OH)3
D. AlCl3溶液中滴加NaOH溶液后铝的存在形式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏德罗常数,下列叙述正确的是 ( )
A. 标准状况下,22.4LH2O含有的分子数为1 NA
B. 常温常压下,16g O2含有的原子数为1 NA
C. 通常状况下,1NA 个SO2分子占有的体积约为22.4L
D. 物质的量浓度为0.5mol/L的K2SO4溶液中,含有SO42-个数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】① NaOH ② CH3COOH ③ NaHCO3 ④ HCl溶液是中学化学中常用的四种物质。
(1)pH相同的CH3COOH和HCl溶液比较,物质的量浓度较大的是____(填序号)。
(2)等体积、等物质的量浓度的CH3COOH和HCl溶液与足量的NaHCO3固体粉末反应,起始反应速率较小的是_______填序号)。
(3)常温下,pH均为10的 NaOH和NaHCO3 溶液,由水电离出的c(OH—)之比为_________________。
(4)常温下,用 0.10 mol/L NaOH溶液滴定 20.00 mL 0.10 mol/L CH3COOH溶液,
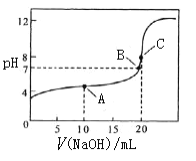
①A点溶质为____________(写化学式),此时c(CH3COO-)_______c(CH3COOH)(填“大于” 、“小于”或“等于”),溶液中水的电离平衡______(填“被抑制”或“被促进”或“无影响”)
②结合化学用语,解释C点pH=8的原因_______________________________________ 。
③下列关于B点的判断正确的是____
a.醋酸和氢氧化钠恰好完全反应
b.混合液中的微粒种类共四种
c.c(CH3COO-) = c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为短周期元素形成的常见单质或化合物(注:A、B、C、D、E可代表各不相同的物质,也可以代表相同的物质),有以下转化关系:
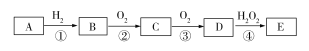
下列说法不正确的是
A. ①②③④步中均发生了氧化还原反应
B. A只能为非金属元素形成的单质
C. Al、Fe均可以在E的浓溶液中发生钝化
D. B、C、D、E均为共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于“摩尔”的理解正确的是
A.摩尔是一个物理量,它表示含有一定数目粒子的集合体
B.摩尔是物质的量的单位,简称摩,符号为mol
C.国际上规定,0.012 kg碳原子所含有的碳原子数目为1摩尔
D.1摩尔任何物质均含有6.02×1023个原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com