



科目:高中化学 来源: 题型:
| A、Ca(OH)2浊液与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O |
| B、稀硫酸滴在铁片上:2Fe+6H+=2Fe3++3H2↑ |
| C、铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag |
| D、大理石溶于醋酸的反应:CaCO3+2H+=Ca2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
 .现有A、B、C、D、E、F六种有机物有如下转化,其中A的分子式为C4H8O3.下列判断正确的是( )
.现有A、B、C、D、E、F六种有机物有如下转化,其中A的分子式为C4H8O3.下列判断正确的是( )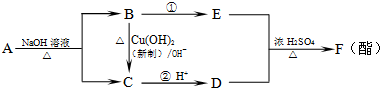
| A、有机物A结构可能有四种 |
| B、反应①属于氧化反应 |
| C、有机物B、D的最简式相同 |
| D、有机物E是交警检测酒驾的重要物证 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
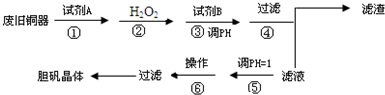
| 物质 | 开始沉淀时的pH值 | 完全沉淀时的pH值 |
| 氢氧化铁 | 2.7 | 3.7 |
| 氢氧化亚铁 | 7.6 | 9.6 |
| 氢氧化铜 | 5.2 | 6.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com