
�о�CO��SO2��NO�ȴ�����Ⱦ������ۺϴ��������þ�����Ҫ���塣
��1����CO��CO2��H2Ϊԭ�ϣ���һ�������¾��ɺϳɼ״�������Ϊ�����ֺϳ������·�����ϡ���ɫ��ѧ��������û�ѧ��Ӧ����ʽ��ʾ�� ��
��2����ͼ��ʾ�����ںϳɼ״���Ʒ�м״������ļ���ǡ�д������������ʱ�ĵ缫��Ӧʽ��
���� ������ ��
��3��һ�������£�NO2��SO2��Ӧ����SO3��g����NO�������壬�ֽ������Ϊ1:2��NO2��SO2�Ļ�����������ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬���� ��������ţ�
| A����ϵѹǿ���ֲ��� | B�����������ɫ���ֲ��� |
| C��SO3��NO������ȱ��ֲ��� | D��ÿ���� 1 mol SO2��ͬʱ����1 mol NO |
��1��CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
��2��������2CH3OH-12e-+2H2O 2CO2+12H+ ������3O2+12e-+12H+ 6H2O
��3�� B 2��67(��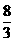 ) ��4��1��7
) ��4��1��7
���������������1����Ϊ��ѧ��Ӧ�Ĺ��̾���ԭ��������ϵĹ��̣����ڡ���ɫ��ѧ�����Ƿ�Ӧ���ԭ����ȫת��ΪĿ�����������ʹ��CO��H2����ȡCH3OH ����Ӧ�ķ���ʽΪ��CO(g)+2H2(g)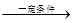 CH3OH(g)����2�����ͨ��״��ĵ缫Ϊ�������缫��ӦΪ��2CH3OH-12e-+2H2O=2CO2+12H+���ұ�ͨ��O2�ĵ缫Ϊ���������������Խ��ʣ������ĵ缫��ӦΪ��3O2+12e-+12H+=6H2O����3��NO2��SO2��Ӧ����SO3��g����NO�ķ���ʽΪ��NO2+SO2
CH3OH(g)����2�����ͨ��״��ĵ缫Ϊ�������缫��ӦΪ��2CH3OH-12e-+2H2O=2CO2+12H+���ұ�ͨ��O2�ĵ缫Ϊ���������������Խ��ʣ������ĵ缫��ӦΪ��3O2+12e-+12H+=6H2O����3��NO2��SO2��Ӧ����SO3��g����NO�ķ���ʽΪ��NO2+SO2 SO3(g)+NO��A���÷�Ӧ�Ƿ�Ӧǰ�����������ȵĿ��淴Ӧ���������۷�Ӧ�Ƿ�ﵽƽ�⣬��Ӧ��ѹǿ�����ᷢ���仯��B�������������ݻ����䣬����Ӧ�ﵽƽ�⣬�κ����ʵ����ʵ������䣬NO2����ɫ�����ʣ���Ũ�Ȳ��䣬���Ի��������ɫ���ֲ��䡣��˸÷�Ӧ�ﵽƽ�⡣��ȷ��C��������ӦNO2+SO2
SO3(g)+NO��A���÷�Ӧ�Ƿ�Ӧǰ�����������ȵĿ��淴Ӧ���������۷�Ӧ�Ƿ�ﵽƽ�⣬��Ӧ��ѹǿ�����ᷢ���仯��B�������������ݻ����䣬����Ӧ�ﵽƽ�⣬�κ����ʵ����ʵ������䣬NO2����ɫ�����ʣ���Ũ�Ȳ��䣬���Ի��������ɫ���ֲ��䡣��˸÷�Ӧ�ﵽƽ�⡣��ȷ��C��������ӦNO2+SO2 SO3(g)+NO ��ÿ����SO31mol,��Ȼͬʱ����NO1mol��������۷�Ӧ�Ƿ�ﵽƽ�⣬SO3��NO�������ʼ�ձ��ֲ��䡣�ʲ�����Ϊ��Ӧ�ﵽƽ��ı�־������D��SO2�Ƿ�Ӧ�NOΪ���������ʽ�ж��ߵ����ʵ����ı�Ϊ1:1,����ÿ���� 1 mol SO2��ͬʱ����1 mol NO ���뷴Ӧ�Ƿ�ﵽƽ���أ���˲�����Ϊ��Ӧ�ﵽƽ��ı�־�������跴Ӧ��ʼʱ��n(NO2)="amol;" n(SO2)=2amol�����ڷ�Ӧ������?n(NO2)="xmol" ����?n(SO2)=xmol,��ﵽƽ���Ƿ�ӦNO2+SO2
SO3(g)+NO ��ÿ����SO31mol,��Ȼͬʱ����NO1mol��������۷�Ӧ�Ƿ�ﵽƽ�⣬SO3��NO�������ʼ�ձ��ֲ��䡣�ʲ�����Ϊ��Ӧ�ﵽƽ��ı�־������D��SO2�Ƿ�Ӧ�NOΪ���������ʽ�ж��ߵ����ʵ����ı�Ϊ1:1,����ÿ���� 1 mol SO2��ͬʱ����1 mol NO ���뷴Ӧ�Ƿ�ﵽƽ���أ���˲�����Ϊ��Ӧ�ﵽƽ��ı�־�������跴Ӧ��ʼʱ��n(NO2)="amol;" n(SO2)=2amol�����ڷ�Ӧ������?n(NO2)="xmol" ����?n(SO2)=xmol,��ﵽƽ���Ƿ�ӦNO2+SO2 SO3(g)+NOƽ����ϵ��n(NO2)=(a-x)mol;n(SO2)=(2a-x)mol;n(SO3)=xmol;n(NO)=xmol������ƽ��ʱNO2��SO2�����Ϊ1:6������(a-x)��(2a-x)=1:6�����
SO3(g)+NOƽ����ϵ��n(NO2)=(a-x)mol;n(SO2)=(2a-x)mol;n(SO3)=xmol;n(NO)=xmol������ƽ��ʱNO2��SO2�����Ϊ1:6������(a-x)��(2a-x)=1:6�����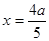 �������ڸ��¶��¸÷�Ӧƽ�ⳣ��
�������ڸ��¶��¸÷�Ӧƽ�ⳣ��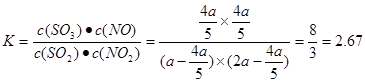 ����4���ɷ���ʽ���Կ�����ÿ����1mol��CO2�����Ļ������2mol�����ڲ���2��24L��־״���µ�CO2��������0��1 mol CO2��������������0��1mol�������������Ħ������Ϊ44g/mol������NOΪxmol, NO2Ϊ(1-x)mol��30x+46(1-x)=44����x:(1-x)=1:7��
����4���ɷ���ʽ���Կ�����ÿ����1mol��CO2�����Ļ������2mol�����ڲ���2��24L��־״���µ�CO2��������0��1 mol CO2��������������0��1mol�������������Ħ������Ϊ44g/mol������NOΪxmol, NO2Ϊ(1-x)mol��30x+46(1-x)=44����x:(1-x)=1:7��
���㣺���黯ѧ��Ӧ�ľ����ԡ�ԭ����е缫��Ӧʽ����д����ѧƽ��״̬���жϡ�ƽ�ⳣ���ļ��㡢�������������ʵĻ�ϱ����ļ����֪ʶ��


 Ŀ�����ϵ�д�
Ŀ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
Ϊ��֤ͭ��ϡ���ᷴӦ�Ļ�ԭ������NO������NO2�����������ͼ��װ�ã����������������
| A��Ӧ�ȴ����ٴ��Ҳ��ϡ���� |
| B�����ϡ������ע�� |
| C���رջ�����ͭ˿��ȫ���ܽ� |
| D����Ӧֹͣ����������ɺ���ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
[��ѧ����ѡ��3�����ʽṹ������]��15�֣�
������Ҫ�İ뵼����ϣ��������ִ����ӹ�ҵ�Ļ������ش��������⣺
��1����̬Siԭ���У�����ռ�ݵ�����ܲ����Ϊ____ �����ܲ���е�ԭ�ӹ����Ϊ____ ��������Ϊ ��
��2������Ҫ�Թ����Ρ�____ �Ȼ��������ʽ�����ڵؿ��С�
��3�����ʹ��������ʯ�ṹ���Ƶľ��壬����ԭ����ԭ��֮���� ���ϣ��侧���й���8��ԭ�ӣ�����������λ�ù���____ ��ԭ�ӡ�
��4�����ʹ��ͨ�����飨SiH4���ֽⷴӦ���Ʊ�����ҵ�ϲ���Mg2Si��NH4C1��Һ�������з�Ӧ�Ƶ�SiH4���÷�Ӧ�Ļ�ѧ����ʽΪ___ ��
��5��̼����йػ�ѧ������������ʾ����Ҫ�����ͽ��������й���ʵ��
�ٹ���̼ͬ�壬Ҳ��ϵ���⻯�������������������϶�Զ���������࣬ԭ���� ��
��SiH4���ȶ���С��CH4���������������ԭ����____ ��
��6���ڹ������У�SiO44�������壨����ͼ��a����ͨ�����ö��������ӿ��γɵ�״����״����״���Ǽ���״�Ĵ���ṹ��ʽ��ͼ��b��Ϊһ�����������ṹ�Ķ�����������Siԭ�ӵ��ӻ���ʽΪ ��Si��O��ԭ����֮��Ϊ ��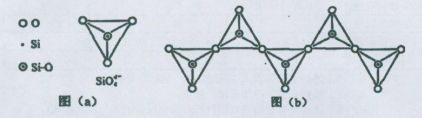
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��13�֣����仯�����й㷺��Ӧ�ã���SO2���ʵ��о��Ǹ��л�ѧ��ѧ��һ����Ҫ���ݡ�
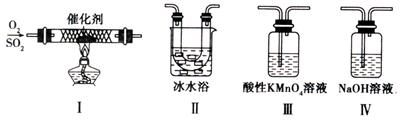
��1���Ա��о���һ����Ҫ���о�������������ĵ��ʼ����ֻ����ﰴ���±���ʾ�ֳ�3�飬���2��������M�Ļ�ѧʽ�� ��
| ��1�� | ��2�� | ��3�� |
| S�����ʣ� | SO2��H2SO3��M��NaHSO3 | SO3��H2SO4����Na2SO4��NaHSO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪ij����X�ܷ�������ת����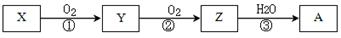
�����й�����ת����ϵ�����ʼ��䷴Ӧ�������������
| A����XΪN2��NH3��������������AΪ���� |
| B����XΪS ��H2S����ȫȼ�գ�����AΪ���� |
| C����XΪ�ǽ������ʻ�ǽ����⻯���A��һ���������ͭ��Ӧ����Y |
| D����Ӧ�ٺ͢�һ��Ϊ������ԭ��Ӧ����Ӧ��һ��Ϊ��������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�������ȣ�ClO2������������ˮ�������Դ���Ϊԭ������ClO2�Ĺ�����Ҫ�������ٴ��ξ��ƣ��ڵ������NaCl��Һ����ClO2����ȡ��������������ͼ��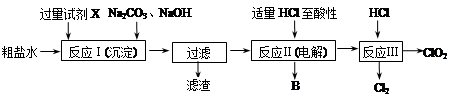
��1����ʳ��ˮ�к���Ca2+��Mg2+��SO42-�����ʡ����Ӳ���ʱ��������ˮ���ȼ���������Լ�X��X���� ��(�ѧʽ)�����������ٲ������ټ��������Na2CO3��NaOH����ַ�Ӧ����һ����ȥ������ⷢ����Һ���Ժ���һ������SO42-����ԭ������ ��������֪��Ksp(BaSO4)��1.1��10��10��Ksp(BaCO3)��5.1��10��9��
��2�����������У���ʳ��ˮ���ض������µ��õ��������������ᷴӦ����ClO2�����ʱ���ɵ�����B���� ������Ӧ��Ļ�ѧ����ʽΪ�� ����
��3��ClO2�ܲ��ȶ������������ƣ�������ˮ���յõ�ClO2��Һ��Ϊ�ⶨ������Һ��ClO2�ĺ���������������ʵ�飺
����1��ȷ��ȡClO2��Һ10.00 mL��ϡ�ͳ�100 mL������
����2����ȡV1mL�������뵽��ƿ�У�����������pH��2.0������������KI���壬ҡ�ȣ��ڰ�������30���ӡ�(��֪��ClO2��I����H+��I2��Cl����H2O δ��ƽ)
����3���Ե�����Һ��ָʾ������c mol��L��1Na2S2O3��Һ�ζ����յ㣬����Na2S2O3��ҺV2 mL������֪��I2��2S2O32-��2I����S4O62-��
�� ȷ��ȡ10.00 mL ClO2��Һ�IJ����������� ����
�� �ζ������У�������ƽ�вⶨ���ε�ԭ������ ����
�� ������������ɼ����ԭClO2��Һ�����ʵ���Ũ��Ϊ����mol��L��1���ú���ĸ�Ĵ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
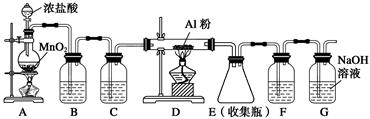
��γ�ȥ���и���ĩ״������е�����(������Ϊ����)����ѡ�������ṩ���Լ��Ͳ�������������ڱ��ڡ�
��ѡ�Լ���A���B�ռ���Һ��C������Dˮ��ECO2��F���������Լ�
��ѡ�������ټ��ȣ��ڼ������ڣ��۹��ˣ��ܽᾧ
| �����ʵ����� | �����Լ� | ��Ҫ���� |
| (1)SiO2(NaHCO3) | | |
| (2)SiO2(CaCO3) | | |
| (3)SiO2(Si) | | |
| (4)NaCl(SiO2) | | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ڻ�ѧ����Χ��Ũ����Ļ�ѧ���ʽ���������ʵ��̽���������������Ƿ����ձ��У����뼸��ˮ��������ȣ�Ȼ�����Ũ���ᣬ���ɺ�ɫ���ʡ�
��ش��������⣺
(1)���ɵĺ�ɫ����(����)�� (�ѧʽ)��
(2)���ֺ�ɫ���ʼ�����Ũ�������û�����������壬����һ�������д̼�����ζ���Ǵ�������Ҫ��Ⱦ��֮һ�����ִ̼�����ζ������ɷ��� (�ѧʽ)����Ӧ�Ļ�ѧ����ʽΪ ��
(3)��������Ũ���ᷴӦ��ʵ������˵��Ũ������� (�����)��
| A������ | B����ˮ�� | C����ˮ�� | D��ǿ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(1)�����뺬�Ȼ������йص�˵����ȷ����________(����ĸ)��
| A��HClO�����ᣬ����NaClO��������� |
| B�����ˮ����μ�����������FeCl3��Һ�����Ƶ�Fe(OH)3���� |
| C��HCl��Һ��NaCl��Һ��ͨ�����ӵ��磬����HCl��NaCl�������ӻ����� |
| D�����NaCl��Һ�õ�22.4 L H2(��״��)����������Ҫת��NA������(NA��ʾ�����ӵ�����) |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com