
【题目】已知下列热化学方程式:①H2(g)+ ![]() O2(g)=H2O(l)△=﹣285.8kJmol﹣1②H2(g)+
O2(g)=H2O(l)△=﹣285.8kJmol﹣1②H2(g)+ ![]() O2(g)=H2O(g)△H=﹣241.8kJmol﹣1
O2(g)=H2O(g)△H=﹣241.8kJmol﹣1
③C(s)+ ![]() O2(g)=CO(g)△H=﹣110.5kJmol﹣1
O2(g)=CO(g)△H=﹣110.5kJmol﹣1
④C(s)+O2(g)=CO2(g)△H=﹣393.5kJmol﹣1 ,
回答下列问题:
(1)上述反应中属于放热反应的是(填序号)
(2)C的燃烧热为
(3)燃烧20g H2生成液态水,放出的热量为
(4)写出CO燃烧的热化学方程式 .
【答案】
(1)①②③④
(2)393.5kJ/mol
(3)2858KJ
(4)CO(g)+ ![]() O2 (g)=CO2 (g)△H=﹣283.0kJ/mol
O2 (g)=CO2 (g)△H=﹣283.0kJ/mol
【解析】解:(1)热化学方程式中△H为负值的反应为放热反应,所以上述反应中属于放热反应的是①②③④,所以答案是:①②③④;(2)1mol纯净物完全燃烧生成稳定的氧化物所放出的热量为燃烧热,则C的燃烧热为393.5kJ/mol;所以答案是:393.5kJ/mol;(3)由H2(g)+ ![]() O2(g)=H2O(l)△=﹣285.8kJmol﹣1可知1mol H2完全燃烧生成液态水,放出的热量为285.8kJ,所以20g H2生成液态水,放出的热量为
O2(g)=H2O(l)△=﹣285.8kJmol﹣1可知1mol H2完全燃烧生成液态水,放出的热量为285.8kJ,所以20g H2生成液态水,放出的热量为 ![]() ×285.8kJmol﹣1=2858KJ;
×285.8kJmol﹣1=2858KJ;
所以答案是:2858KJ;(4)已知③C(s)+ ![]() O2(g)═CO(g)△H=﹣110.5kJ/mol
O2(g)═CO(g)△H=﹣110.5kJ/mol
④C(s)+O2(g)═CO2(g)△H=﹣393.5kJ/mol,
把方程式④﹣③得:CO(g)+ ![]() O2 (g)=CO2 (g)△H=﹣283.0kJ/mol,
O2 (g)=CO2 (g)△H=﹣283.0kJ/mol,
所以答案是:CO(g)+ ![]() O2 (g)=CO2 (g)△H=﹣283.0kJ/mol.
O2 (g)=CO2 (g)△H=﹣283.0kJ/mol.
【考点精析】本题主要考查了吸热反应和放热反应的相关知识点,需要掌握化学上把吸收热量的化学反应称为吸热反应;化学上把放出热量的化学反应称为放热反应才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】将 4mol A 气体和 2mol B 气体在 2L 的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)2C(g),若经 2s (秒)后测得 C 的浓度为 0.6molL﹣1 , 现有下列几种说法,其中正确的是( )
A.用物质A表示的反应的平均速率为0.3 molL﹣1s﹣1
B.用物质B表示的反应的平均速率为0.6 molL﹣1s﹣1
C.2 s 时物质A的转化率为70%
D.2 s 时物质B的浓度为1.4 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的综合利用对于改善大气质量和能源充分利用有重要的意义.
(1)下列说法正确的是(填序号).
a.煤是由有机物和少量无机物组成的复杂混合物
b.煤在燃烧过程中会生成一氧化碳、二氧化硫、氮氧化物、烟尘等有害物质
c.可利用生石灰、熟石灰、石灰石等固硫剂使煤在燃烧过程中生成稳定的硫酸盐
d.煤的干馏属于化学变化、煤的气化和液化都属于物理变化
(2)煤的气化过程中产生的有害气体H2S用氨水吸收生成正盐的离子方程式是 .
(3)燃煤烟气的一种脱硫方案﹣火碱一石灰一石膏法流程图1如下. 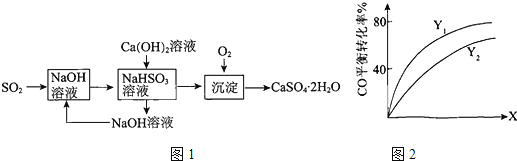
①常温下,用NaOH溶液吸收SO2得到pH=6的NaHSO3溶液,该溶液中离子浓度的大小顺序是
②氢氧化钙与NaHSO3反应的化学方程式是
(4)煤的间接液化法合成二甲醚的三步反应如下:Ⅰ.2H2(g)+CO(g)CH3OH(g)△H=﹣90.8kJmol﹣1
Ⅱ.2CH3OH(g)CH3OCH3(g)+H2O(g)△H=﹣23.5kJmol﹣1
Ⅲ.CO(g)+H2O(g)CO2(g)+H2(g)△H=﹣41.3kJmol﹣1
①总反应热化学方程式:3H2(g)+3CO(g)CH3OCH3(g)+CO2(g)△H=;
②Y(Y1、Y2),X可分别代表压强或温度.如图2表示Y一定时,总反应中CO的平衡转化率随X的变化关系.判断Y1、Y2的大小关系,并简述理由: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 用如图装置电解精炼镁
用如图装置电解精炼镁
B. 用如图装置验证试管中铁丝发生析氢腐蚀
用如图装置验证试管中铁丝发生析氢腐蚀
C. 如图装置中Mg作负极,Al作正极
如图装置中Mg作负极,Al作正极
D. 用如图装置对二次电池进行充电
用如图装置对二次电池进行充电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命.
(1)抗腐蚀处理前,生产中常用盐酸来除铁锈.现将一表面生锈的铁件放入盐酸中,除去铁锈的化学反应的离子方程式为: .
(2)利用如图装置,可以模拟铁的电化学防护. ①若X为碳棒,为减缓铁件的腐蚀,开关K应置于处.
②若X为锌,开关K置于M处,该电化学防护法称为 .
(3)图中若X为粗铜,容器中海水替换为硫酸铜溶液,开关K置于N处,一段时间后,当铁件质量增加3.2g时,转移的电子数为NA . 铁件表面镀铜可有效防止铁被腐蚀,如果铁件部分未镀上铜,或镀层破损,镀铜铁比镀锌铁反而更易被腐蚀,请简要说明原因: . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)已知H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3kJmol﹣1 . 若向三份等体积、等物质的量浓度的NaOH溶液中分别加入醋酸、浓硫酸、稀硝酸至恰好完全反应,并将上述过程中放出的热量分别记为Q1kJ、Q2kJ、Q3kJ.则三者的由小到大关系是(用Q1、Q2、Q3表示).
(2)如图所示A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其目的是; 若实验中不加盖泡沫塑料板,则求得的中和热数值(填偏大、偏小、无影响) 
(3)实验室用50mL 0.50molL﹣1盐酸、50mL 0.55molL﹣1NaOH溶液利用如图装置,进行测定中和热的实验.假设盐酸和氢氧化钠溶液的密度都是1g/cm3 , 又知中和后生成溶液的比热容c=4.18J/(g℃).为了计算中和热,实验时还需测量的数据有(填序号) .
A.反应前盐酸的温度
B.反应前盐酸的质量
C.反应前氢氧化钠溶液的温度
D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.4 |
2 | 20.2 | 20.4 | 23.6 |
3 | 20.5 | 20.6 | 23.8 |
依据该学生的实验数据计算,该实验测得的中和热△H为 . (保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物X(C7H8O)与另一有机化合物Y发生如下反应生成化合物Z(C11H14O2):![]()
(1)X是下列化合物之一,已知X不能与FeCl3溶液发生显色反应,则X是(填字母)。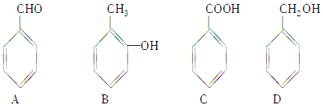
(2)Y的分子式是 , 可能的结构简式是和。
(3)Y有多种同分异构体,其中一种同分异构体E发生银镜反应后,其产物经酸化可得到F(C4H8O3)。F可发生如下反应:![]()
该反应的类型是 , E的结构简式是。
(4)若Y与E具有相同的碳链,则Z的结构简式为?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体内有20多种微量元素,它们质量总和不到体里的千万分之,但是对人的健康却起着重要作用,下列各组元素全部是微量元素的是( )
A. K、CL、S、OB. Mn、Fe、Zn、Cu
C. N、H、P、CD. K、Ca、C、Mg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com