
【题目】已知烃A在标准状况下的密度为1.16g·Lˉ1,B能发生银镜反应。以A和CO为原料制取有机物E的流程如下:

请回答:
(1)反应①的反应类型是__________。
(2)关于物质D(CH2=CHCOOH)化学性质的说法正确的是__________。
A.物质D含有一种官能团 B.物质D与Na2CO3溶液反应能产生气泡
C.物质D不能使酸性KMnO4溶液褪色 D.常温常压时,物质D呈气态
(3)②的反应机理与制取乙酸乙酯相似,写出其化学方程式________________。
【答案】 加成或还原 B CH2=CHCOOH + HOC2H5![]() CH2=CHCOOC2H5+ H2O
CH2=CHCOOC2H5+ H2O
【解析】已知烃A在标准状况下的密度为1.16g·Lˉ1,其摩尔质量为22.4L/mol×1.16g/L=26g/mol,则此烃为C2H2,乙炔与水加成生成的B能发生银镜反应,则B为乙醛;乙醛与氢气发生加成反应生成的C为乙醇,乙醇与丙烯酸发生酯化反应生成丙烯酸乙酯;
(1)反应①为乙醛与氢气发生的加成反应,反应类型是加成或还原反应;
(2)A.CH2=CHCOOH分子内含有碳碳双键和羧基二种官能团,故A错误;B.CH2=CHCOOH与Na2CO3溶液反应生成CO2,故B正确;C.CH2=CHCOOH含有碳碳双键,能使酸性KMnO4溶液褪色,故C错误;D.常温常压时,CH2=CHCOOH呈液态,故D错误;答案为B;
(3)乙醇与丙烯酸发生酯化反应的化学方程式为CH2=CHCOOH + HOC2H5![]() CH2=CHCOOC2H5 + H2O。
CH2=CHCOOC2H5 + H2O。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】下列反应中,浓硫酸既表现强氧化性,又表现酸性的是( )
A. 浓硫酸与氧化亚铁反应 B. 浓硫酸与木炭粉反应
C. 浓硫酸与氧化铜反应 D. 浓硫酸与氯化钠固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明代宋应星著的《天工开物》中有关于“火法”冶炼锌的工艺记载:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,……,冷淀,毁罐取出,……,即倭铅也。”下列说法不正确的是(注:炉甘石的主要成分为碳酸锌)
A.该冶炼锌的反应属于置换反应
B.煤炭中起作用的主要成分是C
C.冶炼Zn的反应方程式为:ZnCO3+2C![]() Zn+3CO↑
Zn+3CO↑
D.倭铅是指金属锌和铅的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列三组物质中,均有一种物质的类别与其它三种不同
A.MgO、Na2O、CO2、CuO B.HCl、H2O、H2SO4、HNO3 C.NaOH、Na2CO3、KOH、Cu(OH)2
(1) 三种物质依次是(填化学式):A______________;B_______________;C________________。
(2) 这三种物质相互作用可生成一种新物质NaHCO3,该反应_______(“是”或“不是”)氧化还原反应。
(3) 写出物质C与足量稀硫酸反应的离子方程式:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用98%浓硫酸(密度1.84g/cm3)配制浓度为0.5mol/L稀硫酸480 mL。
(1) 选用的主要仪器有:量筒、烧杯、玻璃棒、___________、___________。
(2) 应量取浓硫酸的体积为__________mL,现有①10mL②20mL③50mL三种规格的量筒,则所需选用的量筒是___________(填代号)。
(3) 配制时,一般可分为以下几个步骤: ①量取 ②计算 ③稀释 ④摇匀(上下颠倒) ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却,其正确的操作顺序是______________________________。
(4) 在配制过程中,其他操作都准确,下列操作能引起所配溶液浓度偏低的有_____.
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②定容时,加蒸馏水超过标线,又用胶头滴管吸出
③未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
④转移前,容量瓶中含有少量蒸馏水
⑤定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑥定容时,俯视标线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.含有非极性键的分子一定是非极性分子B.非极性分子中一定含有非极性键
C.由极性键形成的双原子分子一定是极性分子D.键的极性决定了分子的极性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
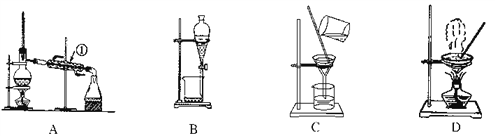
(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置________。
(2)从油水混合物中分离出植物油,选择装置________,该分离方法的名称为________。
(3)装置A中①的名称是________,进水的方向是从________口进水。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用质量分数为98%、密度为1.84g·cm-3的浓硫酸来配制500mL 0.2mol/L的稀硫酸。可供选择的仪器:①玻璃棒,②烧瓶,③烧杯,④胶头滴管,⑤量筒,⑥容量瓶,⑦托盘天平,⑧药匙。
请回答下列问题:
(1)上述仪器中,在配制稀硫酸时用不到的仪器有______(填代号)。
(2)配制溶液时,一般可以分为以下几个步骤:
①量取②计算③稀释④摇匀⑤移液⑥洗涤⑦定容⑧冷却⑨初步振荡⑩装瓶贴签
其正确的操作顺序为②①③______⑥_____④⑩(填序号)。
(3)经计算,需浓硫酸的体积为______mL。现有①10mL、②50mL、③100mL三种规格的量筒,应选用的量筒是_______(填代号)。
(4)在配制过程中,其他操作都准确,下列操作中错误且能使所配溶液浓度偏高的有____ (填代号)
①洗涤量取浓硫酸后的量筒,并将洗涤液转入容量瓶中
②未等稀释后的硫酸溶液冷却至室温就转入容量瓶内
③将浓硫酸直接倒入烧杯,再向烧杯中注入蒸馏水来稀释浓硫酸
④定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
⑦定容时俯视刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com