
【题目】常温下KMnO4氧化浓HCl的反应方程式如下:
2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
(1)用“双线桥法”标明反应中电子转移的方向和数目.
(2)又已知MnO2+4HCl(浓) ![]() MnCl2+Cl2+2H2O,结合以上反应原理,则MnO2、KMnO4、Cl2的氧化性由强到弱的顺序是: .
MnCl2+Cl2+2H2O,结合以上反应原理,则MnO2、KMnO4、Cl2的氧化性由强到弱的顺序是: .
(3)若有63.2g高锰酸钾参加反应,则被氧化的HCl的物质的量为mol,产生的Cl2在标准状况下的体积为L.
【答案】
(1)
(2)KMnO4>MnO2>Cl2
(3)2;22.4
【解析】解:(1)该反应中Mn元素化合价由+7价变为+2价、Cl元素化合价由﹣1价变为0价,其得失电子最小公倍数是10,其电子转移的方向和数目为 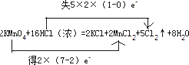 ,所以答案是:
,所以答案是:  ;(2)由氧化剂的氧化性大于氧化产物的氧化性可知,氧化性为KMnO4>Cl2 , MnO2>Cl2 , 结合反应条件可知,与二氧化锰反应需要加热,则氧化性为KMnO4>MnO2>Cl2 ,
;(2)由氧化剂的氧化性大于氧化产物的氧化性可知,氧化性为KMnO4>Cl2 , MnO2>Cl2 , 结合反应条件可知,与二氧化锰反应需要加热,则氧化性为KMnO4>MnO2>Cl2 ,
所以答案是:KMnO4>MnO2>Cl2;(3)有63.2g高锰酸钾参加反应,n(KMnO4)= ![]() =0.4mol,0.4mol高锰酸钾参加反应被还原的HCl的物质的量=
=0.4mol,0.4mol高锰酸钾参加反应被还原的HCl的物质的量= ![]() =2mol,转移电子的物质的量为0.4mol×(7﹣2)=2mol,生成Cl2在标准状况下的体积为1mol×22.4L/mol=22.4L,
=2mol,转移电子的物质的量为0.4mol×(7﹣2)=2mol,生成Cl2在标准状况下的体积为1mol×22.4L/mol=22.4L,
所以答案是:2;22.4.


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】燃料电池是一种将化学反应产生的能量直接转化为电能的装置,你认为下列燃料电池比较适合宇宙飞船上使用的是( )
A. CH4—O2燃料电池 B. C2H5OH—O2燃料电池
C. H2—O2燃料电池 D. CO—O2燃料电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。试回答:

(1)c极的电极反应式为_________。
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,电解进行一段时间后,你能观察到的现象是:___________, 电解进行一段时间后,罩在c极上的试管中也收集到了气体,此时c极上的电极反应式为_____________。
(3)当d极上收集到44.8mL气体(标准状况)时停止电解,a极上放出了____moL气体,此时若b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为_________。此时A池中溶液pH为_________。(假设电解前后A池溶液体积无变化,数据化成最简形式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的水溶液导电性最强的是
A. 10 mL 0.50 mol/LH2SO4溶液 B. 20 mL 0.50 mol/L KNO3溶液
C. 30 mL 0.50 mol/L氨水溶液 D. 40 mL 1.0 mol/L蔗糖溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于取代反应的是
A.乙烯水化法制乙醇B.苯与浓硝酸、浓硫酸混合共热制取硝基苯
C.甲苯使酸性高锰酸钾溶液褪色D.在一定条件下苯与氢气反应制取环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A.除去苯中含有的少量苯酚,可在混合物中加入足量NaOH后分液
B.戊烷(C5H12)有两种同分异构体
C.乙烯、聚氯乙烯和苯分子均含有碳碳双键
D.乙烯、聚乙烯、苯均能使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度、容积相同的3个密闭容器中按不同方式投入反应物,保持恒温恒容,测得反应达到平衡时的有关数据如下(已知:N2(g)+3H2(g)![]() 2NH3(g) ΔH=92.4kJ/mol)
2NH3(g) ΔH=92.4kJ/mol)
容 器 | 甲 | 乙 | 丙 |
反应物投入量 | 1mol N2 3H2 mol | 2mol NH3 | 2mol N2 6molH2 |
NH3浓度(mol·L-1) | C1 | C2 | C3 |
反应的能量变化 | 放出a KJ | 吸收b KJ | 放出cKJ |
体系压强(Pa) | P1 | P2 | P3 |
反应物转化率 | α1 | α2 | α3 |
下列说法正确的是( )
A. C1+C2=C3 B. α2+α3>1 C. P1+P2<P3 D. a=b<92.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国有广阔的海岸线,建设海峡经济区,海水的综合利用大有可为,下图所示为海水综合利用部分流程,有关说法正确的是( )

A. 上述工艺流程中涉及到化合、分解、复分解和置换反应
B. ①只发生了化学变化,②是工业上用电解熔融NaCl制备Cl2
C. ③④涉及的反应均为氧化还原反应,⑤只需要蒸馏即可得到单质Br2
D. ④中反应的离子方程式为SO2+Br2+2H2O===4H++SO42-+2Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某市售“84消毒液”瓶体部分标签如下图所示,该“84 消毒液”通常稀释100 倍(体积之比)后使用. 请回答下列问题: 
(1)该“84 消毒液”的物质的量浓度约为mol/L.( 保留小数点后 1 位)
(2)该同学参阅此“84 消毒液”的配方,欲用NaClO固体配制480mL 与市售物质的量浓度相同的“84 消毒液”,下列说法中正确的是( 填序号).
A.如下图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0g
(3)“84 消毒液”与稀硫酸混合使用可增强其消毒能力,某消毒小组人员用 98%( 密度为1.84g/cm3)的浓硫酸配制 500mL 2.3mol/L 的稀硫酸用于增强“84 消毒液”的消毒能力.
①需用浓硫酸的体积为mL.
②取用任意体积的浓硫酸时,下列物理量中不随所取体积的多少而变化的是
A.溶液中H2SO4的物质的量 B.溶液的浓度
C.溶液的质量 D.溶液的密度
③对浓硫酸稀释过程中遇到下列情况,使所配制的硫酸浓度大于2.3mol/L有
A.未经冷却趁热将溶液注入容量瓶中
B.摇匀后发现液面低于刻度线,再加水至刻度线
C.容量瓶中原有少量蒸馏水
D.定容时俯视观察液面.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com