
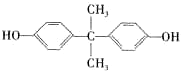
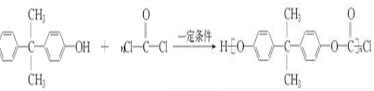
 )可用于制造多种高分子材料.现有如下转化关系.
)可用于制造多种高分子材料.现有如下转化关系.

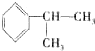 可以得到制取双酚A的原料,该有机物含苯环的同分异构体还有
可以得到制取双酚A的原料,该有机物含苯环的同分异构体还有| 60×60% |
| 12 |
| 60×60% |
| 12 |
| 浓硫酸 |
| △ |
| 浓硫酸 |
| △ |
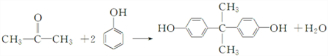 ,故答案为:
,故答案为: ;
; 可以得到制取双酚A的原料,该有机物含苯环的同分异构体中,如果含有一个正丙基、一个异丙基的各有一种,含有一个甲基和一个乙基的有邻间对3种,含有3个甲基的有3种,所以一共有8种,则还有7种,
可以得到制取双酚A的原料,该有机物含苯环的同分异构体中,如果含有一个正丙基、一个异丙基的各有一种,含有一个甲基和一个乙基的有邻间对3种,含有3个甲基的有3种,所以一共有8种,则还有7种,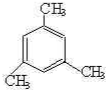 ,故答案为:7;
,故答案为:7; ,
, ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:
| A、标准状况下,22.4L H2O含有的分子数为 NA |
| B、常温常压下,1.42g Na2SO4含有的Na+离子数为0.02 NA |
| C、通常状况下,NA 个CO2分子占有的体积为22.4L |
| D、物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 取适量固体与试管中,加适量蒸馏水使其溶解, |
| 实验一:取黄豆大小的Na与冷水反应;取表面积比Na大的、刚打磨过的Mg条与热水反应,观察反应现象; | 现象:Na与水反应比Mg与水反应剧烈; 结论:金属性:Na>Mg; |
| 实验二: | 现象: 结论: |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
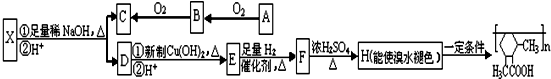
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将饱和氯水滴到淀粉碘化钾试纸上,如果试纸先变蓝后变白,说明氯水具有漂白性 |
| B、将SO2通入含HClO的溶液中,生成H2SO4说明HClO酸性比H2SO4强 |
| C、铁钉放在浓硝酸中浸泡后,在用蒸馏水冲洗,然后放入CuSO4溶液中不反应,说明铁钉表面形成了一层致密稳定的氧化铜 |
| D、FeCl3溶液可与腐蚀线路板上的Cu,说明Fe的金属活性大于Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
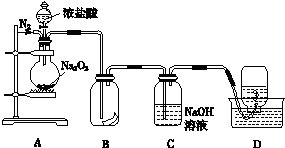
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用10mL量筒量取7.8mL浓H2SO4 |
| B、用碱式滴定管量取18.20mLKMnO4溶液 |
| C、酸碱中和滴定时,滴定管和锥形瓶需分别用标准液和待测液润洗 |
| D、读取标准液读数时,若滴定前仰视,滴定后俯视,会导致测定结果偏低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com