
����Ŀ����ѧ�ϳ���AG��ʾ��Һ�е�lg![]() ��25��ʱ����0.100molL-1��NaOH��Һ�ζ�20.00mL 0.100molL-1��HNO2��Һ��AG������NaOH��Һ�������V���Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��
��25��ʱ����0.100molL-1��NaOH��Һ�ζ�20.00mL 0.100molL-1��HNO2��Һ��AG������NaOH��Һ�������V���Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� ��
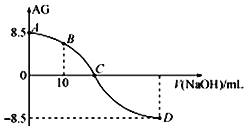
A. D����Һ��pH=11.25
B. C��֮ǰ��Һ�Լ��ԣ�C��֮����Һ������
C. C��ʱ������NaOH��Һ�����Ϊ20mL
D. 25��ʱ��HNO2�ĵ��볣��Ka=1.0��10-5.5
���𰸡�A
��������
A��D��AG= -8.5����lg![]() = -8.5��
= -8.5��![]() =10-8.5������ˮ�����ӻ����ó�c(H+)=10-11.25mol��L-1��pH=11.25����A��ȷ��
=10-8.5������ˮ�����ӻ����ó�c(H+)=10-11.25mol��L-1��pH=11.25����A��ȷ��
B��A��![]() =108.5��˵��c(H+)>c(OH-)����Һ�����ԣ���C��֮ǰ��Һ�����ԣ�
=108.5��˵��c(H+)>c(OH-)����Һ�����ԣ���C��֮ǰ��Һ�����ԣ�![]() =100��c(H+)=c(OH-)����Һ�����ԣ�C��֮����Һ�����ԣ���B����
=100��c(H+)=c(OH-)����Һ�����ԣ�C��֮����Һ�����ԣ���B����
C��HNO2Ϊ���ᣬ������NaOH��Һ�����Ϊ20mLʱ��ǡ����ȫ��Ӧ������ΪNaNO2����Һ�Լ��ԣ����C������NaOH�����С��20mL����C����
D��A�� ![]() =108.5������ˮ�����ӻ����ó�c2(H+)=10-5.5mol��L-1��HNO2
=108.5������ˮ�����ӻ����ó�c2(H+)=10-5.5mol��L-1��HNO2![]() H+��NO2-��Ka=
H+��NO2-��Ka=![]() =
=![]() =
=![]() =10-4.5����D����
=10-4.5����D����
��ѡA��


 һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⻯�ƿ�����������ܼ������Ʊ��⻯���ԭ�ϡ���ѧʵ��С����NaOH�����ʵ��ˮ����(N2H4��H2O)Ϊԭ���Ʊ��⻯�ơ�
��֪����ˮ����(N2H4��H2O)�ķе�118�棬100�濪ʼ�ֽ⣻����ǿ��ԭ�ԡ���I����IO3���ڼ��������¹��棬���������·�Ӧ����I2����ѧʵ��С������ͼ��ʾװ���Ʊ��⻯�ƣ�ʵ�鲽�����£�
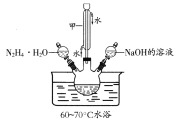
��.�Ʊ�ˮ���£��ã�NaC1O����NH3�Ƶ�ˮ���£�����������Һװ������װ������Һ©����
��.��������ƿ�м���һ�������ʵ⣬���Ҳ��Һ©����������������NaOH��Һ������60��70��ˮԡ����ַ�Ӧ�õ�NaI��NaIO3�Ļ����Һ��
��.������Һ©����������ˮ������Һ��������ƿ��������60��70��ˮԡ����Ӧ��֡�
��.���������Һ�м�����������̿����а�Сʱ�����ˣ�����Һ�з������Ʒ��
�ش��������⣺
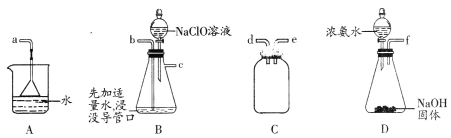
(1)������������________________��
(2)����ͼ��ʾװ���Ʊ�ˮ���£�
�������Ľӿ��������ӵĺ���˳����________________________(����ĸ��ʾ)��
��ʵ������У���Ҫ�����μ�NaC1O��Һ����Ҫԭ����____________________________��
(3)��������¶ȱ�����70�����µ�ԭ����_______________________________________��
(4)������з������Ʒ�IJ�����_____________________��ϴ�ӡ����
(5)��Ʒ������鲽���������Һ�к���NaIO3��__________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������£����и�������һ���ܴ���������ǣ� ��
A.����ʯ����Һ�Ժ�ɫ����Һ��K+��Mg2+��AlO2��SO32
B.1.0mol��L1��KNO3��Һ��H+��Fe2+��Cl��SO42
C.��![]() ��1��1012����Һ�У�NH4+��Fe2+��Cl����NO3
��1��1012����Һ�У�NH4+��Fe2+��Cl����NO3
D.ͨ������CO2����Һ��Ca2+��Cl��K+��Na+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮD2O��ɵ�ˮ��D2O�����ӻ�Ϊ1.6��10-15������pHһ������涨pD= -lg{c(D+)}�����й���pD����������ȷ���ǣ� ��
A. D2O�����ԣ�pD=7
B. ��0.01mol NaOD��D2O��Һ1L��pD=12
C. ��D2O�ܽ�0.1mol DCl��1L��Һ��pD=2
D. ��100mL 0.25mol/L DCl��Һ�м���50mL 0.2mol/L��NaOD��D2O��Һ��pD=1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������º�̼����H2CO3��HCO3����CO32��������CO2��NaOH��Һ��Ӧ�����Һ�У����ǵ����ʵ�����������ҺpH�Ĺ�ϵ��ͼ��ʾ������˵��������ǣ� ��
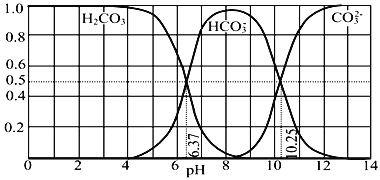
A. Ϊ��þ����ܴ���NaHCO3���˿�����Һ��pHΪ7��9֮��
B. pH=10.25ʱ��c(Na+)=c(CO32��)+c(HCO3��)
C. ����ͼ�����ݣ����Լ���õ�H2CO3��һ�������ƽ�ⳣ��K1(H2CO3)=10��6.37
D. ����0.1mol NaOH��Ӧ�����õ�1L��Һ��pH=10ʱ����Һ�д������¹�ϵ�� c(Na+)��c(HCO3��)��c(CO32��)��c(OH��)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤����������ֵ������˵����ȷ���ǣ� ��
A.7.2g CaO2������������������Ϊ0.3NA
B.�ܱ�������2 mol NO��1mol O2��ַ�Ӧ������ķ�����ĿΪ2NA
C.��һ�������£�6.4gͭ���������Ӧ��ת�Ƶĵ�����ĿΪ0.2NA
D.10g��������Ϊ46%���Ҵ���Һ��O-H����ĿΪ0.7NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ĸ���ͬ�����У���ͬ�����½��кϳɰ���Ӧ����������ͬʱ���ڲⶨ�Ľ���ж����ɰ�������������( )
A. v(N2)=0.1mol��L-1��s-1 B. v(H2)=0.1mol��L-1��min-1
C. v(NH3)=0.15mol��L-1��min-1 D. v(H2)=0.3mol��L-1��min-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʽ�Ȼ�ͭ��CuaClb(OH)c��xH2O����һ����Ҫ����ɱ�����������ͨ�����²����Ʊ�������1����ͭ�ۼ���ϡ�����У�������ͨ������Ӧ����CuCl2����֪Fe3+�Ը÷�Ӧ�д����ã����ԭ������ͼ��ʾ������2�����Ƶõ�CuCl2��Һ�У�����ʯ�����ַ�Ӧ���Ʊ���ʽ�Ȼ�ͭ��
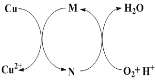
�����й�˵����ȷ����
A. a��b��c ֮��Ĺ�ϵʽΪ��a=b+c
B. ͼ��M��N�ֱ�ΪFe2+��Fe3+
C. ����1��ַ�Ӧ��������CuO��Ϊ�˳�ȥFe3+
D. ���Ʊ�1 mol��CuCl2������������11.2 LO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ƻ������ǽ�ú�е���Ԫ����CaSO4����ʽ�̶�����ú̿ȼ�չ����в�����CO�ֻᷢ����ӦI�ͷ�ӦII����������Ч�ʽ��͡�ij�¶��£���ӦI������(v1)���ڷ�ӦII������(v2)�������з�Ӧ���������仯ʾ��ͼ��ȷ����
��ӦI��CaSO4(s)+CO(g) ![]() CaO(s)+SO2(g)+CO2(g) ��H1=+218.4kJ��mol-1
CaO(s)+SO2(g)+CO2(g) ��H1=+218.4kJ��mol-1
��ӦII��CaSO4(s)+4CO(g) ![]() CaS(s)+4CO2(g) ��H2=��175.6kJ��mol-1
CaS(s)+4CO2(g) ��H2=��175.6kJ��mol-1

A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com