
����ѡ������ȷ����
A. 1L0.5mol��L��1ϡ������1L1mol��L��1����������Һ��Ӧ�ų�57.3kJ��������
H2SO4(aq) +2NaOH(aq) = Na2SO4(aq)+2H2O(1)���� H = ��57.3 kJ�� mol-1
B. ij�����ʽ��NaHYˮ��Һ�Լ��ԣ���H2Y2H++Y2��
C. ������Һ�Լ��Ե�ԭ�������ӷ���ʽ�ɱ�ʾΪ��CO32��+2H2OH2CO3+2OH��
D���Զ��Ե缫���KCl��Һ�����ӷ���ʽΪ��2Cl��+2H2O H2��+2OH��+Cl2��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
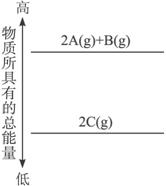
A.2A(g)+B(g)====2C(g)����H��0
B.2A(g)+B(g) ====2C(g)����H��0
C.2A+B====2C����H��0
D.2C====2A+B����H��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

A![]()
![]()
C![]()
![]() 2A+B����H��0
2A+B����H��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013���㽭ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��16�֣�þ����������������й㷺��;����ش��������⣺
��1��дþ��������Ӧ����ĵ���ʽ
��2����ͼ�ǽ���þ��±�ط�Ӧ�������仯ͼ����Ӧ��Ͳ����Ϊ298Kʱ���ȶ�״̬����������ѡ������ȷ����
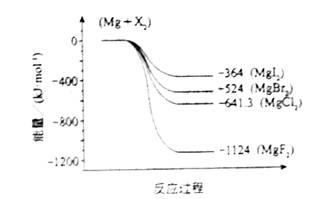
A MgI2��Mg2+��I-�����������MgF2��Mg2+��F-���������
B Mg��X2�ķ�Ӧ�Ƿ��ȷ�Ӧ
C MgBr2��Cl2��Ӧ�ġ�H��0
D ����������ȶ���˳��ΪMgI2��MgBr2��MgCl2��MgF2
��3����298K��100Kpaʱ����1Lˮ�п��ܽ�0.09mol������ʵ��������ˮ��Cl2Լ������֮һ��ˮ��Ӧ����ش��������⣺
�� �÷�Ӧ�����ӷ���ʽΪ ��ƽ�ⳣ������ʽΪ
��������ƽ����ϵ�м�������NaCl���壬ƽ�⽫ ��������ƶ������������ƶ����������ƶ�����������������ѹǿ���������ܽ�Ƚ� ��������ˮ��Ӧ��ƽ�ⳣ����
����������С���������䡱����
����֪��
H2CO3  HCO3�� + H+
Ka1(H2CO3) = 4.45��10��7
HCO3�� + H+
Ka1(H2CO3) = 4.45��10��7
HCO3�� CO32�� + H+
Ka2(H2CO3) = 5.61��10��11
CO32�� + H+
Ka2(H2CO3) = 5.61��10��11
HClO  H+ + ClO��
Ka(HClO) = 2.95��10��8
H+ + ClO��
Ka(HClO) = 2.95��10��8
����������̼��ʹ�����ĵ���ƽ�ⳣ����д����������������������Ӧ�����ӷ���ʽ��
������������ͨ�뵽������̼������Һ��____________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ��ɽ��ʡ������ѧ�ڵ�����������⻯ѧ�Ծ� ���ͣ�ѡ����
����ѡ������ȷ����
A. 1L0.5mol��L��1ϡ������1L1mol��L��1����������Һ��Ӧ�ų�57.3kJ��������
H2SO4(aq) +2NaOH(aq) = Na2SO4(aq) +2H2O(1)���� H = ��57.3 kJ�� mol-1
B. ij�����ʽ��NaHYˮ��Һ�Լ��ԣ���H2Y 2H++Y2��
2H++Y2��
C. ������Һ�Լ��Ե�ԭ�������ӷ���ʽ�ɱ�ʾΪ��CO32��+2H2O H2CO3+2OH��
H2CO3+2OH��
D���Զ��Ե缫���KCl��Һ�����ӷ���ʽΪ��2Cl��+2H2O  H2��+2OH��+Cl2��
H2��+2OH��+Cl2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�캣��ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ�ѡ����
��������������仯ͼ���ж�����ѡ������ȷ����

A. 2A(g)+B(g) === 2C(g) ��H<0 B. 2A(g)+B(g) === 2C(g) ��H>0
C. 2A+B=== 2C ��H<0 D. 2C=== 2A+B ��H<0
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com