
【题目】2016 年国际纯粹与应用化学联合会命名第 117 号元素为 Ts(中文名,钿)。关于 294Ts 的叙述错误的是
A. 原子序数 117B. 中子数 177C. 核外电子数 117D. 相对原子质量 294
 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:
【题目】已知90℃时,Kw =1.0×10-12,在90℃将pH=9的NaOH溶液与pH=4的硫酸溶液混合,若所得溶液pH=7,则NaOH溶液与硫酸溶液的体积比为
A.1:9B.9:1C.10:1D.1:10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇可以与水蒸气反应生成氢气,反应方程式如下:CH3OH(g)+H2O(g)CO2(g)+3H2(g)△H>0
(1)一定条件下,向体积为2L的恒容密闭容器中充入1mol CH3OH(g)和3mol H2O(g),20s后,测得混合气体的压强是反应前的1.2倍,则用甲醇表示该反应的速率为 .
(2)判断(1)中可逆反应达到平衡状态的依据是(填序号) . ①v正(CH3OH)=v正(CO2)
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④CH3OH、H2O、CO2、H2的浓度都不再发生变化
(3)图中P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入1mol CH3OH(g)和2mol H2O(g),向B容器中充入1.2mol CH3OH(g)和2.4mol H2O(g),两容器分别发生上述反应.已知起始时容器A和B的体积均为a L.试回答: 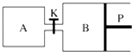
①反应达到平衡时容器B的体积为1.5a L,容器B中CH3OH的转化率为;A、B两容器中H2O(g)的体积百分含量的大小关系为:BA(填“>”“<”或“=”).
②若打开K,一段时间后重新达到平衡,容器B的体积为L(连通管中气体体积忽略不计,且不考虑温度的影响).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究实验富制氯气过程中反应物与生成氯气之间量的关系.设计了如图所示的装置 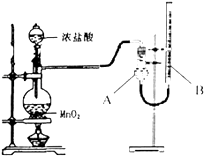
(1)装置A的名称是
(2)该实验装置检查气密性的方法是
(3)如果将过二氧化锰与20mL12mol/L的盐酸混合加热,充分反应后收集到的氯气少于0.06mol,其可能原因有
a.加热使浓盐酸放出大量HCl
b.盐酸变稀后不发生该反应
c.烧瓶中残留有氯气
d.装置B中液面高于A.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素 R 有某种同位素的氯化物 RClX,该氯化物中 R 微粒核内中子数为 Y,核外电子数为 Z,该同位素的符号为
A. YZRB. Y+X+ZX+ZRC. YZ+XRD. Y+XZR
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以苯甲醛为原料,通过Cannizzaro反应来制备苯甲醇和苯甲酸,反应式为:
主反应:
副反应:![]()
主要物料的物理常数如表:
名称 | 分子量 | 性状 | 相对密度 | 沸点 | 溶解度 | |
水 | 乙醚 | |||||
苯甲醛 | 106 | 无色液体 | 1.04 | 179 | 微溶 | 易溶 |
苯甲酸 | 122 | 无色晶体 | 1.27 | 249 | 0.21g | 66g |
苯甲醇 | 108 | 无色液体 | 1.04 | 205 | 微溶 | 易溶 |
乙醚 | 74 | 无色液体. | 0.71 | 35 | 不溶 | ﹣﹣ |
实验步骤: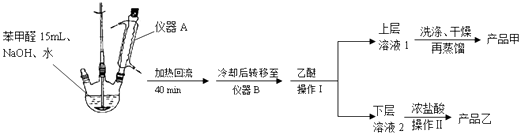
(1)仪器A的作用是 .
(2)蒸馏操作时温度应该控制在左右.获得产品乙时进行的操作Ⅱ的名称是 .
(3)①上层溶液1中除乙醚外主要有机杂质是、 .
洗涤时先后用到了饱和NaHSO3溶液、10%的NaHCO3溶液和水.
②洗涤操作在中进行.
a.烧杯 b.布氏漏斗 c.烧瓶 d.分液漏斗
③加入10%的NaHCO3溶液至(填现象)时说明杂质已被除尽.
(4)若产品甲的质量为5.40g,则产品甲的产率是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲同学进行了FeCl2溶液的配制、浓度的测定以及Fe2+还原性的实验,并针对异常现象进行探究.
(1)步骤一:制取FeCl2 甲同学准备用两种方案制取.
方案1:按如图装置用H2还原无水FeCl3制取.
E中盛放的试剂是;D中反应的化学方程式为 . 此方案有个明显的缺陷是 .
方案2:由0.1molL﹣1 FeCl3溶液制取FeCl2溶液,你认为其操作应该是 .
(2)步骤二:测定方案2所配FeCl2溶液的物质的量浓度.用重铬酸钾法(一种氧化还原滴定法)可达到目的.若需配制浓度为0.01000molL﹣1的K2Cr2O7标准溶液480mL,实验中用到的玻璃仪器有量筒、玻璃棒、烧杯,还缺少 ,
本实验滴定过程中操作滴定管的图示正确的是(填编号).
下列错误的操作使测定的FeCl2溶液浓度偏小的是
A.若在配制K2Cr2O7标准溶液定容时采取俯视姿势
B.若滴定操作中,如果滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失.
C.锥形瓶洗净后未干燥
(3)步骤三:向2mL FeCl2溶液中滴加2滴0.1molL﹣1KSCN溶液,无现象;再滴加5滴5% H2O2溶液(物质的量浓度约为1.5molL﹣1、pH约为5),观察到溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2).
甲同学探究“步骤三”中溶液褪色的原因:
实验I.取褪色后溶液两份,一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色;
实验II.取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀,并测得生成了两种可直接排放到空气中的气体.
实验III.向2mL 0.1molL﹣1 FeCl3溶液中滴加2滴0.1molL﹣1KSCN溶液,变红,通入O2 , 无明显变化.
①实验I说明溶液红色褪去是因为SCN﹣发生了反应而不是Fe3+发生反应.
②实验III的目的是 .
得出结论:溶液褪色的原因是酸性条件下H2O2将SCN﹣氧化成SO42﹣和相关气体.写出该反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气化和液化是使煤变成清洁能源的有效途径。煤的气化的主要反应是:C+H2O(g) ![]() CO+H2 , CO和H2的混合气体是合成多种有机物的原料气,研究由CO、H2合成有机物的化学称为一碳化学。下图是合成某些物质的路线图:
CO+H2 , CO和H2的混合气体是合成多种有机物的原料气,研究由CO、H2合成有机物的化学称为一碳化学。下图是合成某些物质的路线图: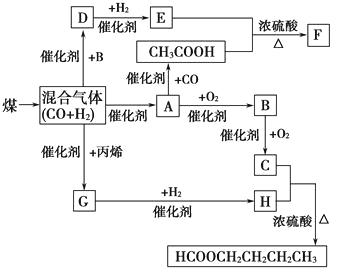
其中,D易溶于水,且与CH3COOH互为同分异构体,F分子中的碳原子数是D中的3倍,H经催化氧化可得到G。请回答下列问题:
(1)写出下列物质的结构简式:A: , H: , 指出A和H的关系。
(2)利用合成气(H2+CO)生产汽油、甲醇和氨等已经实现了工业化,合成气也可合成醛、酸、酯等多种产物,下列表述正确的是。
①以合成气为原料的反应都是化合反应
②改变合成气中CO与H2的体积比,可得到不同的产物
③合成气的转化反应需在适当的温度和压强下通过催化完成
④从合成气出发生成气态烃或醇类有机物是实现“煤变油”的有效途径
⑤以合成气为原料的反应产物中不可能有烯烃或水
A.①②④
B.②③④
C.②④⑤
D.③④⑤
(3)写出下列反应的化学方程式:
①CH3COOH+E→F:。
②D与新制氢氧化铜悬浊液加热:。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com