
【题目】以苯甲醛为原料,通过Cannizzaro反应来制备苯甲醇和苯甲酸,反应式为:
主反应:
副反应:![]()
主要物料的物理常数如表:
名称 | 分子量 | 性状 | 相对密度 | 沸点 | 溶解度 | |
水 | 乙醚 | |||||
苯甲醛 | 106 | 无色液体 | 1.04 | 179 | 微溶 | 易溶 |
苯甲酸 | 122 | 无色晶体 | 1.27 | 249 | 0.21g | 66g |
苯甲醇 | 108 | 无色液体 | 1.04 | 205 | 微溶 | 易溶 |
乙醚 | 74 | 无色液体. | 0.71 | 35 | 不溶 | ﹣﹣ |
实验步骤: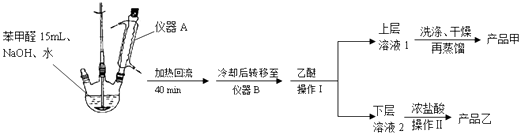
(1)仪器A的作用是 .
(2)蒸馏操作时温度应该控制在左右.获得产品乙时进行的操作Ⅱ的名称是 .
(3)①上层溶液1中除乙醚外主要有机杂质是、 .
洗涤时先后用到了饱和NaHSO3溶液、10%的NaHCO3溶液和水.
②洗涤操作在中进行.
a.烧杯 b.布氏漏斗 c.烧瓶 d.分液漏斗
③加入10%的NaHCO3溶液至(填现象)时说明杂质已被除尽.
(4)若产品甲的质量为5.40g,则产品甲的产率是 .
【答案】
(1)冷凝回流
(2)205℃;抽滤(过滤、减压过滤)
(3)苯甲醛;苯甲酸;d;无气泡生成
(4)67.9%
【解析】解:由流程结合题中信息可知,苯甲醛与NaOH反应生成白色糊状物为苯甲醇、苯甲酸钠的混合物,然后加水、乙醚萃取苯甲醇,则乙醚溶液中含苯甲醇,操作I为蒸馏,得到产品甲为苯甲醇;水溶液中含苯甲酸钠,加盐酸发生强酸制取弱酸的反应,生成苯甲酸,苯甲酸的溶解度小,则操作为过滤,则产品乙为苯甲酸,(1)由仪器结构特征,可知A为冷凝管,作用是冷凝回流,所以答案是:冷凝回流;(2)苯甲醛和氢氧化钠反应得到苯甲酸钠和苯甲醇,二者互溶,分离采用蒸馏法,苯甲醇的沸点是205℃,所以蒸馏操作时温度应该控制在205℃左右,苯甲酸钠可以和盐酸之间反应得到苯甲酸,获得产品乙苯甲酸时进行的操作Ⅱ的名称是 抽滤(过滤、减压过滤).所以答案是:205℃;抽滤(过滤、减压过滤);(3)①上层液中还含有未反应的苯甲醛、苯甲酸,苯甲酸、苯甲醛的沸点较低,易溶于有机物溶剂中,即上层溶液1中除乙醚外主要有机杂质是苯甲醛、苯甲酸,所以答案是:苯甲醛、苯甲酸;②苯甲醛、苯甲酸易溶解在有机溶剂中,洗涤操作在分液漏斗正确进行;
所以答案是:d;③加入10%的Na2CO3溶液除去生成的苯甲酸,加入10%的Na2CO3溶液除去生成的苯甲酸,没有气泡生成时说明杂质已被除尽,
所以答案是:无气泡生成;(4)15.0mL苯甲醛的质量为15.0mL×1.06g/mL,其物质的量为 ![]() mol≈0.15mol,122g、mol由方程式可知生成苯甲酸为
mol≈0.15mol,122g、mol由方程式可知生成苯甲酸为 ![]() =0.075mol,故苯甲醇的产率为
=0.075mol,故苯甲醇的产率为 ![]() ×100%=67.9%,
×100%=67.9%,
所以答案是:67.9%.


 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案科目:高中化学 来源: 题型:
【题目】参考下列①~③项回答问题:
①皂化值是使1g油脂皂化所需要的氢氧化钾的毫克数;
②碘值是使100g油脂加成时消耗单质碘的克数;
③各种油脂的皂化值、碘值列表如下:
花生油 | 亚麻仁油 | 牛油 | 黄油 | 硬化大豆油 | 大豆油 | |
皂化值 | 190 | 180 | 192 | 226 | 193 | 193 |
碘值 | 90 | 182 | 38 | 38 | 5 | 126 |
(1)单纯油(C17H33COO)3C3H5(相对分子质量884)形成的油,用氢氧化钾皂化时,皂化值为?
写出其反应方程式?
(2)在下列①~④的空格内填入适当的词句。
①亚麻仁油比花生油所含的脂肪酸多(填写“饱和”或“不饱和”);
②黄油比牛油所含的脂肪酸多(填写“低级”或“高级”);
③硬化大豆油的碘值小的原因是;
④不同油脂的皂化值越大,则油脂的平均相对分子质量;碘化值越高,则表明含越多。
(3)为使碘值为180的100g鱼油硬化,所需氢气的体积在标准状况下为多少升?
(4)用下列结构式所代表的酯,若皂化值为430,求n为多少?并完成下面反应方程式: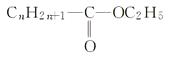 +KOH―→+
+KOH―→+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016 年国际纯粹与应用化学联合会命名第 117 号元素为 Ts(中文名,钿)。关于 294Ts 的叙述错误的是
A. 原子序数 117B. 中子数 177C. 核外电子数 117D. 相对原子质量 294
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】未来新能源的特点是资源丰富,在使用时对环境无污染或很少污染,且有些可以再生.下列属最有希望的新能源的是( )
①天然气 ②煤 ③核能 ④水电 ⑤太阳能 ⑥燃料电池 ⑦风能 ⑧氢能.
A.①②③④
B.⑤⑥⑦⑧
C.③④⑤⑥
D.除①②外
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.10mol·L-1NH3·H2O溶液中,加入少量NH4Cl晶体后,引起的变化是
A.NH3·H2O的电离程度减小
B.NH3·H2O的电离常数增大
C.溶液的导电能力不变
D.溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对水体污染物的处理方法中,不正确的是
A.含盐酸的酸性废水用中和法处理B.含Cu2+、Fe3+的废水用沉淀法处理
C.含有细菌的污水用臭氧杀菌D.含有重金属离子的废水用明矾处理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅单质及其化合物应用很广。请回答下列问题:
(1)制备硅半导体材料必须先得到高纯硅。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程示意图如下:![]()
①写出由纯SiHCl3制备高纯硅的化学反应方程式。
②整个制备过程必须严格控制无水、无氧。SiHCl3遇水剧烈反应生成H2SiO3、
HCl和另一种物质,写出配平的化学反应方程式;H2
还原SiHCl3过程中若混有O2 , 可能引起的后果是。
(2)下列有关硅材料的说法正确的是( )。
A.单质硅化学性质稳定,但可以被强碱溶液腐蚀
B.盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅
C.普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高
D.光导纤维的主要成分是SiO2
(3)硅酸钠水溶液俗称水玻璃。取少量硅酸钠溶液于试管中,逐滴加入盐酸,
振荡。写出实验现象并给予解释(用化学方程式说明)。
(4)在人体器官受到损伤时,需要使用一种新型无机非金属材料来植入体内,这种材料是________(填字母)。
A.高温结构陶瓷
B.生物陶瓷
C.导电陶瓷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学事实正确且能用元素周期律解释的是
①原子半径:Cl>P②沸点:HCl>H2S③还原性:S2->C1-④相同条件下电离程度:H2CO3>H2SiO3
A. ①④B. ③④C. ①D. ②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com