
【题目】元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
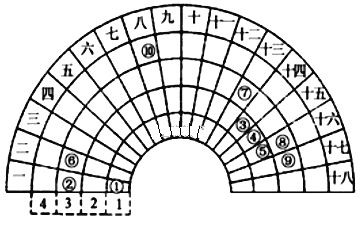
A. ⑥、⑧、⑨对应单核离子的半径依次增大
B. ⑤的三种核素的化学性质不相同
C. ④的最高价氧化物对应的水化物能与其氢化物反应,生成离子化合物
D. ⑧、⑨两种元素的气态氢化物及其最高价氧化物的水化物均为强酸
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】下列物质的分离或提纯,可选用蒸馏法的是
A. 除去石灰水中悬浮的碳酸钙颗粒
B. 除去氯化钠晶体中混有的碘单质
C. 分离汽油和煤油的混合物
D. 分离水和苯的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学活动小组设计以下装置进行不同的实验.其中a为用于鼓入空气的气囊,b为螺旋状铜丝,c中盛有冰水.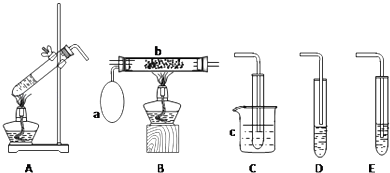
(1)若用A装置做乙醇与乙酸的酯化反应实验,则还需连接的装置是(填序号),该装置中应加入试剂 .
(2)该小组同学欲做乙醇氧化成乙醛的实验,则应选用的装置是(填序号),再用制得的乙醛进行银镜反应,正确的操作顺序是(填序号).①向试管中滴入3滴乙醛溶液
②一边振荡一边滴入2%的稀氨水,直至最初产生的沉淀恰好溶解为止
③振荡后放入热水中,水浴加热
④在洁净的试管中加入1mL2%的AgNO3溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室通常用如图所示的装置来制取氨气。回答下列问题:
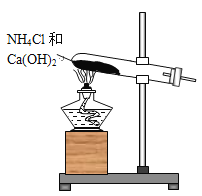
(1)安装仪器时要求试管口略低于试管底的原因是:_____________________________________________。
(2)制取氨气时的化学反应方程式为:___________________________________________。
(3)收集氨气时必须使用干燥的集气装置的原因是________________________。
(4)加热后将蘸有浓盐酸的玻璃棒靠近导管口,产生的现象是:____________________________________________________。
(5)除氨气外,还可以用该装置制取的常见气体是 _______________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组欲用酸性KMnO4和H2C2O4反应通过测定单位时间内生成 CO2的量来探究影响反应速率的因素,设计实验方案如表:
实验序号 | A 溶液 | B 溶液 |
① | 20 mL 0.1 molL﹣1 H2C2O4 溶液 | 30 mL 0.01 molL﹣1KMnO4 酸性溶液 |
② | 20 mL 0.2 molL﹣1 H2C2O4 溶液 | 30 mL 0.01 molL﹣1 KMnO4酸性溶液 |

(1)检验如图装置气密性的最简便方法为: .
(2)H2C2O溶液与酸性 KMnO4溶液反应的化学方程式为 .
(3)该实验探究的是因素对化学反应速率的影响,相同时间内针筒中所得CO2的体积大小关系是(填实验序号).
(4)若实验①在2min末收集了4.48mL CO2(标准状况下),则在2min末,c(MnO4﹣)=(若忽略溶液混合前后体积的变化).
(5)小组同学发现反应速率总是如图所示,积极探究t1~t2时间内速率变快的主要原因,提出假设可能是:①、②、③K+对该反应有催化作用.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一水合硫酸四氨合铜(Ⅱ)[Cu(NH3)4]SO4)H2O为深蓝色晶体,在工业上用途广泛,常用作杀虫剂、媒染剂.某学习小组探究制备该晶体并测定其组成的实验过程如下:(Ⅰ)晶体的制备原理及流程:
CuSO4+4NH3+H2O═[Cu(NH3)4]SO4)H2O
回答下列问题:
(1)无水乙醇的作用;烘干晶体的温度性质60℃的原因是;
(2)实验制得产物晶体中往往有Cu2(OH)2SO4杂质,分析产生该杂质的原因可能是;
(3)(Ⅱ)晶体中溶解于酸性溶液中,加入NaI溶液,Cu2+可与I作用产生I2和白色沉淀,该反应的离子方程式为 , 再用Na2S2O3溶液滴定I2 , 即可得Cu2+含量;
(4)(Ⅲ)晶体中氮含量的测定实验装置如图所示,称取0.9380g[Cu(NH3)x]SO4H2O晶体[M=(178+17x)g/mol]于锥形瓶a中,通过分液漏斗向锥形瓶a中滴加10%NaOH溶液,用1.000mol/L的NaOH标准滴定b中剩余的HCl.
滴定管读数如图所示,消耗标准液mL;[Cu(NH3)x]SO4H2O中x= , 推测测量值(x)比理论值偏小的原因是;
(5)(Ⅳ)SO42﹣含量的测定﹣﹣沉淀法称取一定质量的试样,加稀盐酸溶解,将BaCl2加入溶液中,静置得到BaSO4沉淀,检验沉淀已完全的操作为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.KMnO4溶液用盐酸酸化并加入H2O2:2MnO ![]() +6H++5H2O2=2Mn2++5O2↑+8H2O
+6H++5H2O2=2Mn2++5O2↑+8H2O
B.Fe2(SO4)3和Ba(OH)2溶液混合:Fe3++SO ![]() +Ba2++3OH﹣=BaSO4↓+Fe(OH)3↓
+Ba2++3OH﹣=BaSO4↓+Fe(OH)3↓
C.等体积等物质的量浓度的AlCl3、Ba(OH)2、HCl溶液混合:3H++Al3++6OH﹣=Al(OH)3↓+3H2O
D.水玻璃与稀醋酸混合:SiO ![]() +2H+=H2SiO3↓
+2H+=H2SiO3↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关化学反应的方向和速率的研究可以指导化工生产.下列说法正确的是( )
A.N2+3H2 ![]() 2NH3△H<0,在任何温度下均为自发反应
2NH3△H<0,在任何温度下均为自发反应
B.向新制氯水中加入少量小苏打固体可提高其漂白能力
C.1L密闭容器中发生反应4NH3+5O2?4NO+6H2O,充少量 N2可加快反应速率
D.湿法炼铜的反应为Fe+CuSO4=FeSO4+Cu,反应中的Fe可以用Na代替
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的装置,两烧杯中均为相应的水溶液,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,下列说法正确的是( ) 
A.某盐溶液可能是Mg(NO3)2溶液
B.甲池是a极上析出金属银,乙池是d极上析出某金属
C.甲池是b极上析出金属银,乙池是c极上析出某金属
D.某盐溶液可能是CuSO4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com