
| A、标准状况下,2.24L二氧化碳中含有共用电子对的数目为0.2NA |
| B、25℃时,pH=12的Na2CO3溶液中含有OH-的数目为0.01NA |
| C、常温常压下,28g乙烯和丙烯的混合气体中含有碳原子的数目为2NA |
| D、0.1mol Cl2与足量铁粉反应转移电子的数目为0.3NA |
| V |
| 22.4 |
| V |
| 22.4 |
| 2.24L |
| 22.4L/mol |
| 28g |
| 14g/mol |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子液体可以作为电池的电解质 |
| B、硝酸乙基铵水溶液呈碱性 |
| C、硝酸乙基铵水解的离子方程式表示为:C2H5NH3++H2O═C2H5NH2+H3O+ |
| D、相同温度下,相同物质的量浓度的硝酸乙基铵溶液和硝酸铵溶液前者的pH值小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
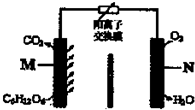 一种新型污水处理装置如图所示.该装置可利用一种微生物将有机废水的化学能直接转化为电能.下列说法中不正确的是( )
一种新型污水处理装置如图所示.该装置可利用一种微生物将有机废水的化学能直接转化为电能.下列说法中不正确的是( )| A、电池工作时H+从M极区移向N极区 |
| B、N极为正极,发生还原反应 |
| C、M极的电极反应式为:C6H12O6+6H2O-24e-═6CO2↑+24H+ |
| D、当N极消耗5.6L(标况下)气体时,则有2NA个H+通过离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠与氧气、水等反应时钠均作还原剂,则金属单质参与反应时金属单质均作还原剂 |
| B、铁能从硫酸铜溶液中置换出铜,则钠也能从硫酸铜溶液中置换出铜 |
| C、碳在少量氧气中燃烧生成CO、在过量氧气中燃烧生成CO2,则硫在少量氧气中燃烧生成SO2、在过量氧气中燃烧生成SO3 |
| D、铝粉在氧气中燃烧生成Al2O3,则铁丝在氧气中燃烧生成Fe2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验剩余的药品一般不能放回原试剂瓶 |
| B、溶解时用玻璃棒搅拌 |
| C、可燃性气体点燃前必须验纯 |
| D、过滤时玻璃棒靠在三层滤纸处 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定条件下,2.3g金属钠与氧气完全反应失电子数为0.1NA |
| B、常温常压下,氧气和臭氧(O3)的混合物32g中含有NA个氧原子 |
| C、1molOH- 中含有的电子数为9NA |
| D、0.1mol/L硫酸铝溶液中含有硫酸根的个数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Z与M形成的化合物中不可能含有非极性键 |
| B、对应氢化物的热稳定性:X>Y>M |
| C、单质的还原性:R>M>Y>X |
| D、X、Y、M、Z四种元素组成的离子化合物受热易分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com