
【题目】下列变化中,由加成反应引起的是
A. 乙烯通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色
B. 含碳原子较多的烷烃加热、加压、催化剂条件下反应生成含碳原子较少的烷烃和烯烃
C. 在光照条件下,C2H6与Cl2反应生成了油状液体
D. 在催化剂作用下, 乙烯与水反应生成乙醇
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
【题目】对于A+2B(g)![]() nC(g)。在一定条件下达到平衡后,改变下列条件,请回答:
nC(g)。在一定条件下达到平衡后,改变下列条件,请回答:
(1)当n=3时,增压,平衡不移动,则A为______态。
(2)若A为固态,增大压强,C的组分含量增加,则n_________,反应的平衡常数__________(填增大、减小或不变)。
(3)升温,平衡向右移动,达到新平衡前,υ正 ______υ逆(填>、< 或 =),则该反应的逆反应为_______热反应,反应的平衡常数__________(填增大、减小或不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把二氧化硫通入硝酸铁溶液中,溶液由黄色变为浅绿色,但立即又变为黄色,此时若滴入氯化钡溶液,则会产生白色沉淀。在上述一系列变化过程中,最终被还原的是
A. SO2 B. NO3- C. Fe3+ D. Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种短周期主族元素,原子序数依次增大.已知A的气态氢化物能与其最高价氧化物的水化物反应,B原子最外层电子数是电子层数的3倍,C+和D3+离子的电子层结构相同,B与E属于同一主族.
请回答下列问题:
(1)E在元素周期表中的位置是
(2)上述元素形成的简单离子中,半径最小的是(填离子符号).
(3)由上述元素中的一种或几种组成的物质甲可以发生如图1反应:
①若乙具有漂白性,则乙的电子式为 .
②若丙的水溶液是强碱性溶液,则甲为或(填化学式).
③若乙为二元弱酸,丙既能溶于强酸、又能溶于强碱,则乙的名称为;用电离方程式表示丙既能溶于强酸、又能溶于强碱的原因 .
④乙遇空气变为红棕色,有同学认为“浓硫酸可以干燥气体甲”,为验证其观点是否正确.用如图2装置进行实验时,分液漏斗中应加入(填试剂名称).实验过程中,浓硫酸中未发现有气体逸出,且溶液变为红棕色,由此得出的结论是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸是一种非常重要的化工原料,在工业上和实验室中有着广泛的应用.
(1)除铁锈(主要成分为Fe2O3),写出反应原理的离子方程式;
(2)制备硅胶,工业上可利用水玻璃和盐酸反应制备硅酸后,进一步处理可得到硅胶,写出水玻璃和盐酸反应的化学方程式;
(3)制氯气,实验室可以利用浓盐酸和高锰酸钾常温下反应来制取氯气, 反应同时还生成了MnCl2、KCl和H2O,写出该反应的化学方程式 , 在此反应中盐酸表现出了性.
(4)工业上可以利用如图所示装置制备盐酸,首先向(填A或B)管中通入氢气并点燃,然后再向(填A或B)管中通入氯气进行反应,此时火焰的颜色为 , 这样操作的理由是 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国工业制硫酸主要反应有(均为放热反应):①4FeS2+11O2![]() 8SO2+2Fe2O3,②2SO2+O2
8SO2+2Fe2O3,②2SO2+O2 ![]() 2SO3,③SO3+H2O=H2SO4。回答下列问题:
2SO3,③SO3+H2O=H2SO4。回答下列问题:
(1)为了提高反应①硫铁矿的利用率,可采取的措施有____________________。工业上也可以使用硫作为制取硫酸的方法,1g硫粉在氧气中充分燃烧放出9.36 kJ热量,写出硫燃烧的热化学方程式__________________________。
(2)反应②中SO2的平衡转化率(α)与某条件的关系如下图所示,其中正确的是________。
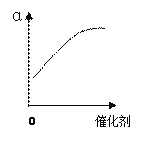

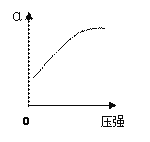
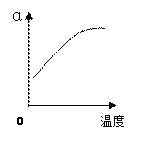
A B C D
(3)500oC和1.01×105Pa时将4.0 mol SO2和2.0 mol O2置于2L密闭容器中,反应达平衡时c(O2)=0.1 mol/L,则该反应的平衡常数等于_______,若将温度降到400oC,该反应的化学平衡常数__________(增大、减小或不变)。
(4)反应③得到“发烟硫酸”,往往稀释成98%的浓硫酸再出售。若分别用98%的浓硫酸、10%的稀硝酸、10%的稀醋酸分别与等量的NaOH溶液进行中和热的测定实验,三个反应的反应热依次为△H1、△H2、△H3,则它们的大小关系是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是( )
A.1L pH=l的硫酸溶液中含有的H+数目为0.2NA
B.1 mol羟基与l mol氢氧根离子所含质子数均为9NA
C.14 g由N2与CO组成的混合气体中含有的原子数目为2NA
D.标准状况下,2.24 L Cl2溶于水,转移的电子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅单质及其化合物的说法正确的是
①硅酸盐Na2Fe2Si3O10用氧化物的形式表示为:Na2O·2FeO·3SiO2
②水泥、玻璃、水晶饰物都是硅酸盐制品
③高纯度的硅单质广泛用于制作光导纤维
④单质硅是将太阳能转变为电能的常用材料
A. ②③ B. ①③ C. ①④ D. ④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的体积约为22.4L的是( )
A.标准状况下1molH2O
B.20℃、101kPa时36.5gHCl
C.常温常压下17gNH3
D.标准状况下0.4mol H2和0.6molO2的混合气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com