
【题目】盐酸是一种非常重要的化工原料,在工业上和实验室中有着广泛的应用.
(1)除铁锈(主要成分为Fe2O3),写出反应原理的离子方程式;
(2)制备硅胶,工业上可利用水玻璃和盐酸反应制备硅酸后,进一步处理可得到硅胶,写出水玻璃和盐酸反应的化学方程式;
(3)制氯气,实验室可以利用浓盐酸和高锰酸钾常温下反应来制取氯气, 反应同时还生成了MnCl2、KCl和H2O,写出该反应的化学方程式 , 在此反应中盐酸表现出了性.
(4)工业上可以利用如图所示装置制备盐酸,首先向(填A或B)管中通入氢气并点燃,然后再向(填A或B)管中通入氯气进行反应,此时火焰的颜色为 , 这样操作的理由是 . 
【答案】
(1)Fe2O3+6H+=2 Fe3++3H2O
(2)2HCl+Na2SiO3=H2SiO3(胶体)+2NaCl
(3)16HCl+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O;还原
(4)B;A;苍白色;氯气被过量的氢气所包围,使氯气得到充分反应,防止了对空气的污染
【解析】解:(1)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O,反应的离子方程式为:Fe2O3+6H+=2 Fe3++3H2O,所以答案是:Fe2O3+6H+=2 Fe3++3H2O;(2)制备硅胶,工业上可利用水玻璃和盐酸反应制备硅酸后,进一步处理可得到硅胶,写出水玻璃和盐酸反应的化学方程式为:2HCl+Na2SiO3=H2SiO3(胶体)+2NaCl,
所以答案是:2HCl+Na2SiO3=H2SiO3(胶体)+2NaCl;(3)制氯气,实验室可以利用浓盐酸和高锰酸钾常温下反应来制取氯气,反应同时还生成了MnCl2、KCl和H2O,写出该反应的化学方程式为:16HCl+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O,其中HCl表现了还原性和酸性,
所以答案是:16HCl+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O;还原性和酸性;(4)工业上可以利用如图所示装置制备盐酸,首先向B管中通入氢气并点燃,然后再向A管中通入氯气进行反应,此时火焰的颜色为苍白色火焰,这样操作的理由是氯气被过量的氢气所包围,使氯气得到充分反应,防止了对空气的污染,
所以答案是:B; A; 苍白色; 氯气被过量的氢气所包围,使氯气得到充分反应,防止了对空气的污染.
【考点精析】解答此题的关键在于理解氯气的实验室制法的相关知识,掌握实验室制法:MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】①②③④四种金属片两两相连浸入稀硫酸中都可组成电池,①②相连时,电路电流从②流向①;①③相连时,③为正极,②④相连时,②有气泡逸出现,③④相连时,③的质量减少,据此判断这四种金属活动性由大到小的顺序是
A. ①③②④ B. ①③④② C. ③④②① D. ③①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.NO2、SO2、BF3分子中所有原子的最外层电子都满足了8e-稳定结构
B.P4和CH4都是正四面体分子且键角都为109o28ˊ
C.NaCl晶体中与每个Na+距离相等且最近的Na+共有12个
D.原子间通过共价键而形成的晶体一定具有高的熔、沸点及硬度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组用浓度为0.20mol·L-1的盐酸标准液滴定含有一定量杂质的烧碱样品(杂质与酸不反应)溶于水形成的溶液。
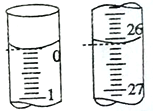
(1)准确量取一定体积的待测液需要使用的仪器是______________。
(2)若滴定开始和结束时,滴定管中的液面如图所示,则消耗盐酸标准液的体积为________mL。
(3)滴定时,若以酚酞为指示剂,滴定达到终点的标志是______________________________。
(4)将准确称取的5.0g烧碱样品配制成250mL待测液,并用盐酸标准液滴定。滴定前读数及滴定后读数如下表所示。
滴定次数 | 待测液体积(mL) | 0.20mol·L-1的盐酸体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 10.00 | 0.70 | 20. 60 |
第一次 | 10.00 | 4.00 | 24.10 |
第三次 | 10.00 | 1.10 | 21.10 |
由实验数据可知,烧碱的纯度为__________。
(5)下列操作会导致测得的待测液的浓度偏大的是________(填字母)。
a.部分标准液滴出锥形瓶外 b.用待测溶液润洗锥形瓶
C.锥形瓶洗净后还留有蒸馏水 d.放出碱液的滴定管开始有气泡,放出液体后气泡消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合处理“工业三废”,有利于保护环境,节约资源. 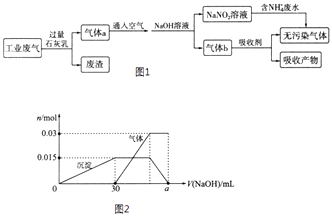
(1)为处理某工厂的工业废气(主要含N2、SO2、NO、CO,不考虑其他成分),设计了如图1流程:
已知:NO+NO2+2NaOH=2NaNO2+H2O;
2NO2+2NaOH=NaNO3+NaNO2+H2O.
①废渣的成分为(填化学式).
②通入空气不能过量,原因是 .
③吸收剂所吸收的气体主要是
④处理含NH4+废水时,发生反应的离子方程式为
(2)某无色工业废水中可能含有NH4+、Na+、Al3+、Cu2+、Cl﹣、SO42﹣、CO32﹣等离子中的几种离子.为确定其成分,设计如下实验:
a.取10mL该废水于试管中,加入足量的Ba(NO3)2溶液和稀硝酸,充分反应后过滤得到0.04mol白色沉淀,向滤液中加入AgNO3溶液无沉淀产生.
b.另取10mL该废水于试管中,滴加NaOH溶液产生白色沉淀,当沉淀增加到一定量后开始产生气体,最后沉淀完全溶解.沉淀和气体的物质的量随加入NaOH溶液体积的变化关系如图2所示.(不考虑沉淀、气体的溶解和损失)
根据上述实验和图表数据:
①该废水中一定含有的离子有(填离子符号).
②实验室配制100mL所需浓度的NaOH溶液时,用到的玻璃仪器除烧杯、玻璃棒、量筒外,还需要(填仪器名称).
③图中a= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中,由加成反应引起的是
A. 乙烯通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色
B. 含碳原子较多的烷烃加热、加压、催化剂条件下反应生成含碳原子较少的烷烃和烯烃
C. 在光照条件下,C2H6与Cl2反应生成了油状液体
D. 在催化剂作用下, 乙烯与水反应生成乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用废旧铝铁合金(主要成分为Fe、Al、Fe2O3、Al2O3)制备纳米材料磁性Fe3O4粒子及副产物Al,制备流程图如图: 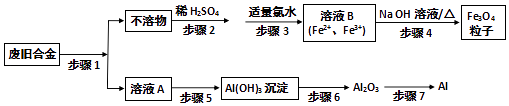
回答下列问题:
(1)步骤1中所用的试剂是 , 涉及的化学反应中属于氧化还原反应的化学方程式为
(2)步骤3中反应的离子方程式为 .
(3)步骤5可选用的试剂或操作最合理的是(填序号). a.NaOH溶液 b.氨水 c.盐酸 d.通入过量的CO2
(4)步骤7中每获得副产物Al 27g,转移的电子数目为 .
(5)下列关于磁性Fe3O4粒子的说法正确的是(填序号).
A.磁性Fe3O4粒子会产生丁达尔效应
B.磁性Fe3O4粒子的化学性质与原来的Fe3O4完全不同
C.磁性Fe3O4粒子属于胶体分散系
D.磁性Fe3O4粒子能透过滤纸.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)能净化有毒废水中的氰化钠(NaCN),生成NaCl、CO2和N2 , 下列说法正确的是( )
A.被氧化的元素是氯元素
B.氧化产物与还原产物的物质的量之比为1:1
C.消耗1mol还原剂,转移5 mol电子
D.净化1 L含CN﹣1.04 mgL﹣1的废水,理论上需用2×l0﹣5mol C1O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图是一学生设计的在实验室制取纯净、干燥的氯气的实验装置图. 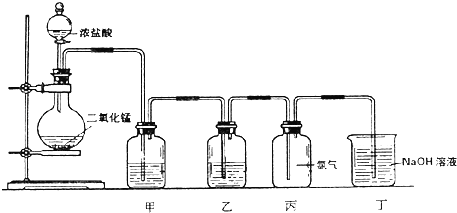
(1)该实验装置中还缺少的仪器及用品是; .
(2)为除去Cl2中混有的水蒸汽和氯化氢气体,洗气瓶甲和乙中分别盛放下列哪种溶液(填序号):甲 , 乙 A.浓H2SO4 B.饱和食盐水 C.澄清石灰水 D.淀粉KI溶液
(3)丁装置的作用是 , 反应的离子方程式是 .
(4)烧瓶中发生反应的化学方程式是 .
(5)若要检验集气瓶丙的瓶塞处是否密封好,可用湿润的淀粉碘化钾试纸进行检测,若漏气,试纸变色,反应的离子方程式是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com