
为减小和消除过量CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)最近有科学家提出“绿色自由”构想:先把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
写出分解池中反应的化学方程式 。在合成塔中,当有4.4 kg CO2与足量H2
完全反应,可放出热量4947 kJ,写出合成塔中反应的热化学方程式 。
(2)以CO2为碳还可以制备乙醇,反应如下:
2CO2(g) + 6H2(g)= CH3CH2OH(g) + 3H2O(g) △H=-173.6kJ/mol
写出由CH3OH(g)合成CH3CH2OH(g)的反应的热化学方程式 。
(3)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。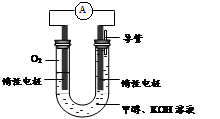
①该电池正极的电极反应为 。
②工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为 。当电子转移 mol时,参加反应的氧气的体积是6.72L(标准状况下)。
(4)以甲醇为燃料还可制作新型燃料电池,电池的正极通入O2,负极通入甲醇,用熔融金属氧化物MO作电解质(可传导O2-)。该电池负极发生的电极反应是 ;放电时,O2-移向电池的 (填“正”或“负”)极。
(1)2KHCO3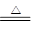 K2CO3+H2O+CO2↑(2分)
K2CO3+H2O+CO2↑(2分)
CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H=-49.47kJ/mol(2分)
(2)2CH3OH(g) =CH3CH2OH(g)+ H2O(g) △H=-74.66kJ/mol(2分)
(3)① O2 + 2H2O + 4e-= 4OH- (2分)
②2CH3OH + 3O2 + 4OH-= 2CO32- + 6H2O (2分) ; 1.2mol(2分)
(4)CH3OH-6e-+3O2-= CO2+2H2O(2分) 负(1分)
解析试题分析:(1)分解池中反应的化学方程式2KHCO3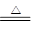 K2CO3+H2O+CO2↑。根据4.4 kg CO2与足量H2恰好完全反应,可放出4 947 kJ的热量,则1 mol CO2与氢气合成甲醇放出热量49.47 kJ的热量,所以热化学方程式为CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=﹣49.47kJ/mol;(2)2CO2(g) + 6H2(g)= CH3CH2OH(g) + 3H2O(g) △H=-173.6kJ/mol,根据盖斯定律,对(1)中方程式乘以2然后用该方程式减去(1),可以得到CH3OH(g)合成CH3CH2OH(g)的反应的热化学方程式2CH3OH(g) =CH3CH2OH(g)+ H2O(g) △H=-74.66kJ/mol。(3)氧气在正极上被还原,在碱性条件下生成水,电池正极电极反应式为 O2 + 2H2O + 4e-= 4OH- ,电池的正极上有聚集的电子,放电时,电解质溶液的阳离子向电池的正极移动,即H+移向电池的正极。②工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为 2CH3OH + 3O2 + 4OH-= 2CO32- + 6H2O 。参加反应的氧气的体积是6.72L(标准状况下),物质的量是0.3mol,转移电子物质的量为1.2mol。(4)甲醇在负极失去电子,该电池负极发生的电极反应是CH3OH-6e-+3O2-= CO2+2H2O;放电时,O2-移向电池的负极。
K2CO3+H2O+CO2↑。根据4.4 kg CO2与足量H2恰好完全反应,可放出4 947 kJ的热量,则1 mol CO2与氢气合成甲醇放出热量49.47 kJ的热量,所以热化学方程式为CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=﹣49.47kJ/mol;(2)2CO2(g) + 6H2(g)= CH3CH2OH(g) + 3H2O(g) △H=-173.6kJ/mol,根据盖斯定律,对(1)中方程式乘以2然后用该方程式减去(1),可以得到CH3OH(g)合成CH3CH2OH(g)的反应的热化学方程式2CH3OH(g) =CH3CH2OH(g)+ H2O(g) △H=-74.66kJ/mol。(3)氧气在正极上被还原,在碱性条件下生成水,电池正极电极反应式为 O2 + 2H2O + 4e-= 4OH- ,电池的正极上有聚集的电子,放电时,电解质溶液的阳离子向电池的正极移动,即H+移向电池的正极。②工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为 2CH3OH + 3O2 + 4OH-= 2CO32- + 6H2O 。参加反应的氧气的体积是6.72L(标准状况下),物质的量是0.3mol,转移电子物质的量为1.2mol。(4)甲醇在负极失去电子,该电池负极发生的电极反应是CH3OH-6e-+3O2-= CO2+2H2O;放电时,O2-移向电池的负极。
考点:本题以对CO2创新利用的研究为载体,考查热化学方程式、原电池,难度中等,旨在考查学生对知识的掌握及迁移运用能力。


科目:高中化学 来源: 题型:填空题
甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g)=CH3OH(g) ΔH1
反应Ⅱ:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH2
①上述反应符合“原子经济”原则的是________(填“Ⅰ”或“Ⅱ”)。
②下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)。
| 温度 | 250 ℃ | 300 ℃ | 350 ℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
保护环境已成为当前和未来的一项全球性重大课题。为解决目前燃料使用过程中的环境污染问题,并缓解能源危机,有的专家提出利用太阳能促使燃料循环使用的构想,如图所示: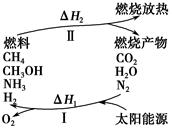
过程Ⅰ可用如下反应表示:
①2CO2 2CO+O2 ②2H2O===2H2+O2 ③2N2+6H2O
2CO+O2 ②2H2O===2H2+O2 ③2N2+6H2O 4NH3+3O2 ④2CO2+4H2O
4NH3+3O2 ④2CO2+4H2O 2CH3OH+3O2 ⑤2CO+4H2O
2CH3OH+3O2 ⑤2CO+4H2O ________+3O2
________+3O2
请回答下列问题:
(1)过程Ⅰ的能量转化形式为________能转化为________能。
(2)请完成第⑤个反应的化学方程式:____________________。
(3)上述转化过程中,ΔH1和ΔH2的关系是________。
(4)断裂1 mol化学键所需的能量见下表:
| 共价键 | H—N | H—O | N≡N | O===O |
| 断裂1 mol化学键所需能量/(kJ·mol-1) | 393 | 460 | 941 | 499 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
运用化学反应原理知识在工业生产中有重要意义。
(1) 工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下: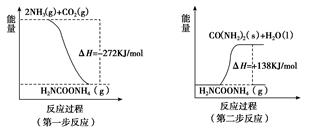
则NH3(g)与CO2(g)反应生成尿素的热化学方程式为___________ _____。
(2)工业生产中用CO可以合成甲醇CO(g)+2H2(g)  CH3OH(g),ΔH=-90.1 kJ·mol-1 在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示。
CH3OH(g),ΔH=-90.1 kJ·mol-1 在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如图所示。
①p1________p2(填“大于”、“小于”或“等于”);
②100 ℃时,该反应的化学平衡常数K=_ ____(mol·L-1)-2;
③在其它条件不变的情况下,再增加a mol CO和2a molH2,达到新平衡时,CO的转化率________(填“增大”、“减小”或“不变”)。
(3)工业生产中用SO2为原料制取硫酸
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池的负极的电极反应式___ ____________。
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如下图所示。请写出开始时阳极反应的电极反应式____ ______。
(4)工业生产中用氨水吸收SO2
若将等物质的量的SO2与NH3溶于水充分反应,写出该反应的离子方程式 ,所得溶液呈 性。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铜单质及其化合物在工业生产和科研中有重要作用。
(1)已知:2Cu2O(s) + O2(g) = 4CuO(s)△H=-292kJ·mol-1
2C(s)+O2(g)=2CO(g) △H=-221kJ·mol-1
请写出用足量炭粉还原CuO(s)制备Cu2O(s)的热化学方程式: ;
(2)现用氯化铜晶体(CuCl2·2H2O,含氯化亚铁杂质)制取纯净的CuCl2·2H2O。先将其制成水溶液,后按如图步骤进行提纯: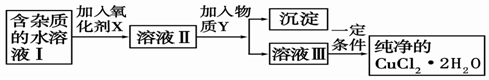
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表
| 金属离子 | Fe3+ | Fe2+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9.0 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上常利用CO和H2合成可再生能源甲醇。
(1)已知CO(g)、CH3OH(l)的燃烧热分别为283.0 kJ·mol-1和726.5 kJ·mol-1,则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为 。
(2)合成甲醇的方程式为CO(g)+2H2(g) CH3OH(g) ΔH <0。
CH3OH(g) ΔH <0。
在230 ℃?270 ℃最为有利。为研究合成气最合适的起始组成比n(H2):n(CO),分别在230 ℃、250 ℃和270 ℃进行实验,结果如下左图所示。其中270 ℃的实验结果所对应的曲线是_____(填字母);当曲线X、Y、Z对应的投料比达到相同的CO平衡转化率时,对应的反应温度与投较比的关系是 。
(3)当投料比为1∶1,温度为230 ℃,平衡混合气体中,CH3OH的物质的量分数为 (保留1位小数);平衡时CO的转化率 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氨有着广泛的用途,可用于化肥、硝酸、合成纤维等工业生产。
(1)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应可生成氨气: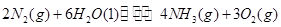
该反应在固定体积的密闭容器中进行,有关说法正确的是_____________(填序号字母)。
A.反应处于平衡状态时,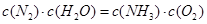 |
B.反应达到平衡后,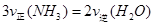 |
| C.体系的总压强不变,说明反应已达平衡 |
| D.混合气体的密度保持不变,说明反应已达平衡 |
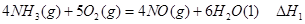 ①
①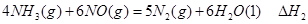 ②
②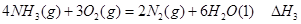 ③
③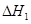 、
、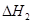 、
、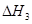 三者之间关系的表达式,
三者之间关系的表达式,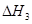 =_________。
=_________。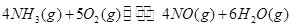
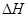 =
=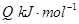


| 时间/浓度 |   | 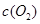  | 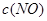  | 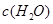  |
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第2min | 3.2 | a | 0.8 | 1.2 |
| 第4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第6min | 2.0 | 3.0 | 2.0 | 3.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氨在国民经济中占有重要地位。
(1)工业合成氨时,合成塔中每产生1 mol NH3,放出46.1 kJ的热量。
① 工业合成氨的热化学方程式是 。
② 已知:
N2 (g)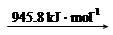 2N (g)
2N (g)
H2 (g)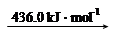 2H (g)
2H (g)
则断开1 mol N-H键所需的能量是_______kJ。
(2)下表是当反应器中按n(N2):n(H2)=1:3投料后,在200℃、400℃、600℃下,反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线。
① 曲线a对应的温度是 。
② 关于工业合成氨的反应,下列叙述正确的是 (填字母)。
A. 及时分离出NH3可以提高H2的平衡转化率
B. 加催化剂能加快反应速率且提高H2的平衡转化率
C. 上图中M、N、Q点平衡常数K的大小关系是K(M)=" K(Q)" >K(N)
③ M点对应的H2转化率是 。 (3)氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。电池的总反应为:
(3)氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料。电池的总反应为:
4NH3(g) + 3O2(g) = 2N2(g) + 6H2O(g)。
则该燃料电池的负极反应式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
Ⅰ在催化剂作用下,CO2和H2可以制取甲醇。用工业废气中的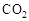 可制取甲醇,其反应为:CO2+3H2
可制取甲醇,其反应为:CO2+3H2 CH3OH+H2O 常温常压下已知下列反应的能量变化如图示:
CH3OH+H2O 常温常压下已知下列反应的能量变化如图示:
写出由二氧化碳和氢气制备甲醇的热化学方程式: 。
Ⅱ硼氢化钠(NaBH4)是有机合成中的重要还原剂。最新研究发现,以NaBH4和H2O2为原料,NaOH溶液作电解质溶液,可以设计成全液流电池,其工作原理如图所示,假设电池工作前左右两槽溶液的体积各为1L,回答下列问题:
(1)电极b为 (填“正极”或“负极”),电极a上发生反应的电极反应式为 。
(2)电池工作时,Na+向 极(填“a”或“b”)移动,当左槽产生0.0125molBO2—离子时,右槽溶液pH=
(3)用该电池电解一定浓度的CuSO4溶液至无色后继续电解一段时间。断开电路,向溶液中加入0.1molCu(OH)2,溶液恢复到电解之前状态,则电解过程中转移电子数目为_________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com