
| A、碱性条件下KIO3与KI溶液发生反应生成I2:IO3-+5I-+6H+=3I2+3H2O |
| B、氯气与水反应:Cl2+H2O═2H++Cl-+ClO- |
| C、石灰乳中滴加少量Na2CO3溶液:Ca2++CO32-═CaCO3↓ |
| D、NO2与水反应:3NO2+H2O═2H++2NO3-+NO↑ |


科目:高中化学 来源: 题型:
| A、酸性:HClO4>HBrO4>HIO4 |
| B、非金属性:F>O>S |
| C、稳定性:PH3>H2S>HCl |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱电解质 | HCOOH | HCN | H2CO3 | NH3?H2O |
| 电离平衡常数(25℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=1.8×10-5 |
| A、结合H+的能力:CO32->CN->HCO3->HCOO- |
| B、0.1mol/L的HCOONH4溶液中存在以下关系式:c(HCOO-)>c(NH4+)>c(H+)>c(OH-) |
| C、pH=3的盐酸与pH=11的氨水混合,若溶液显中性,则V(盐酸)>V(氨水) |
| D、0.1mol/L的Na2CO3溶液中:c(Na+ )+c(H+)=c(HCO3-)+c(OH-)+c(CO3 2-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na、Mg、Al原子的最外层电子数依次减小 |
| B、C、N、O的原子半径依次减小 |
| C、Si、P、S元素的最高价依次降低 |
| D、Li、Na、K的金属性依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
查看答案和解析>>
科目:高中化学 来源: 题型:
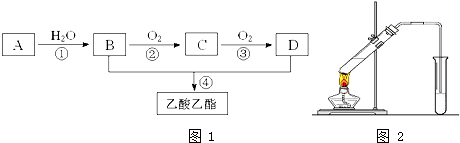
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com