
【题目】粮食仓储常用磷化铝(A1P)熏蒸杀虫,A1P遇水即产生强还原性的PH3气体。国家标准规定粮食中磷化物(以PH3计)的残留量不超过0.05 mgkg-1时为合格。某小组同学用图所示实验装置和原理测定某粮食样品中磷化物的残留量。C中加入100 g原粮,E 中加入20.00mL2.50×l0-4molL-1KMnO4溶液(H2SO4酸化),C中加入足量水,充分反应后,用亚硫酸钠标准溶液滴定E中的溶液。
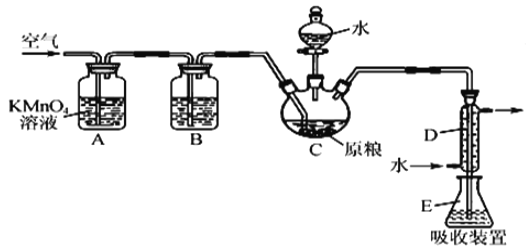
(1)装置A中的KMnO4溶液的作用是_____。
(2)装置B中盛装焦性没食子酸的碱性溶液吸收空气中的O2。若去掉该装置,则测得的磷化物的残留量______________________(填“偏髙”“偏低”或“不变”)。
(3)装置E中PH3氧化成磷酸,MnO4-被还原为Mn2+,写出该反应的离子方程式:___________
(4)收集装置E中的吸收液,加水稀释至250 mL,量取其中的25.00 mL于锥形瓶中, 用4.0×l0-5molL-1的Na2SO3标准溶液滴定,消耗Na2SO3标准溶液20.00mL,反应原理是 SO32-+MnO4-+H+→SO42-+Mn2++H20(未配平)通过计算判断该样品是否合格(写出计算过程)___________。
【答案】吸收空气中的还原性气体,防止其干扰PH3的测定 偏低 5PH3+8MnO4-+24H+=5H3PO4+8Mn2++12H2O 不合格(过程见解析)
【解析】
(1)利用PH3的还原性,测定PH3的含量;
(2)空气中的O2能氧化PH3;
(3)根据得失电子守恒配平氧化还原反应的离子方程式。
(4)PH3、Na2SO3共同消耗KMnO4溶液。
(1) 利用PH3的还原性,测定PH3的含量,所以装置A中的KMn04溶液的作用是吸收空气中的还原性气体,防止其干扰PH3的测定。
(2)空气中的O2能氧化PH3,若不用焦性没食子酸的碱性溶液吸收空气中的O2,则消耗KMnO4溶液的体积偏小,测得的磷化物的残留量偏低;
(3)装置E中PH3氧化成磷酸,MnO4-被还原为Mn2+,根据得失电子守恒,该反应的离子方程式是5PH3+8MnO4-+24H+=5H3PO4+8Mn2++12H2O;
(4) 25mL溶液中未反应的n(KMnO4)=![]() ;
;
250mL溶液中未反应的n(KMnO4) ![]() ;
;
与PH3反应的n(KMnO4)=![]() ;
;
n(PH3 )=![]() n(KMnO4)=
n(KMnO4)= ![]()
![]() =
= ![]() ;
;
100g原粮中n(PH3 )= ![]()
![]() 3.825
3.825![]() g;
g;
1Kg原粮中n(PH3 )= 3.825![]() g=0.3825mg>0.05mg,所以不合格。
g=0.3825mg>0.05mg,所以不合格。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】次磷酸钠(NaH2PO2)是有机合成的常用还原剂,一般制备方法是将黄磷(P4)和过量烧碱溶液混合、加热,生成次磷酸钠和PH3,PH3是一种无色、有毒且能自燃的气体。实验装置如图所示:
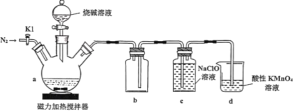
回答下列问题:
(1)在a中加入黄磷、活性炭粉末,打开K1,通入N2一段时间,关闭K1,打开磁力加热搅拌器,滴加烧碱溶液。
①仪器a的名称是______,已知NaH2PO2能与盐酸反应但不能与NaOH溶液反应,则次磷酸(H3PO2)是_______元弱酸。
②反应开始时,首先打开K1,通入N2一段时间,其目的是________。
③为了尽可能避免PH3造成的空气污染,拆卸装置前还要进行的一项操作是_________,a中反应的化学方程式为_______。
(2)装置c中生成NaH2PO2和NaCl,相关物质溶解度(S)如下,通过______的方法可分离出NaH2PO2固体。

(3)产品纯度测定:
取产品m g配成250mL溶液,取25mL于锥形瓶中,然后用0.01 mol/L KMnO4标准溶液滴定至终点(氧化产物是PO43-),达到滴定终点时消耗V1 mL KMnO4标准溶液,产品纯度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某烷烃分子中电子总数为42。
(1)该烷烃的分子式为_____________________________________。
(2)写出该烷烃分子的所有同分异构体的结构简式______________________。
(3)上述同分异构体中,在相同条件下沸点最低的是______________________________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验可以达到目的或得出结论的是( )
选项 | 实验目的或结论 | 实验过程 |
A | 探究浓硫酸的脱水性 | 向表面皿中加入少量胆矾,再加入约3mL浓硫酸,搅拌,观察实验现象 |
B | 相同温度下,Ksp(ZnS)<Ksp(CuS) | 向2mL ZnSO4 和CuSO4的混合溶液中逐滴加入0.01mol/L Na2S溶液,先出现白色沉淀 |
C | 淀粉已经完全水解 | 取少量酸催化后的淀粉水解液于试管中,先加入过量氢氧化钠溶液中和酸,再加少量碘水,溶液未变蓝 |
D |
| 向NaAlO2的试管中滴加碳酸氢钠溶液,产生白色沉淀 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.甲烷分子的比例模型为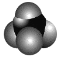 ,其二氯取代物有 2 种结构
,其二氯取代物有 2 种结构
B.苯和乙烯都能使溴水褪色,其褪色原理相同
C.相同质量的乙炔与苯分别在足量的氧气中完全燃烧,消耗氧气的物质的量相同
D.在一定条件下,乙烯与氢气反应生成乙烷属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取乙酸乙酯的装置。请回答:
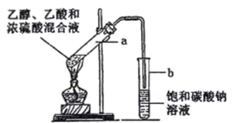
(1) 写出乙酸、乙醇酯化反应方程式__________
(2) 浓硫酸的作用是__________
(3) 下列有关该实验的说法中,正确的是__________
A.向 a 试管中加入沸石,其作用是防止加热时液体暴沸
B.饱和碳酸钠溶液可以除去产物中混有的乙酸
C.乙酸乙酯是一种无色透明、密度比水大的油状液体
D.若原料为 CH3COOH 和 CH3CH218OH,则乙酸乙酯中不含18O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用小粒径零价铁(ZVI)的电化学腐蚀处理三氯乙烯,进行水体修复的过程如图所示。H+,O2,NO3-等共存物的存在会影响水体修复效果,定义单位时间内ZVI释放电子的物质的量为nt,其中用于有效腐蚀的电子的物质的量为ne。下列说法错误的是( )
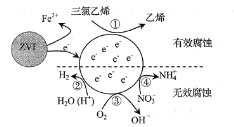
A. 反应①②③④均在正极发生
B. 单位时间内,三氯乙烯脱去amolCl时ne=amol
C. ④的电极反应式为NO3-+10H++8e-=NH4++3H2O
D. 增大单位体积水体中小粒径ZVI的投入量,可使nt增大
查看答案和解析>>
科目:高中化学 来源: 题型:
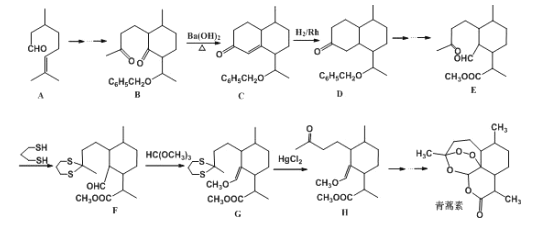
【题目】我国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学或医学奖。青蒿素的一种化学合成方法的部分工艺流程如图所示:
己知:①C6H5-表示苯基;②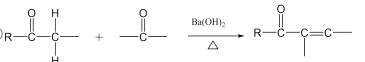
(1)化合物E中含有的含氧官能团有__、__和羰基(写名称)。
(2)合成路线中设计E→F、G→H的目的是__。
(3)B→C实际上是分两步反应进行的,先进行加成反应,再进行__反应。
(4)A在Sn-p沸石作用下,可生成同分异构体异蒲勒醇,己知异蒲勒醇分子中有3个手性碳原子(连有四个不同基团的碳原子称为手性碳原子),异蒲勒醇分子内脱水后再与H21:1发生1,4-加成可生成![]() ,则异蒲勒醇的结构简式为:__。
,则异蒲勒醇的结构简式为:__。
(5)A的同分异构体Y含有醛基和六元碳环,且环上只有一个支链,满足上述条件的Y有__种,其中核磁共振氢谱峰数最少的物质的结构简式为__。
(6)如图是以乙烯为原料制备苄基乙醛![]() 的合成路线流程图。
的合成路线流程图。
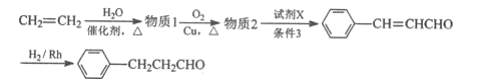
请填写下列空白(有机物写结构简式):
物质1为__;物质2为__;试剂X为__;条件3为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组利用右图所示装置制备CO2气体,其中K为止水夹,多孔塑料板固定在试管的某一位置。请问答以下问题:
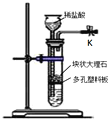
(1)当止水夹K打开时,大理石即可与稀盐酸反应产生CO2气体;当止水夹关闭后,该反应可随后停止。起到这种随关随停作用的主要原因是 __________
(2)实验室可以利用上述装置制备某些气体,能达到随开随用,随关随停的有__________
A.锌粒和稀硫酸制氢气 B.浓盐酸和二氧化锰制取氯气
C.Na2SO3固体和硫酸反应制备SO2 D.利用FeS块状固体与稀硫酸反应制备H2S气体
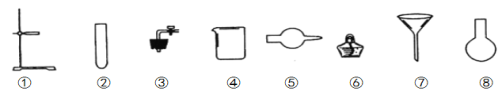
(3)请你选用如图所示的部分仪器,装配成一个简易的、能随开随用、随关随停的CO2气体发生装置。应选用的仪器是__________(填仪器的编号)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com