
Fe和Al是两种常见的金属,将它们按一定的质量比组成混合物。
(1)取一定质量的该混合物,向其中加入足量的NaOH溶液。生成气体的体积在标准状况下为a L,则反应的离子方程式为________________;混合物中的Al的物质的量为________(用含字母的表达式表示)。
(2)另取相同质量的该混合物,向其中加入足量的稀硫酸,固体全部溶解,生成气体的体积在标准状况下b L,则反应中转移电子的物质的量为________;混合物中Fe的质量为________(用含字母的表达式表示)。
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
28(10分)水钴矿中除SiO2外,还有9.24% CoO、2.78% Fe2O3、0.96% MgO、0.084 % CaO。从中提 取钴的主要工艺流程如下:
取钴的主要工艺流程如下:

(1)请配平下列除铁的化学方程式:
Fe2(SO4)3+ H2O+ Na2CO3= Na2Fe6(SO4)4(OH)12↓+ Na2SO4+ CO2↑
(2)“除钙、镁”的原理反应为:
MgSO4+2NaF=MgF2↓+Na2SO4,CaSO4+2NaF=CaF2↓+Na2SO4
已知KSP(CaF2)=1.11×10-10,KSP(MgF2)=7.40×10-11,加入过量NaF溶液反应完全后过滤,则滤液中 。
。
(3)“沉淀”中含杂质离子主要有SO42-、F-、 和 ;“操作X”包括 和 。
(4)向氯化铜溶液中加入一定量的铁粉和铝粉混合物,充分反应后,下列情况可能出现的是________
a.溶液中有Cu2+、Fe2+、Al3+,不溶物为Cu
 b.溶液中有Fe2+、Al3+,不溶物为Cu、Fe
b.溶液中有Fe2+、Al3+,不溶物为Cu、Fe
c.溶液中有Fe3+、Al3+,不溶物为Cu
d.溶液中有Fe2+,不溶物为Cu、Al
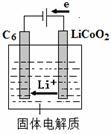
(5)某锂离子电池正极是LiCoO2,含Li+导电固体为电解质。充电时,Li+还原为Li,并以原子形式嵌入电池负极材料碳-6(C6)中(如图所示)。电池反应为
 LiCoO2 + C6 CoO2 + LiC6 ,写出该电池放电时的正极反应式 。
LiCoO2 + C6 CoO2 + LiC6 ,写出该电池放电时的正极反应式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有一真空瓶质量为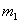 ,该瓶充入空气后质量为
,该瓶充入空气后质量为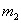 。在相同状况下,若改为充入某气体A时,总质量为
。在相同状况下,若改为充入某气体A时,总质量为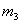 。则A的相对分子质量是( )
。则A的相对分子质量是( )
A.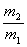 ×29 B.
×29 B.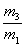 ×29 C.
×29 C.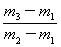 ×29 D.
×29 D.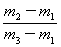 ×29
×29
查看答案和解析>>
科目:高中化学 来源: 题型:
能完全中和20 mL 1 mol /L NaOH溶液生成正盐的溶液是( )。
A.40 mL 0.1 mol /L盐酸 B.20 mL1 mol /L硫酸溶液
C.10 mL 1 mol /L硫酸溶液 D.5mL 1 mol /L磷酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下面有关氧化还原反应的叙述正确的是( )。
A.金属单质在反应中只作还原剂
B.非金属单质在反应中只作氧化剂
C.金属原子失电子越多其还原性越强
D.Cu2+比Fe2+的氧化性强,Fe比Cu的还原性强
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4HNO3(浓)+Cu=Cu(NO3)2+2NO2↑+2H2O,下列说法正确的是( )。
A.HNO3是氧化剂,NO2是氧化产物
B.若2mol HNO3(浓)完全反应,则反应中共转移了NA个电子
C.还原剂与氧化剂的物质的量比是1 :4
D.氧化产物和还原产物的物质的量之比为2 :1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列反应的热化学方程式为:
(1)C(s)+O2(g)=CO2(g) ΔH 1=-393.5kJ/mol
(2)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH 2=-870.3kJ/mol
(3)H2(g)+1/2O2(g)=H2O(l) ΔH 3=-285.8kJ/mol
则2C(s)+2H2(g)+O2(g)=CH3COOH(l) 的反应热ΔH为
A.+488.3 kJ/mol B.-488.3 kJ/mol C.-244.15 kJ/mol D.+244.15 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
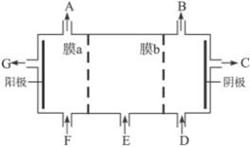
现有阳离子交换膜、阴离子交换膜、石墨电极,请用氯碱工业中的膜技术原理,回答下列问题。
(1)写出氯碱工业中电解饱和食盐水的离子方程式 ;
(2)请利用交换膜技术,根据上图框架,设计一个电解硫酸钠溶液制氢氧化钠溶液和硫酸溶液的装置,标出进出物质的化学式:
A_________;C_________; E_________;膜b为 离子交换膜(填“阳”或“阴”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com