
����Ŀ��25��ʱ����20.00mL0.100molL-1�İ�ˮ�ʹ������Һ�зֱ�μ�0.100molL-1��������Һ����ҺpH�������������ı仯��ͼ��ʾ������˵������ȷ���ǣ� ��
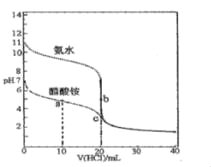
A.25��ʱ��Kb��NH3H2O����Ka��CH3COOH����10-5
B.b����Һ��ˮ�ĵ���̶ȱ�c����Һ�еĴ�
C.��c�����Һ�У�c��Cl������c��CH3COOH����c��NH4+����c��OH����
D.��a�����Һ�У�c��NH4+��+2c��H+���T2c��CH3COO-��+c��NH3H2O��+2c��OH-��
���𰸡�C
��������
A.����ͼ���֪��0.100molL��1�İ�ˮ��pH=11��c��OH����=10��3mol/L��Kb��NH3H2O��=![]() =10��5���������Һ��pH=7��˵��笠����Ӻʹ����ˮ��̶���ȣ�����ߵĵ���ƽ�ⳣ����ȣ���25��ʱ��Kb��NH3H2O��=Ka��CH3COOH����10��5����A��ȷ��
=10��5���������Һ��pH=7��˵��笠����Ӻʹ����ˮ��̶���ȣ�����ߵĵ���ƽ�ⳣ����ȣ���25��ʱ��Kb��NH3H2O��=Ka��CH3COOH����10��5����A��ȷ��
B.����20mL��Ũ�ȵ�HCl��Һ��ˮǡ�÷�Ӧ�����Ȼ�泥�b��笠�����ˮ��ٽ���ˮ�ĵ��룬��c������Ϊ������Ȼ�泥�����������������ʹ��Һ�����ԣ�������ˮ�ĵ��룬��b����Һ��ˮ�ĵ���̶ȱ�c����Һ�еĴ�B��ȷ��
C.Kb��NH3H2O��=Ka��CH3COOH����10��5��Kh��NH4+��=![]() ��10��9��10��5������ĵ���̶Ƚϴ���c��NH4+����c��CH3COOH������ȷ������Ũ�ȴ�СΪ��c��Cl������c��NH4+����c��CH3COOH����c��OH��������C����
��10��9��10��5������ĵ���̶Ƚϴ���c��NH4+����c��CH3COOH������ȷ������Ũ�ȴ�СΪ��c��Cl������c��NH4+����c��CH3COOH����c��OH��������C����
D.��a�����Һ�з�Ӧ������Ϊ��Ũ�ȵ�CH3COONH4��NH4Cl��CH3COOH�����ݵ���غ��֪��c��NH4+��+c��H+���Tc��CH3COO����+c��Cl����+c��OH���������������غ�ɵã�2c��Cl����=c��NH4+��+c��NH3H2O�������߽�Ͽɵã�c��NH4+��+2c��H+���T2c��CH3COO����+c��NH3H2O��+2c��OH��������D��ȷ��
��ѡC��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧģ�����о���ѧ���⣬��ֱ���ּ�࣬���н���������ģ����ȷ���ǣ� ��
A������������ȼ�գ��Ƶ��������![]()
B������Cl2��ȼ�գ������������![]()
C��A1C13��Һ�еμ�NaOH��Һ����ϵ����Ԫ�صĴ�����ʽ:![]()
D��FeI2��Һ��ͨ��Cl2����Ԫ�ش�����ʽ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ϊ1L���ܱ�������(�������)����1molCO2��3molH2��һ�������·�����Ӧ��CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)�����CO2��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ������˵����ȷ���ǣ� ��
CH3OH(g)+H2O(g)�����CO2��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ������˵����ȷ���ǣ� ��

A.���е�3����ʱ������Ӧ���ʺ��淴Ӧ�������
B.10���Ӻ������и�����Ũ�Ȳ��ٸı�
C.�ﵽƽ��������¶ȣ�����Ӧ���������淴Ӧ���ʼ�С
D.10min����H2��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ0.075mol/(L��s)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ��Ⱦ������̫���ܵ�ص�ʾ��ͼ����ص�һ���缫���л�����Ⱦ�ϣ�R��Ϳ����TiO2����������Ƴɣ���һ�缫�ɵ��粣���Ʋ����ɣ����й��ڸõ����������ȷ���ǣ� ��

A.Ⱦ������TiO2�缫Ϊ��ظ���������������Ӧ
B.�����缫��Ӧʽ�ǣ�I3-+2e-=3I-
C.����ܷ�Ӧ�ǣ�2R++3I-=I3-+2R
D.��ع���ʱ��̫����ת��Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȷ��ȡ6.0 g��������Ʒ(��Ҫ�ɷ�ΪAl2O3,��Fe2O3����)������100 mLϡ�����У���ַ�Ӧ������Һ�м���10 mol��L��1NaOH��Һ�����������������ͼ���NaOH��Һ���֮��Ĺ�ϵ��ͼ��ʾ���������������ʵ���Ũ��Ϊ�� ��

A. 3.50 mol��L��1
B. 1.75 mol��L��1
C. 0.85 mol��L��1
D. ��ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����ģ������ӵ绯ѧ������������������ˮ��������狀�ȥ����ˮ���Ƴɳ�ʼ��ģ���ˮ������NaCl������Һ��������Ũ�ȣ���ͼ��ʾ����ģ��ʵ�顣
��1��������ӦʽΪ___��
��2��ȥ��NH4+�����ӷ�Ӧ����ʽΪ___��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ͼ��װ��ģ�ҵ������ȡ��������ƣ��г������ͼ���������ʡ�ԣ����䷴Ӧԭ��Ϊ2Na2S+Na2CO3+4SO2![]() 3Na2S2O3+CO2
3Na2S2O3+CO2

��ش�
��1������˵������ȷ����___��
A��װ��A����ƿ�е��Լ�Ӧ��Na2SO3����
B�����C��ˮԡ���ȵ��¶ȣ��ܼӿ췴Ӧ���ʣ�ͬʱҲ������ԭ�ϵ�������
C��װ��E����Ҫ����������CO2β��
D��װ��B������֮һ�ǹ۲�SO2���������ʣ��ô���ƿ�п�ѡ��Ũ�����NaHSO3��Һ
��2����Ӧ������C����Һ�лẬ������Na2SO4���ʣ������������ԭ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס�����ͬѧ�ֱ���������̽��ʵ�顣
(1)����̽��![]() ��
��![]() ��Һ��Ӧ��ʵ��װ�����£�
��Һ��Ӧ��ʵ��װ�����£�
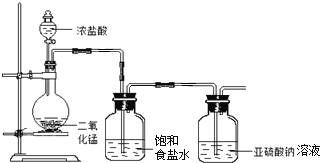
����ָ����װ�õIJ���֮�� ______ �� ______ ��
��![]() ��
��![]() ��Һ��Ӧ�����ӷ���ʽΪ ______ ��
��Һ��Ӧ�����ӷ���ʽΪ ______ ��
�����ʵ�飬����ʵ�鲽�裬֤��ϴ��ƿ�е�![]() �ѱ����� ______ ��
�ѱ����� ______ ��
(2)����̽����������![]() �е�
�е�![]() �ڲ�ͬ�¶ȡ���ͬŨ��NaOH��Һ�е�ˮ�����ʡ�ȡ��֧��С��ͬ���Թܣ����Թ������������̶�ֽ�����±����ж���ʵ�顣�����ֲ�ͬ�¶ȵ�ˮԡ�м�����ͬʱ���¼����������ȷ��ˮ�ⷴӦ������
�ڲ�ͬ�¶ȡ���ͬŨ��NaOH��Һ�е�ˮ�����ʡ�ȡ��֧��С��ͬ���Թܣ����Թ������������̶�ֽ�����±����ж���ʵ�顣�����ֲ�ͬ�¶ȵ�ˮԡ�м�����ͬʱ���¼����������ȷ��ˮ�ⷴӦ������
�Թܢ� | �Թܢ� | �Թܢ� | �Թܢ� | |
�������� | 1 | V1 | V2 | V3 |
| V4 | 3 | 0 | V5 |
����ˮ | 0 | V6 | 5 | 2 |
��������ϱ�������![]() ______ ��
______ ��![]() ______ ��
______ ��![]() ______ ��
______ ��
��ʵ���У����ñ���ʳ��ˮ�������ˮ�����ŵ��� ______ ���������ñ���![]() ��Һ�������ˮ����ԭ���� ______ ��
��Һ�������ˮ����ԭ���� ______ ��
��ʵ���У��Թܢ����Թܢ��е�������ٸ��죬��ԭ���У��¶ȸ����ʿ죬�������� ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ��W��X��Y��Z��ԭ�������������ӣ��Ҿ�������20��W��X��Z������֮��Ϊ10��Y��ԭ�Ӱ뾶��ͬ��������Ԫ������С��W��Z�γɵĻ����ﳣ���¿��뱥��NaCl��Һ��Ӧ�����������峣�����и�ͺ��ӽ���������˵���������

A. X�ĵ��������ཫ̫����ת��Ϊ���ܵij��ò���
B. YԪ�ؿ����γɶ��ֺ�����
C. XԪ������Ȼ����ֻ�л���̬û������̬
D. W��Z�γɵĻ������뱥��NaCl��Һ�ķ�ӦҪѡ������ͼװ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com