
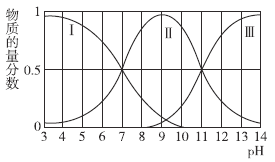
【题目】常温下,向二元弱酸H2A溶液中滴加NaOH溶液,不同pH时,相关微粒的物质的量分数如图所示,下列说法正确的是( )
A.pH=7时,溶液中c(Na+)=c(H2A)
B.pH=9时,c(OH-)=c(H2A)+c(H+)
C.pH=3和pH=11时,溶液中水的电离程度完全相同
D.H2A的一级电离常数和二级电离常数相差2个数量级
【答案】A
【解析】
A.由图分析知I代表H2A,Ⅱ代表HA-,Ⅲ代表A2-,根据电荷守恒:2c(A2-)+c(HA- )+c(OH-)=c(Na+)+c(H+),pH=7时,c(A2-)=0,c(HA-)=c(H2A)可知c(Na+)=(H2A),故A正确;
B.pH=9时,为NaHA溶液,根据物料守恒和电荷守恒可知c(A2-)+c(OH-)=c(H2A)+c(H+),故B错误;
C.pH=3时溶液中的溶质主要为H2A,水的电离被抑制,pH=11时溶液中的溶质为NaHA和Na2A,溶液显碱性,促进水的电离,故C错误;
D.H2A的一级电离常数为10-7,H2A的二级电离常数为10-11,H2A的一级电离常数和二级电离常数相差4个数量级,故D错误;
故选A。


科目:高中化学 来源: 题型:
【题目】化合物H是一种用于合成γ分泌调节剂的药物中间体,其合成路线流程图如下:
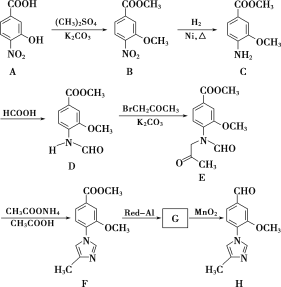
(1)C中的非含氧官能团名称为______。
(2)D→E 的反应类型为___________。
(3)写出A的一种羧酸同系物的结构简式: ____________。
(4)写出同时满足下列条件的![]() 的一种同分异构体的结构简式:_________。
的一种同分异构体的结构简式:_________。
①含有苯环,且苯环上只有2种不同化学环境的氢;
②属于α-氨基酸,且分子中有一个手性碳原子。
(5)G的分子式为C12H14N2O2 ,经氧化得到H,写出G的结构简式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】读下列药品标签,有关分析不正确的是( )
选项 | A | B | C | D |
物品标签 | 饱和氯水1.01×105 Pa,20 ℃ | 药品:×××
| 碳酸氢钠NaHCO3俗名小苏打(84 g·mol-1) | 浓硫酸H2SO4 密度1.84 g·mL-1浓度98.0% |
分析 | 该试剂应装在橡胶塞的细口瓶中 | 该药品不能与皮肤直接接触 | 该物质受热易分解 | 该药品标签上还标有
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化六氨合钴[Co(NH3)6]Cl3 是橙黄色、微溶于水的配合物,是合成其它一些含钴配合物的原料。下图是某科研小组以含钴废料(含少量Fe、Al 等杂质)制取[Co(NH3)6]Cl3 的工艺流程:
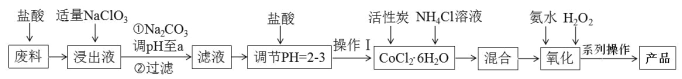
回答下列问题:
(1)写出加“适量NaClO3”发生反应的离子方程式______________。
(2)“加Na2CO3 调pH至a”会生成两种沉淀,分别为_______________________(填化学式)。
(3)操作Ⅰ的步骤包括_____________________________、冷却结晶、减压过滤。
(4)流程中NH4Cl除作反应物外,还可防止加氨水时c(OH-) 过大,其原理是_________________。
(5)“氧化”步骤,甲同学认为应先加入氨水再加入H2O2,乙同学认为试剂添加顺序对产物无影响。你认为___________(填“甲”或“乙”)同学观点正确,理由是_________________________________。写出该步骤的化学方程式:________________________________
(6)通过碘量法可测定产品中钴的含量。将 [Co(NH3)6]Cl3 转化成Co3+后,加入过量KI 溶液,再用Na2S2O3标准液滴定(淀粉溶液做指示剂),反应原理:2Co3++2I-=2Co2++I2,I2+2S2O32-=2I-+S4O62-,实验过程中,下列操作会导致所测钴含量数值偏高的是_______。
a.用久置于空气中的 KI 固体配制溶液
b.盛装Na2S2O3标准液的碱式滴定管未润洗
c.滴定结束后,发现滴定管内有气泡
d.溶液蓝色退去,立即读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g),反应进行到10 s末达到平衡,此时测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+2D(g),反应进行到10 s末达到平衡,此时测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为________。
(2)10 s末,生成物D的浓度为________。
(3)A与B的平衡转化率之比为________。
(4)反应过程中容器内气体的平均相对分子质量变化是_____(填“增大”、“减小”或“不变”,下同),气体的密度变化是______。
(5)在一定温度下,体积不变的密闭容器中,上述反应达到平衡的标志是_______(填字母)。
A. 气体总质量保持不变 B. A、B、C、D的浓度都相等
C. 每消耗3 mol A的同时生成2 mol D D. A、B、C、D的分子数之比为3∶1∶2∶2
E. 3V正(A) = 2V逆(C) F. A的转化率保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锌是制造锌钡白和锌盐的主要原料,也可用于湿法电解制锌,如图为由锌灰制ZnSO4·7H2O晶体的工艺流程。

已知:
①锌灰的主要成分为ZnO,还含有CuO、PbO、MnO和FeO;
②“滤渣2”的主要成分为Fe(OH)3和MnO(OH)2。
请回答下列问题:
(1)MnO(OH)2中Mn元素的化合价为___。
(2)为提高浸出效率,锌灰在“酸浸”前可采取的措施有___;“酸浸”时,若硫酸浓度过高,可能发生副反应的化学方程式为___。
(3)“滤渣1”的主要成分为___。
(4)“氧化”时,需控制溶液的pH=5.1,Fe2+被氧化的离子方程式为___。
(5)操作a为___、过滤、洗涤、干燥。
(6)ZnSO4·7H2O产品的纯度可用配位滴定法测定。
准确称取一定量的ZnSO4·7H2O晶体加入250mL的锥形瓶中,加水约20mL,再加入2-3滴5%的二甲酚橙作指示剂、约5mL六亚甲基四胺缓冲溶液,摇匀。用已标定的0.0160mol·L-1EDTA溶液滴定,滴定至溶液由红紫色变成亮黄色,即为终点(ZnSO4·7H2O与EDTA按物质的量之比1:1反应)。实验数据如下表:

ZnSO4·7H2O产品的纯度为___ (保留2位有效数字)。
(7)工业上采用惰性电极作阳极电解ZnSO4溶液可实现湿法炼锌,电解过程中的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸罗匹尼罗用于治疗帕金森症,治疗中度到重度的不宁腿(多动腿)综合症,罗匹尼罗(H)的一种合成路线如图所示。
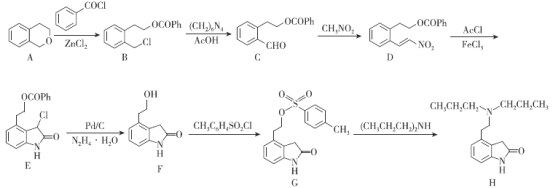
已知:①路线中Ph-代表![]() ,Ac-代表CH3COO-;
,Ac-代表CH3COO-;
②RCOOR’![]() R’OH
R’OH
请回答下列问题:
(1)D中含氧官能团的名称为___。
(2)E的分子式为___;一定条件下,1molE最多与___molH2发生加成反应(不考虑开环加成)。
(3)G→H的反应类型为___。
(4)A→B的化学方程式为___。
(5)同时满足下列条件的A的同分异构体有___种(不考虑立体异构);
①含苯环②遇FeCl3溶液显紫色③有两个取代基
其中核磁共振氢谱为5组峰且峰面积之比为4:2:2:1:1的结构简式为___。
(6)参照上述合成路线,请设计以![]() 为起始原料制备
为起始原料制备![]() 的合成路线为___(其他无机试剂任选)。
的合成路线为___(其他无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应X2(g)+Y2(g)![]() 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.2 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.2 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
A. Z为0.2 mol·L-1 B. Y2为0.35 mol·L-1
C. X2为0.3 mol·L-1 D. Z为0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,固定容积的容器中可逆反应A(g)+ 3B(g) ![]() 2C(g)未达到平衡状态的是
2C(g)未达到平衡状态的是
A.B的生成速率与B的分解速率相等B.容器内压强不再发生变化
C.单位时间生成nmol A消耗2nmolCD.混合气体的平均摩尔质量是一个定值
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com