
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g),反应进行到10 s末达到平衡,此时测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+2D(g),反应进行到10 s末达到平衡,此时测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为________。
(2)10 s末,生成物D的浓度为________。
(3)A与B的平衡转化率之比为________。
(4)反应过程中容器内气体的平均相对分子质量变化是_____(填“增大”、“减小”或“不变”,下同),气体的密度变化是______。
(5)在一定温度下,体积不变的密闭容器中,上述反应达到平衡的标志是_______(填字母)。
A. 气体总质量保持不变 B. A、B、C、D的浓度都相等
C. 每消耗3 mol A的同时生成2 mol D D. A、B、C、D的分子数之比为3∶1∶2∶2
E. 3V正(A) = 2V逆(C) F. A的转化率保持不变
【答案】0.04 mol·L-1·s-1 0.4 mol·L-1 1∶1 不变 不变 F
【解析】
(1)依据化学反应速率的基本定义式作答;
(2)依据生成D的物质的量进行计算;
(3)依据转化率的定义结合题意分析作答;
(4)混合气体的质量和物质的量、容器的体积均不变化;
(5)根据平衡状态判断的标志作答;
(1)![]() =
=![]() =0.04 mol·L-1·s-1;
=0.04 mol·L-1·s-1;
(2)根据方程式可知,10s末,生成物D的物质的量与C的物质的量相等,为0.8mol,则10s末,生成物D的浓度为![]() = =0.4mol/L;
= =0.4mol/L;
(3)平衡转化率等于转化量与初始量的比值,因平衡时A与B的物质的量之比等于1.8mol:0.6mol=3:1,转化量之比等于化学计量数之比也等于3:1,则平衡转化率之比:![]() =1:1;
=1:1;
(4)反应过程中容器内气体的总质量保持不变,总的物质的量保持不变,则平均相对分子质量不变,又是在固定容积为2 L的密闭容器中进行,则气体的体积保持不变,即气体的密度不变;
(5)由反应3A(g)+B(g)![]() 2C(g)+2D(g)可知:
2C(g)+2D(g)可知:
A.气体总质量始终保持不变,不能说明反应达到平衡状态,A项错误;
B. A、B、C、D的浓度都相等,不能说明浓度保持不变,则不能说明反应达到平衡状态,B项错误;
C. 每消耗3 mol A的同时生成2 mol D,均表示的正反应方向,C项错误;
D.A、B、C、D的分子数之比为3∶1∶2∶2,不能说明反应的物质的量保持不变,D项错误;
E. 2V正(A) =3 V逆(C),说明正反应速率等于逆反应速率,反应已经达到平衡状态,但题中的定量关系不能说明反应达到平衡状态,E项错误;
F. A的转化率保持不变,说明反应达到平衡状态,F项正确;
答案选F。


 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】硅及其化合物在材料领域中的应用广泛.下列叙述不正确的是( )
A. 硅单质可用来制造太阳能电池
B. 二氧化硅是制造光导纤维的材料
C. 石英(SiO2)可用来制作工艺品
D. 硅单质是制造玻璃的主要原料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】周期表前四周期的元素A、B、C、D、E、F,原子序数依次增大,A是周期表中原子半径最小的元素,B的基态原子中只有1个未成对电子,C基态原子中有7种不同运动状态的电子,D的最外层电子数是其所处周期数的3倍,E与D同主族,F的一价阳离子最外层有18个电子。回答下列问题:
(1)F在周期表中的位置是_____________,它的基态原子的电子排布式为_____________
(2)A元素与其他元素形成的含氧酸中,酸根呈三角锥结构的酸是_________,该酸的中心原子的杂化方式为_________
(3)CA3极易溶于水,试从下图中判断CA3溶于水后形成CA3·H2O的合理结构为_____(填字母代号),推理依据是___________

(4)元素B可形成H3BO3,已知H3BO3的电离方程式为H3BO3+2 H2O![]() [B(OH)4]一+H3O+
[B(OH)4]一+H3O+
①基态B、D原子的第一电离能由小到大的顺序为__________(用元素符号表示)
②[B(OH)4]一中B原子的杂化类型为_______________
③写出一种与H3O+互为等电子体的分子的化学式:___________
④H3BO3晶体在热水中的溶解度大于冷水中的溶解度的原因为__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
①化石燃料在任何条件下都能充分燃烧
②化石燃料在燃烧过程中能产生污染环境的CO、SO2 等有害气体
③直接燃烧煤不如将煤进行深加工后再燃烧效果好
④固体煤变为气体燃料后,燃烧效率将更低
A.①④B.②③④C.②③D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn (s、白)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH1
②Sn (s、灰)+2HCl (aq)=SnCl2 (aq)+H2 (g);DH2
③Sn (s、灰)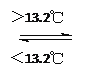 Sn (s、白);DH3=+2.1 kJ/mol
Sn (s、白);DH3=+2.1 kJ/mol
下列说法正确的是( )
A. DH1>DH2
B. 锡在常温下以灰锡状态存在
C. 灰锡转化为白锡的反应是放热反应
D. 锡制器皿长期处于低于13.2 ℃的环境中,会自行毁坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种气体,取X和Y按物质的量之比1∶1混合,放入某密闭容器中发生反应X+2Y![]() 2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于
2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于
A. 33% B. 40% C. 50% D. 65%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物I是治疗制揽伤的药物,合成I的--种路线如下:
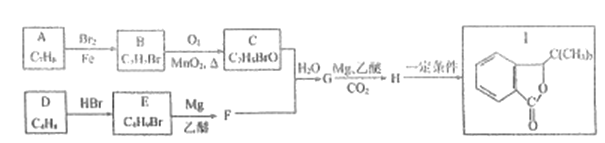
已知:
①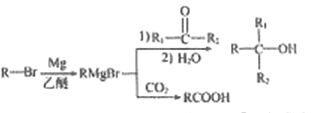
②E的核磁共振氢谱只有1组峰
③C能发生银镜反应。
请回答下列问题:
(1)有机物C的结构简式________,D的化学名称________。
(2)C中所含官能团的名称为__________.
(3)H![]() I的化学方程式为_______,其反应类型为_____。
I的化学方程式为_______,其反应类型为_____。
(4)X与B含有相同的官能团,相对分子质量比B大14,X的结构有______种,其中核磁共振氢谱有4组峰,且峰面积之比为2:2:3:3的有________ (写结构简式)。
(5)写出用乙烯为原料制备化合物 (丁二酸二乙酯)的合成路线_______ (其他无机试剂任选)。
(丁二酸二乙酯)的合成路线_______ (其他无机试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com