
����Ŀ�����Ȼ���������[Co(NH3)6]Cl3 �dzȻ�ɫ������ˮ�������Ǻϳ�����һЩ����������ԭ�ϡ���ͼ��ij����С���Ժ��ܷ��ϣ�������Fe��Al �����ʣ���ȡ[Co(NH3)6]Cl3 �Ĺ������̣�
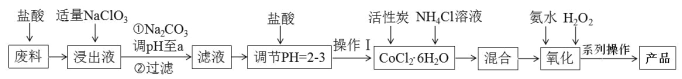
�ش��������⣺
��1��д���ӡ�����NaClO3��������Ӧ�����ӷ���ʽ______________��
��2������Na2CO3 ��pH��a�����������ֳ������ֱ�Ϊ_______________________���ѧʽ����
��3��������IJ������_____________________________����ȴ�ᾧ����ѹ���ˡ�
��4��������NH4Cl������Ӧ���⣬���ɷ�ֹ�Ӱ�ˮʱc(OH��) ������ԭ����_________________��
��5�������������裬��ͬѧ��ΪӦ�ȼ��백ˮ�ټ���H2O2����ͬѧ��Ϊ�Լ�����˳��Բ�����Ӱ�졣����Ϊ___________����ס����ҡ���ͬѧ�۵���ȷ��������_________________________________��д���ò���Ļ�ѧ����ʽ��________________________________
��6��ͨ���������ɲⶨ��Ʒ���ܵĺ������� [Co(NH3)6]Cl3 ת����Co3���������KI ��Һ������Na2S2O3��Һ�ζ�(������Һ��ָʾ��)����Ӧԭ����2Co3����2I����2Co2����I2��I2��2S2O32����2I����S4O62����ʵ������У����в����ᵼ�������ܺ�����ֵƫ�ߵ���_______��
a���þ����ڿ����е� KI ����������Һ
b��ʢװNa2S2O3��Һ�ļ�ʽ�ζ���δ��ϴ
c���ζ��������ֵζ�����������
d����Һ��ɫ��ȥ����������
���𰸡�6Fe2����ClO3����6H��=6Fe3����Cl����3H2O Fe(OH)3 �� Al(OH)3 HCl��Χ������Ũ�� NH4Cl����ˮ�����NH4�������ƺ��ڼ����NH3��H2O�ĵ��� �� ��ֹCo(OH)3������ H2O2��2CoCl2��2NH4Cl��10NH3��H2O��2Co(NH3)6Cl3����12H2O ab
��������
�Ժ��ܷ��ϣ�������Fe��Al �����ʣ���ȡ[Co(NH3)6]Cl3 ���������ܽ���ϣ��õ�Co2+��Fe2+��Al3+��������Һ������������NaClO3��������������Ϊ�����ӣ��ټ���̼���Ƶ���pH�����������ӡ�������Ϊ�����������������������ˣ��õ���Һ������Co2+����Һ�м����������pH=2-3,�������̿���Ȼ����Һ�õ�CoCl2 6H2O�������μ��백ˮ�������⣬������ӦH2O2��2CoCl2��2NH4Cl��10NH3��H2O��2Co(NH3)6Cl3����12H2O���ٽ��������Ȼ����Ϊ������Ũ������ȴ�ᾧ����ѹ���˵õ���Ʒ���ݴ˷�������
(1)������NaClO3��Ŀ���ǽ�������������Ϊ�����ӣ����������ӷ�ӦΪ6Fe2����ClO3����6H��=6Fe3����Cl����3H2O��
(2)����̼���Ƶ���pH�����������Ӻ������ӣ�ת��ΪFe(OH)3 �� Al(OH)3��
(3)����ֹ��Ʒˮ�⣬��Ӧ��HCl��Χ������Ũ����
(4)�������Ȼ�麟���Ϊ��Ӧ���⣬NH4Cl����ˮ�����NH4�������ƺ��ڼ����NH3��H2O�ĵ��룬�ɷ�ֹ�Ӱ�ˮʱ����������Ũ�ȹ���
(5)���ȼ���������⣬����Ԫ��������Co3+������백ˮ���������������ܣ������ڲ�Ʒ�����ɣ��ʼ�ͬѧ��ȷ���ȼ��백ˮ�ټ���������⣬�ɷ�ֹCo(OH)3�����ɣ���ʱ�ķ�ӦΪH2O2��2CoCl2��2NH4Cl��10NH3��H2O��2Co(NH3)6Cl3����12H2O��
(6) a���þ����ڿ����е� KI ����������Һ���⻯�ز��ֱ�����Ϊ�ⵥ�ʣ��ζ�ʱ���ĵ���������Ʊ����࣬�ⶨ���ƫ�ߣ�����ȷ��
b��ʢװNa2S2O3��Һ�ļ�ʽ�ζ���δ��ϴ�����Ҳ��ϡ�ͣ��ζ�ʱ���ĵ���������Ʊ�Ҳ������࣬�ⶨ���ƫ�ߣ�����ȷ��
c���ζ��������ֵζ����������ݣ�����ռ����������ĵ���������Ʊ�Һ�������ƫС���ⶨ���ƫ�ͣ��ʴ���
d����Һ��ɫ��ȥ��������������ʱ��Һ��ϲ������ⵥ�ʲ�δ��ȫ����Һ��Ӧ��ȫ���������ĵı�Һ���٣��ⶨ���ƫ�ͣ��ʴ���ѡab��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�ַ�����ά������ǿ�ȱȸ�˿�������㷺�����������ϡ���ṹƬ������ͼ
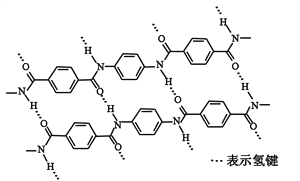
���й��ڸø߷��ӵ�˵����ȷ����
A. ��ȫˮ�����ĵ����������������ϵ���ԭ�Ӿ��в�ͬ�Ļ�ѧ����
B. ��ȫˮ�����ĵ��������������й������DCOOH���DNH2
C. ����Ըø߷��ӵ�����û��Ӱ��
D. �ṹ��ʽΪ��![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ�����ӵ�������ֵ������������ȷ����(����)
A. 1 mol����һ�������·ֱ������������������ȫ��Ӧת�Ƶ�������Ϊ2NA
B. 30 g�����Ǻͱ�����Ļ�����к��е���ԭ����Ϊ4NA
C. 12 gʯīϩ(����ʯī)�к�����Ԫ���ĸ���Ϊ2NA
D. 2.1 g DTO�к��е�������ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ú���еĵ�Ԫ����ʹ�ù����е�ת����ϵ��ͼ��ʾ��

(1)����NH3���뷴Ӧ�Ļ�ѧ����ʽΪ_______��
(2)��̿������һ�ֳ����ĺ����л������(![]() )������������ڵ�C��Nԭ����ȣ�Nԭ����������������___________(����ǿ����������)����ԭ�ӽṹ�ǶȽ���ԭ��________��
)������������ڵ�C��Nԭ����ȣ�Nԭ����������������___________(����ǿ����������)����ԭ�ӽṹ�ǶȽ���ԭ��________��
(3)��ҵ�ϳɰ����˹��̵�����Ҫ������2007�껯ѧ�Ҹ���������ض�֤ʵ�������뵪���ڹ����������ϳɰ��ķ�Ӧ���̣�ʾ����ͼ��
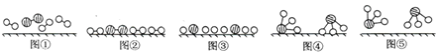
����˵����ȷ����________(ѡ����ĸ)��
a. ͼ�ٱ�ʾN2��H2�����о��ǵ���
b. ͼ����ͼ����Ҫ��������
c. �ù��̱�ʾ�˻�ѧ�仯�а����ɻ�ѧ���Ķ��Ѻ��»�ѧ��������
(4)��֪��N2(g) �� O2(g) = 2NO(g) ��H = a kJ��mol-1
N2(g) �� 3H2(g) = 2NH3(g) ��H = b kJ��mol-1
2H2(g) �� O2(g) = 2H2O(l) ��H = c kJ��mol-1
��Ӧ��ָ������³�ѹ������NH3���뷴Ӧ���Ȼ�ѧ����ʽΪ________��
(5)�ü�ӵ绯ѧ����ȥNO�Ĺ��̣���ͼ��ʾ��

����֪���ص�����������Һ��pH��4~7֮�䣬д�������ĵ缫��Ӧʽ��________��
�������ӷ���ʽ��ʾ���ճ��г�ȥNO��ԭ����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ��� ����
A. 1 mol H2O���е�������Ϊ10 mol
B. 0.5 mol SO42-��8 mol����
C. 18 gˮ�к��е���ԭ����Ϊ6.02��1022
D. 1 mol NaHSO4�����к��е�������������Ϊ3��6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҿ����û�������������Ӧ�Ʊ�����ͪ����Ӧԭ����ʵ��װ��(���ּг�װ����)��ͼ��
![]()
![]()
![]()
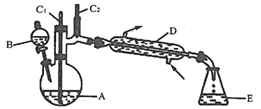
�й����ʵ��������ʼ�����
���� | �е�(��) | �ܶ�(g��cm3��20��) | �ܽ��� |
������ | 161.1(97.8)* | 0.96 | ������ˮ���� |
����ͪ | 155.6(95.0)* | 0.95 | ����ˮ���������� |
ˮ | 100.0 | 1.0 |
*�����е����ݱ�ʾ���л�����ˮ�γɵľ��й̶���ɵĻ����ķе㡣
ʵ��ͨ��װ��B������Na2Cr2O7��Һ�ӵ�ʢ��10mL��������A�У�55��60����з�Ӧ����Ӧ��ɺ�������ˮ�������ռ�95��100�����֣��õ���Ҫ������ͪ��Ʒ��ˮ�Ļ���
(1)װ��D������Ϊ___________��
(2)����Na2Cr2O7��Һ������������Ӧ��H��0����Ӧ���ҽ�������ϵ�¶�Ѹ������������Ӧ���ࡣ
�ٵμ�����Na2Cr2O7��Һʱ��Ӧ�����ӷ���ʽ__________��
�������ܷ��뻷��ͪ��ˮ��ԭ����____________��
(3)����ͪ���ᴿ��Ҫ��������һϵ�еIJ�����
a.����ȥ���Ѻ��ռ�151��156�����
b.ˮ��������(���ѷе�34.6�棬��ȼ��)��ȡ����ȡҺ�����л���
c.����
d.��Һ���м���NaCl���������ͣ����ã���Һ
e.������ˮMgSO4���壬��ȥ�л�����������ˮ
�������ᴿ�������ȷ˳����_____________��
��b��ˮ����������ȡ��Ŀ����___________��
����������c��d��ʹ�õIJ����������ձ�����ƿ���������⣬����Ҫ�IJ���������_______������d�У�����NaCl�����������____________��
(4)�ָ�������ʱ������õ�����Ʒ���Ϊ6mL������ͪ�IJ���____________��(��������ȷ��0.1%)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����Ԫ����H2A��Һ�еμ�NaOH��Һ����ͬpHʱ������������ʵ���������ͼ��ʾ������˵����ȷ���ǣ� ��
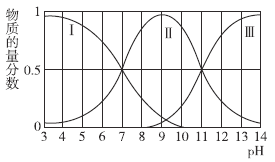
A.pH=7ʱ����Һ��c(Na��)=c(H2A)
B.pH=9ʱ��c(OH-)=c(H2A)��c(H��)
C.pH=3��pH=11ʱ����Һ��ˮ�ĵ���̶���ȫ��ͬ
D.H2A��һ�����볣���Ͷ������볣�����2��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X(g)+3Y(g)![]() 2Z(g) ��H=-akJ��mol-1��һ�������£���1molX��3molYͨ��2L�ĺ����ܱ������У���Ӧ10min�����Y�����ʵ���Ϊ2.4mol������˵����ȷ����
2Z(g) ��H=-akJ��mol-1��һ�������£���1molX��3molYͨ��2L�ĺ����ܱ������У���Ӧ10min�����Y�����ʵ���Ϊ2.4mol������˵����ȷ����
A.10min�ڣ�Y��ƽ����Ӧ����Ϊ0.03mol��L-1��s-1
B.��10minʱ��X�ķ�Ӧ����Ϊ0.01mol��L-1��min-1
C.10min�ڣ�����0.2molX������0.4molZ
D.10min�ڣ�X��Y��Ӧ�ų�������ΪakJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪NH4NO3�ķֽ�������¶��йأ�
NH4NO3![]() NH3��+HNO3����
NH3��+HNO3����
NH4NO3![]() N2O��+2H2O����
N2O��+2H2O����
2NH4NO3![]() 2N2��+O2��+4X����
2N2��+O2��+4X����
4NH4NO3![]() 3N2��+2NO2��+8H2O����
3N2��+2NO2��+8H2O����
����˵���������
A.�ĸ���Ӧ����������������ԭ��Ӧ
B.��Ӧ�����û���������Է���������26.7
C.��Ӧ����X�Ļ�ѧʽ��H2O
D.��Ӧ�ܵ�����������N2����ԭ������NO2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com