
【题目】物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液的体积比为3:2:1时,三种溶液中Cl-的物质的量浓度之比为( )
A. 1:1:1 B. 1:2:3 C. 3:2:1 D. 3:4:3
科目:高中化学 来源: 题型:
【题目】下列溶液中有关物质的浓度关系正确的是( )
A.c(NH ![]() )相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl)
)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液:c(NH4HSO4)>c[(NH4)2SO4]>c(NH4Cl)
B.等物质的量的NaClO、NaHCO3混合溶液:c(HClO)+c(ClO﹣)=c(HCO ![]() )+c(H2CO3)+c(CO
)+c(H2CO3)+c(CO ![]() )
)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO﹣)>c(H+)>c(OH﹣)
D.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH﹣)+c(HA﹣)+c(A2﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表对某些反应方程式的评价合理的是( )
编号 | 离子方程式或电极反应式 | 评价 | |
A | 次氯酸钙溶液中通入足量SO2 | Ca2++ClO﹣+SO2+H2O=CaSO4+Cl﹣+2H+ | 正确 |
B | 硫酸铁溶液与氢氧化钡溶液混合 | Fe3++SO | 正确 |
C | 醋酸铵溶于水 | CH3COO﹣+NH | 错误,阴离子水解相互促进,应该用“=”号 |
D | 用惰性电极电解氯化铜和氯化钠的混合溶液一段时间 | 阴极:2Cu2++4e﹣=2Cu | 错误,该阴阳两极反应不可能同时发生 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组拟制备氯气并验证其一系列性质.Ⅰ.【查阅资料】
①当溴水浓度较小时,溶液颜色与氯水相似也呈黄色.
②硫代硫酸钠溶液在工业上可作为脱氯剂.
(1)Ⅱ.【性质验证】实验装置如图1所示(省略夹持装置)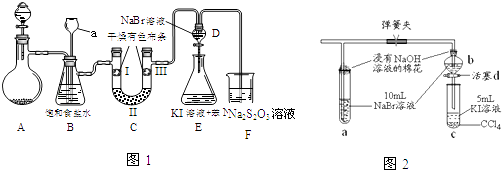
实验步骤:
a.检查装置气密性,按图2加入试剂.仪器a的名称是;装置CⅡ处加的试剂可以是(选填下列字母编号).
A.碱石灰 B.硅胶 C.浓硫酸 D.无水氯化钙
b.装置B的作用有 .
c.写出装置F中相应的离子反应方程式: .
(2)Ⅲ.【探究与反思】a.图1中设计装置D、E的目的是比较氯、溴、碘的非金属性,有同学认为该设计不能达到实验目的,其理由是 . 该组的同学思考后将上述D、E、F装置改为实验操作步骤如下:
①打开弹簧夹,缓缓通入氯气
②当a和b中的溶液都变为黄色时,夹紧弹簧夹.
③当a中溶液由黄色变为棕色时,停止通氯气.
④ .
b.设计步骤③的实验思想是 .
c.步骤④的操作是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国明代《本草纲目》中收载药物1892种,其中“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”这里所用的“法”是指( )
A. 萃取 B. 渗析 C. 蒸馏 D. 分液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在平板电视显示屏生产过程中产生的大量废玻璃粉末中含有二氧化铈(CeO2).
(1)①煅烧Ce(OH)CO3可制备CeO2 , 配平该反应的化学方程式Ce(OH)CO3+O2=CeO2+CO2+H2O
②已知在一定条件下,电解熔融状态的CeO2可制备Ce,在阴极获得铈,写出阴极的电极反应式;
(2)某课题组以上述废玻璃粉末(含有SiO2、Fe2O3、CeO2以及其他少量不溶于稀酸的物质)为原料,设计如图1流程对资源进行回收,得到Ce(OH)4和硫酸铁铵.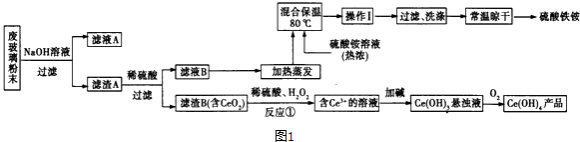
①得到滤渣B时,需要将其表面杂质洗涤干净.检验滤渣B已经洗涤干净的方法是 .
②反应①的离子方程式为 .
③如图2,氧化还原滴定法测定制得的Ce(OH)4产品的纯度.
该产品中Ce(OH)4的质量分数为(保留小数点后两位).若滴定所用FeSO4溶液已在空气中露置了一段时间,则测得该Ce(OH)4产品的纯度(“偏高”、“偏低”或“无影响”).
(3)操作I的名称是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的选项正确的是( )
A.配制0.10molL﹣1NaOH溶液 | B.除去CO中的CO2 | C.苯萃取碘水中I2 , 分出水层后的操作 | D.记录滴定终点读数为12.20mL |
|
|
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】成环是有机合成的重要环节.如反应①化合物(Ⅰ)可由(Ⅲ)合成: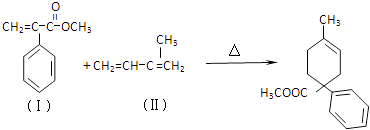
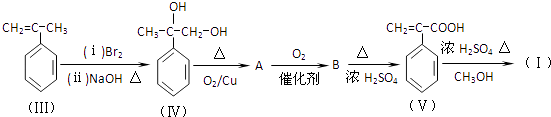
(1)(Ⅰ)的分子式为 , 1mol(Ⅰ)最多能与molH2发生加成反应.
(2)写出(Ⅳ)→A的化学方程式 .
(3)酸性条件下,化合物B能发生聚合反应,化学方程式为 .
(4)化合物B→(Ⅴ)的反应类型为 .
(5)(Ⅲ)与(Ⅱ)也能发生类似反应①的反应,生成含两个六元环的化合物的结构简式为(任写一种)
(6)下列物质与(Ⅴ)互为同分异构体的是(填序号)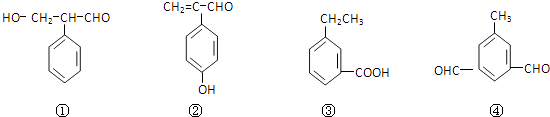
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天津港爆炸致大量氰化钠(NaCN)泄露,NaCN是剧毒物质.专家们使用双氧水(H2O2)来处理氰化钠,反应方程式如下:H2O2+NaCN+H2O═NaHCO3+NH3
(1)若有0.49吨 NaCN泄露至少需要质量分数为34%的H2O2溶液吨进行处理 (假设H2O2的处理效果是100%,且不考虑H2O2自身分解)
(2)相比于双氧水,漂白粉(主要成分Ca(ClO)2)的价格要便宜的多,若处理相同质量的NaCN(生成物相同)需要消耗Ca(ClO)2mol(假设Ca(ClO)2的处理效果是100%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com