
【题目】钠离子电池开始成为下一轮电池研究的重点,下图是一种可充电钠离子电池![]() 电解质溶液
电解质溶液![]() 溶液
溶液![]() 工作示意图。下列说法正确的是
工作示意图。下列说法正确的是![]()

A.电池放电时,![]() 从a极区移动到b极区
从a极区移动到b极区
B.电池放电时,b极区发生的反应是![]()
C.金属钠可以作为该电池的负极材料
D.离子交换膜也可以改成阴离子交换膜
科目:高中化学 来源: 题型:
【题目】用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作不正确的是( )
A.酸式滴定管用蒸馏水洗净后,直接加入已知浓度的盐酸
B.锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液
C.滴定时,眼睛观察锥形瓶中溶液颜色的变化
D.读数时,视线与滴定管内液体的凹液面最低处保持水平
查看答案和解析>>
科目:高中化学 来源: 题型:
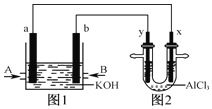
【题目】图1为甲烷和![]() 构成的燃料电池示意图,电解质为KOH溶液,图2为电解
构成的燃料电池示意图,电解质为KOH溶液,图2为电解![]() 溶液的装置,电极材料均为石墨.用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀.下列说法正确的是( )
溶液的装置,电极材料均为石墨.用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀.下列说法正确的是( )
A.图1中电解质溶液的pH增大
B.图2中电解![]() 溶液的总反应为
溶液的总反应为![]()
C.A处通入的气体为![]() ,电极反应式为
,电极反应式为![]()
D.电解池中![]() 向x极移动
向x极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
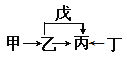
【题目】A、B、C、D、E、F是原子序数依次增大的短周期主族元素。E是同周期元素金属性最强的元素。甲、乙、丙、丁、戊是由上述部分元素中的两种或几种组成的化合物,它们的转化关系如图所示。其中甲是生活中的调味品,丁是淡黄色固体。下列说法不正确的是
A. 原子半径由大到小的顺序为:r(E)>r(F)>r(C)>r(D)
B. 元素F的氧化物的水物化的酸性一定比硫酸酸性强
C. 元素B的氢化物可能具有正四面体结构
D. 化合物A4BC2D既可能是共价化合物,也可是离子化合物
【答案】B
【解析】A、B、C、D、E、F是原子序数依次增大的短周期主族元素。E是同周期元素金属性最强的元素,则E为钠元素;根据流程图推导,且甲是生活中的调味品,丁是淡黄色固体,可知甲为氯化钠,丁为过氧化钠,则丙为碳酸钠,乙为氢氧化钠,戊是二氧化碳,则A、B、C、D、E、F分别为H、C、N、O、Na、Cl。A. 同周期性元素从左到右原子半径逐渐减小,同主族元素从上而下原子半径逐渐增大,故原子半径由大到小的顺序为:r(Na)>r(Cl)>r(N)>r(O),选项A正确;B. 元素Cl的最高价氧化物的水物化的酸性一定比硫酸酸性强,若不是最高价氧化物的水化物,则可能比较弱,如HClO是弱酸,选项B不正确;C. 元素B的氢化物CH4具有正四面体结构,选项C正确;D. 化合物A4BC2D既可能是共价化合物CO(NH2)2,也可是离子化合物NH4CNO,选项D正确。答案选B。
【题型】单选题
【结束】
6
【题目】下图所示装置可间接氧化工业废水中含氮离子(NH4+)。下列说法不正确的是

A. 乙是电能转变为化学能的装置
B. 含氮离子氧化时的离子方程式为:3Cl2 + 2NH4+=N2 + 6Cl-+8H+
C. 若生成H2和N2的物质的量之比为3:1,则处理后废水的pH减小
D. 电池工作时,甲池中的Na+移向Mg电极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氯苯的废水可通过加入适量乙酸钠,设计成微生物电池将氯苯转化为苯而除去,其原理如图所示。下列叙述正确的是
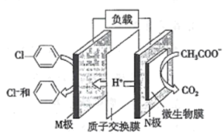
A.电子流向:N极→导线→M极→溶液→N极
B.M极的电极反应式为![]()
C.每生成lmlCO2,有3mole-发生转移
D.处理后的废水酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某公司生产的镁空气电池使用水作为电解液,其自带的LED灯可持续照明![]() ,这种镁空气电池可作为应急电源。工作原理可用如图表示,下列说法正确的是
,这种镁空气电池可作为应急电源。工作原理可用如图表示,下列说法正确的是

A.放电时,正极的电极反应式为![]()
B.放电过程中,电解液的pH逐渐增大
C.放电过程中,每消耗标准状况下![]() 空气,理论上转移4mol电子
空气,理论上转移4mol电子
D.此电池中的水可转换为非水体系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种新型电池放电时的总反应方程式为:![]() ,装置如图。下列说法正确的是
,装置如图。下列说法正确的是![]()

A.放电过程中![]() 通过膜向正极移动
通过膜向正极移动
B.右侧的电极反应式为:![]()
C.若M为Al,则电池放电过程的负极反应式为:![]()
D.在![]() 空气电池中,为防止负极区沉积
空气电池中,为防止负极区沉积![]() ,可改用稀硫酸做电解质溶液
,可改用稀硫酸做电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+3B(g)![]() 2C(g)+2D(g)在四种不同情况下的反应速率分别为:
2C(g)+2D(g)在四种不同情况下的反应速率分别为:
①v(A)=0.45mol/(Ls)
②v(B)=0.6mol/(L·s)
③v(C)==0.4mol/(L·s)
③v(D)=0.45mol/(Ls)
下列有关反应速率的比较中正确的是
A.④>③>②>①B.④<③=②<①C.①>②>③>④D.④>③=②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在4 L密闭容器中充入6 mol A气体和5 mol B气体,在一定条件下发生反应:3A(g)+B(g)![]() 2C(g)+xD(g),达到平衡时,生成了2 mol C,经测定,D的浓度为0.5 mol·L-1,下列判断正确的是( )。
2C(g)+xD(g),达到平衡时,生成了2 mol C,经测定,D的浓度为0.5 mol·L-1,下列判断正确的是( )。
A. x=1
B. B的转化率为20%
C. 平衡时A的浓度为1.50 mol·L-1
D. 达到平衡时,在相同温度下容器内混合气体的压强是反应前的85%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com