
高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是 
A铁是阳极,电极反应为Fe-6e一+4H2O=FeO42-+ 8H+
B电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极
C若隔膜为阴离子交换膜,则OH-自右向左移动
D电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:单选题
把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池。对该电池的描述合理的是①溶液中硫酸的物质的量浓度保持不变;②Cu极上有气泡产生,发生还原反应;③Cu为负极,Zn为正极;④原电池在工作时电子由负极通过溶液流向正极;⑤该装置将化学能转变为电能
| A.②⑤ | B.③⑤ | C.①② | D.④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y两根金属棒插入Z溶液中构成下图的装置,实验中电流表指针发生偏转,同时X棒变粗,Y棒变细,则X、Y、Z可能是下列中的( )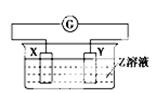
| 编号 | X | Y | Z |
| A | Zn | Cu | 稀硫酸 |
| B | Cu | Zn | 稀硫酸 |
| C | Cu | Ag | 硫酸铜溶液 |
| D | Ag | Zn | 硝酸银溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
图Ⅰ的目的是精炼铜,图Ⅱ的目的是保护钢闸门。下列说法不正确的是

| A.图Ⅰ中a为纯铜 |
| B.图Ⅰ中SO42—向b极移动 |
| C.图Ⅱ中如果a、b间连接电源,则a连接负极 |
| D.图Ⅱ中如果a、b间用导线连接,则X可以是铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
甲醇、氧气和强碱溶液做电解质的手机电池中的反应为:
2CH3OH+3O2+4OH-  2CO32-+6H2O,有关说法正确的是
2CO32-+6H2O,有关说法正确的是
| A.放电时,CH3OH参与反应的电极为正极 |
| B.放电时,负极电极反应:CH3OH+8OH--6e- =CO32-+6H2O |
| C.标况下,通入11.2LO2完全反应有1mol电子转移 |
| D.充电时电解质溶液的pH逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
太阳能电池板面对太阳时,一部分电能直接供给“天宫一号”,一部分电能则储存在电池里,供背离太阳时使用。“天宫一号”使用的是镍氢电池,电解质溶液显碱性。其反应方程式为: LaNi5+Ni(OH)2 LaNi5H+NiOOH。下列有关说法不正确的是
LaNi5H+NiOOH。下列有关说法不正确的是
| A.放电时镍被还原 | B.放电时负极LaNi5H+OH——e—=LaNi5+H2O |
| C.充电时OH—向阴极移动 | D.充电时每消耗lmol Ni(OH)2转移lmol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
利用太阳光分解水制氢是未来解决能源危机的理想方法之一。某研究小组设计了如图所示的循环系统实现光分解水制氢(a、b、c、d均为惰性电极)。反应过程中所需的电能由太阳能光电池提供,反应体系中I2 和Fe3+ 等可循环使用。下列说法正确的是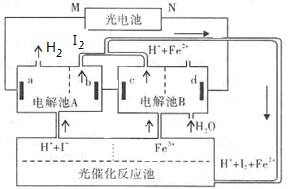
| A.电极M为光电池的正极 |
| B.d的电极反应式为2H2O + 4e- = 4H+ + O2↑ |
C.光催化反应池中反应的离子方程式为2Fe3++ 2I-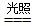 2Fe2+ + I2 2Fe2+ + I2 |
D.若循环系统处于稳定工作状态时,电解池A中流入和流出的HI浓度分别为a mol·L-1和b mol·L-1,光催化反应生成Fe3+ 的速率为c mol·min-1,则循环系统中溶液的流量为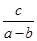 L·mol -1 L·mol -1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
据中国储能网讯2012年8月23日报道,锂离子电池常见的正极材料主要成分为LiCoO2,负极则是特殊分子结构的碳.电解质为能传导Li+的高分子材料,充电时,加在电池两极的电势迫使正极的化合物释出锂离子,嵌入负极分子排列呈片层结构的碳中,这种锂离子电池的电池反应为:Li(C)+LiCoO2 Li2CoO2,下列说法不正确的是
Li2CoO2,下列说法不正确的是
A.该电池属于二次电池
B.充电时LiCoO2既发生氧化反应又发生还原反应
C.填充在正负极之间的电解质,除了保持稳定,还需要具有良好导电性,减小电池内阻
D.放电过程中Li+向负极移动
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
设计如下装置探究HCl溶液中阴、阳离子在电场中的相对迁移速率(已知:Cd的金属活动性大于Cu)。恒温下,在垂直的玻璃细管内,先放CdCl2溶液及显色剂,然后小心放入HCl溶液,在aa'处形成清晰的界面。通电后,可观察到清晰界面缓缓向上移动。下列说法不正确的是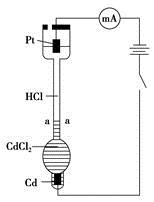
| A.通电后,可观察到清晰界面缓缓向上移动的原因是Cd2+向Pt电极迁移的结果 |
| B.装置中Pt电极附近的pH增大 |
| C.一定时间内,如果通过HCl溶液某一界面的总电量为5.0 C,测得H+所迁移的电量为4.1 C,说明该HCl溶液中H+的迁移速率约是Cl-的4.6倍 |
| D.如果电源正负极反接,则下端产生大量Cl2,使界面不再清晰,实验失败 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com