
【题目】常温下将盐酸溶液滴加到联氨(N2H4)的水溶液中,混合溶液中的微粒的物质的量分数δ(X)随-1g(OH-)变化的关系如图所示。下列叙述错误的是
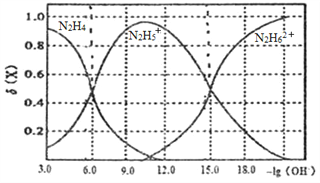
A. 反应N2H62++N2H4=2N2H5+的pK=90(已知pK=-lgK)
B. N2H5Cl溶液中存在:c(Cl-)+c(OH-)=c(N2H5+)+2c(N2H62+)+c(H+)
C. N2H5Cl溶液中c(H+)>c(OH-)
D. Kb1(N2H4)=10-6
【答案】A
【解析】
A.根据电离平衡常数概念结合图像计算;
B.根据电荷守恒分析;
C.根据N2H5+水解分析;
D. 根据电离平衡常数概念结合图像计算。
A、由N2H5+的电离方程式N2H5++H2O![]() N2H62++OH-可得Kb2(N2H4)=
N2H62++OH-可得Kb2(N2H4)=![]() ,则Kb1(N2H4)/Kb2(N2H4)=
,则Kb1(N2H4)/Kb2(N2H4)=![]() ,即为反应N2H62++N2H4=2N2H5+的K=Kb1(N2H4)/Kb2(N2H4)=
,即为反应N2H62++N2H4=2N2H5+的K=Kb1(N2H4)/Kb2(N2H4)=![]() ,所以pK= -9.0,A错误;
,所以pK= -9.0,A错误;
B、N2H5C1溶液中存在的电荷守恒为c(Cl-)+c(OH-)=c(N2H5+)+2c(N2H62+)+c(H+),B正确。
C、N2H5C1溶液中因N2H5+的水解使溶液呈酸性,所以c(H+)>c(OH-),C正确;
D、由图象可知当-lg(OH-)=6时,N2H4和N2H5+的物质的量分数相等,可推知其浓度相等,由N2H4的电离方程式N2H4+H2O![]() N2H5++OH-,得Kb1(N2H4)=
N2H5++OH-,得Kb1(N2H4)=![]() ,D正确;答案选A。
,D正确;答案选A。


科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素,它们在周期表中位置如图所示,下列说法不正确的是( )

A. W、Y、X三种元素的原子半径依次减小
B. Z元素的气态氢化物的热稳定性比Y的高
C. W元素与氢元素可能会形成W2H6
D. Y元素的单质能从NaZ溶液中置换出Z元素的单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物如NH3及铵盐、N2H4、N2O4等在中学化学、化工工业、国防等领域占有重要地位。
(1)发射航天火箭常用肼(N2H4)与N2O4作燃料与助燃剂。肼(N2H4)与N2O4的反应为2N2H4(1)+N2O4(g)=3N2(g)+4H2O(g) △H = -1077 kJ/mol
已知相关反应的化学键键能数据如下:
![]()
则使1 mol N2O4(g)分子中化学键完全断裂时需要吸收的能量是__________ 。
(2)N2O4与NO2之间存在反应N2O4(g)![]() 2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度的变化如图所示。
2NO2(g)。将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度的变化如图所示。
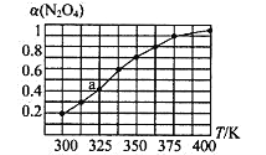
①由图推测该反应△H_______0(填“>”或“<”),理由为______________ 。
②图中a点对应温度下,己知N2O4的起始压强p0为108 kPa,则该温度下反应的平衡常数为:Kp=_____________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,取四位有效数字)。
③在一定条件下,该反应N2O4、NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1p(N2O4),v(NO2)=k2p2(NO2),其中k1、k2是与反应温度有关的常数。相应的速率-压强关系如图所示,一定温度下,k1、k2与平衡常数Kp的关系是k1=________,在下图标出的点中,能表示反应达到平衡状态的点为______。

(3)电解NO2制备NH4NO3,其工作原理如图所示。
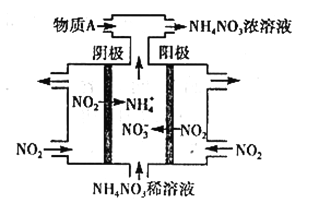
①阳极的电极反应式为_______________________。
②为使电解产物全部转化为NH4NO3,需补充物质A,则A的化学式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2 mol Na2O2与2mol NaHCO3固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是
A. NaOH和Na2CO3 B. NaOH
C. Na2CO3 D. NaOH、Na2O2和Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg和Al的混合物投入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示。则下列说法正确的是( )

A. Mg和Al的总质量为8g B. 硫酸的物质的量浓度为5mol/L
C. NaOH溶液的物质的量浓度为5mol/L D. 生成的H2在标准状况下的体积为11.2L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)(CH3)2CHCH(CH3)2的系统命名为___________________;
(2)有机物的结构可用“键线式”简化表示,CH3-CH=CH-CH3的键线式为________;
(3)下列化合物分子中,在核磁共振氢谱图中能给出一种信号的是(______)
A.CH3CH2CH3 B. CH3COCH2CH3 C.CH3CH2OH D.CH3OCH3
(4)分子式为C2H6O的有机物,有两种同分异构体,乙醇(CH3CH2OH)、甲醚(CH3OCH3),则通过下列方法,不可能将二者区别开来的是 (______)
A.红外光谱 B. 1H核磁共振谱 C.质谱法 D.与钠反应
(5)已知乙烯分子是平面结构, 1,2-二氯乙烯可形成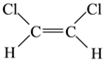 和
和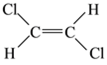 两种不同的空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是(_____)
两种不同的空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是(_____)
A.1-丙烯 B.4-辛烯 C.1-丁烯 D.2-甲基-1-丙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)现有下图所示A、B、C、D四种仪器,写出名称:
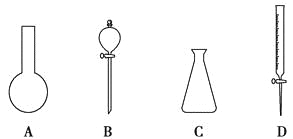
A. ,B. ,
C. ,D. 。
(2)“磨砂”是增加玻璃仪器密封性的一种处理工艺,可使仪器不漏液或不漏气。在下列仪器中:①试管;②分液漏斗;③细口试剂瓶;④广口试剂瓶;⑤集气瓶;⑥滴瓶;⑦酸式滴定管;⑧碱式滴定管,肯定用不到“磨砂”处理的有 (填序号)。
(3)以下是中学化学实验中常见的定量仪器:
a.量筒 b.容量瓶 c.滴定管 d.托盘天平
①其中标有仪器使用温度的是 (填编号)。
②实验时用来精确量取液体体积的是 (填编号)。
③使用前要检查仪器是否漏液的是 (填编号)。
(4)玻璃棒的作用主要有以下四种:①搅拌、②引流、③蘸取溶液、④转移固体。不同实验中其作用可能不完全相同,请回答下列问题:
A.在“用无水碳酸钠配制100 mL 0.12 mol·L-1的碳酸钠溶液”的实验中,玻璃棒的作用是 (填写编号)。
B.在“用氢氧化钠溶液、碳酸钠溶液、氯化钡溶液、盐酸、水等试剂除去粗盐中的Mg2+、Ca2+、SO42-等杂质离子以制得纯净的食盐”的实验中玻璃棒的作用可能是 (填写编号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 加入铝粉能产生H2的溶液中,可能存在大量的Na+、Ba2+、AlO2-、NO3-
B. 某温度下,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液一定显中性
C. 向苯和少量苯酚的混合溶液中加入适量浓溴水,过滤,可除去苯中少量苯酚
D. 已知I3-![]() I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大
I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)向偏铝酸钠溶液中滴入1~2滴酚酞溶液,溶液显____色,用离子方程式表示原因________。
(2)Fe(OH)3胶体可用作净水剂,取少量Fe(OH)3胶体于试管中,向试管中逐渐滴加稀盐酸至过量,现象为_________________________
(3)已知:5NH4NO3![]() 2HNO3+4N2↑+9H2O,则该反应中氧化产物与还原产物的质量比为______。
2HNO3+4N2↑+9H2O,则该反应中氧化产物与还原产物的质量比为______。
(4)有机物CH3CH(C2H5)CH(C2H5)CH(CH3)2系统命名法命名为 ______________________
(5)邻甲基苯甲酸( )有多种同分异构体,其中属于酯类,但分子结构中含有甲基和苯环的异构体有____________种
)有多种同分异构体,其中属于酯类,但分子结构中含有甲基和苯环的异构体有____________种
(6)甲酸和甲醇发生酯化反应方程式______________________________________________
(7)![]() 与足量NaOH溶液反应的化学方程式______________;
与足量NaOH溶液反应的化学方程式______________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com