
分析 (1)根据中和热测定的实验步骤选用需要的仪器烧杯(大小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、量筒、酸、碱溶液、温度计和环形玻璃搅拌棒,然后判断还缺少的仪器;
(2)醋酸是弱酸,电离过程需要吸热,中和反应是放热的,焓变是负值;
(3)根据中和热的计算公式△H=Q=-cm△T来确定实验中需要的数据.
解答 解:(1)中和热测定的实验步骤选用需要的仪器有:烧杯(大小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、量筒、盐酸、NaOH溶液、温度计和环形玻璃搅拌棒,
故答案为:温度计和环形玻璃搅拌棒;
(2)醋酸是弱酸,电离过程需要吸热,但中和反应是放热的,焓变是负值,若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会比(1)测出的△H偏大,
故答案为:偏大;
(3)根据反应热的计算公式△H=Q=-cm△T可知,酸碱反应的中和热计算时,至少需要的数据有:比热容c、反应后溶液的质量以及生成水的物质的量m、反应前后温度,根据反应前后的温度获得反应前后温度变化△T,故选C.
点评 本题考查学生中和热的测定实验知识,属于教材知识的考查,较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 1mol氯气参加氧化还原反应,转移的电子数一定为2 NA | |
| B. | 0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3NA | |
| C. | 常温常压下,44g二氧化碳分子中所形成的共用电子对数为4NA | |
| D. | 常温常压下,1.6gO2和O3混合气体中质子总数为0.8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol苯乙烯中含有的C=C数为4NA | |
| B. | 1mol甲醇中含有C-H键的数目为4NA | |
| C. | 0.1molCnH2n+2中含有的C-C键数为0.1NA | |
| D. | 1molC4H10中含有共用电子对数是13NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 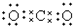 | B. | K+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$H]- | ||
| C. | 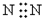 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①②④⑤ | C. | ②④ | D. | ④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | C2H6 | B. | C4H8 | C. | C3H8 | D. | C3H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
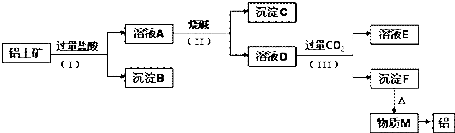
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com