
【题目】常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL的溶液含NaOH 1mol/L,然后滴加1mol/L的盐酸,测得生成沉淀的质量与消耗盐酸的体积关系如
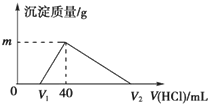
A. 原合金质量为0.92g B. 图中V2的值为60
C. 图中m的值为1.56 D. 产生氢气的体积为896mL(标准状况下)
【答案】C
【解析】
试题由图象可知,向合金溶解后的溶液中加盐酸,先发生NaOH+HCl═NaCl+H2O,后发生NaAlO2+HCl+H2O═NaCl+Al(OH)3↓,最后发生Al(OH)3↓+3HCl═AlCl3+3H2O,合金溶解后剩余的氢氧化钠的物质的量为0.02L×1mol/L=0.02mol,
由NaOH+HCl═NaCl+H2O,
0.02mol 0.02mol
则V1为![]() =0.02L=20mL,
=0.02L=20mL,
生成沉淀时消耗的盐酸为40mL-20mL=20mL,其物质的量为由0.02L×1mol/L=0.02mol,
由NaAlO2+HCl+H2O═NaCl+Al(OH)3↓,
0.02mol 0.02mol 0.02mol
A、由钠元素及铝元素守恒可知,合金的质量为0.04mol×23g/mol+0.02mol×27g/mol=1.46g,故A错误;B、由Al(OH)3↓+3HCl═AlCl3+3H2O可知,溶解沉淀需要0.06molHCl,其体积为60mL,则V2为40mL+60mL=100mL,故B错误C、由上述计算可知,生成沉淀为0.02mol,其质量为0.02mol×78g/mol=1.56g,故C正确;D、由2Na+2H2O═2NaOH+H2↑、2Al+2H2O+2NaOH═2NaAlO2+3H2↑,生成氢气的物质的量为0.02mol+0.03mol=0.05mol,其标况下的体积为0.05mol×22.4L/mol=1.12L,故D错误;故选C。


科目:高中化学 来源: 题型:
【题目】现有六种短周期元素,原子序数逐渐增大。请根据以下信息,用元素符号回答下列问题:
L | 原子中只有一个电子 |
M | 原子的最外层电子数是次外层电子数的2倍 |
N | 地壳中含量最多的元素 |
Q | 所在的周期数是族序数的3倍 |
R | R2+具有与氖原子相同的电子层结构 |
T | 最高正化合价与最低负化合价的代数和为6 |
(1)写出这两种元素的名称:M_________、Q________。
(2)T在周期表中的位置是______,T的原子结构示意图为_______,T的最高价氧化物对应水化物的化学式为_______。
(3)上述六种元素中原子半径最大的是__________,非金属性最强的是____________。
(4)写出MN2的电子式_________,用电子式表示化合物RT2的形成过程:______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组构想将汽车尾气(NO、NO2)转化为重要的化工原料HNO3,其原理如图所示,其中A、B为多孔材料.下列说法正确的是
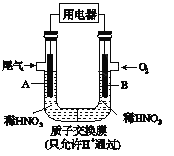
A. 电极A表面反应之一为NO2-e-+H2O= NO3_+2H+
B. 电极B附近的c(NO3_)增大
C. 电解质溶液中电流的方向由B到A,电子的流向与之相反
D. 该电池工作时,每转移4mol电子,消耗22.4L O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的数值,下列说法正确的是
A. 1molCO2与SO3的混合气体氧原子数为2NA
B. 1mol/L KClO3溶液中含有NA个ClO3﹣
C. 标准状况下,11.2LCCl4所含的分子数为0.5NA
D. 25℃,1.01×105Pa,88gCO2中所含原子数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单斜硫和正交硫转化为二氧化硫的能量变化如下图所示。下列说法正确的是( )

A. 由图可知,单斜硫转化为正交硫的反应为吸热反应
B. 正交硫比单斜硫性质活泼
C. 相同条件下,等量的正交硫比单斜硫所含有的能量低
D. 相同条件下,生成等量的二氧化硫气体,正交硫放出的热量多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的检验方法正确的是( )
A. 向某无色溶液中滴加氯化钡溶液,产生白色沉淀,再加入稀盐酸后该沉淀不溶解,说明原溶液中一定含有SO![]()
B. 将某白色固体粉末与氢氧化钠浓溶液共热,产生能使湿润的红色石蕊试纸变蓝的气体,证明原固体中一定含有NH![]()
C. 向某白色固体粉末中滴加稀盐酸,产生能使澄清石灰水变浑浊的气体,则原固体粉末中一定含有CO![]() 或HCO
或HCO![]()
D. 某溶液能使淀粉碘化钾溶液变蓝,则该溶液一定为氯水或者溴水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】373K时把0.24 mol无色的N2O4气体通入体积500 mL的密闭容器中,发生反应:N2O4![]() 2NO2,容器中立即出现红棕色。反应进行到2s时,测得生成NO2的物质的量为0.04 mol;反应进行到60 s时达到平衡,此时容器内N2O4与NO2的物质的量相等。请计算:(本小题要求写出解过程)
2NO2,容器中立即出现红棕色。反应进行到2s时,测得生成NO2的物质的量为0.04 mol;反应进行到60 s时达到平衡,此时容器内N2O4与NO2的物质的量相等。请计算:(本小题要求写出解过程)
①开始2 s内以N2O4表示的化学反应速率______;
②达到平衡时体系的压强与开始时体系的压强之比______;
③N2O4的平衡转化率______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:①Cl2+2KBr=2KCl+Br2, ②KClO3+6HCl=3Cl2+KCl +3H2O,
③2KBrO3+Cl2=Br2+ 2KClO3,下列说法正确的是
A. 上述三个反应都有单质生成,所以都是置换反应
B. 氧化性由强到弱顺序为 KBrO3>KClO3>Cl2>Br2
C. 反应②中还原剂与氧化剂的物质的量之比为6:1
D. ③中lmol还原剂反应则氧化剂得到电子的物质的量为2mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com